
Mengurutkan benda dari yang besar ke kecil Artofit
Urutan kelarutan senyawa tersebut dari yang besar ke yang kecil adalah.. 1, 4, 3, dan 2.. 100 mL NaOH 1,8 M + 100 mL CH 3 COOH 1,8 M ke dalam larutan garam uji terbentuk. timbal azida Pb(N 3) 2 dan strontium fluorida (SrF 2) adalah sama besar pada temperatur yang sama. Jika kelarutan dinyatakan denagn s, maka pada temperatur yang.

Nama IUPAC dan rumus struktur yang tepat dari senyawa den...
Kelarutan suatu zat dapat ditinjau dari nilai zat tersebut. Semakin besar nilai , semakin besar kelarutan suatu zat atau sukar mengendap, sebaliknya, semakin kecil nilai , maka semakin kecil juga kelarutan suatu zat dan cenderung mudah mengendap.. Berdasarkan data nilai di soal, maka urutan kelarutan senyawa tersebut dari yang terbesar ke yang terkecil adalah (2), (1), (4), (3).

Kenaikan Titik Didih Penurunan Titik Beku Sifat Koligatif Larutan Reverasite
Hubungan Kelarutan (s) dan Tetapan Hasil Kali Kelarutan (K sp) Kelarutan dari suatu zat dapat berubah bergantung pada beberapa faktor. Misalnya, kelarutan dari senyawa hidroksida seperti Mg (OH) 2, bergantung pada pH larutan. Kelarutan zat juga dipengaruhi oleh konsentrasi ion-ion lain dalam larutan, khususnya ion-ion senama.

Pada suhu 25oC Ksp Ni(OH)2 = 6 x 1018. Hitunglah kelarutan Ni(OH)2 pada a. Larutan NaOH 0,001
Sehingga, urutan kelarutan garam sulfat alkali yang benar adalah: MgSO4. CaSO4. SrSO4. BaSO4. Adapun, dalam urutan tersebut tidak terdapat garam sulfat berilium. Dilansir dari Chemistry LibreTexts, hal tersebut dikarenakan berilium sulfat (BeSO4) tidak dapat larut dalam air. Dapatkan update berita pilihan dan breaking news setiap hari dari.
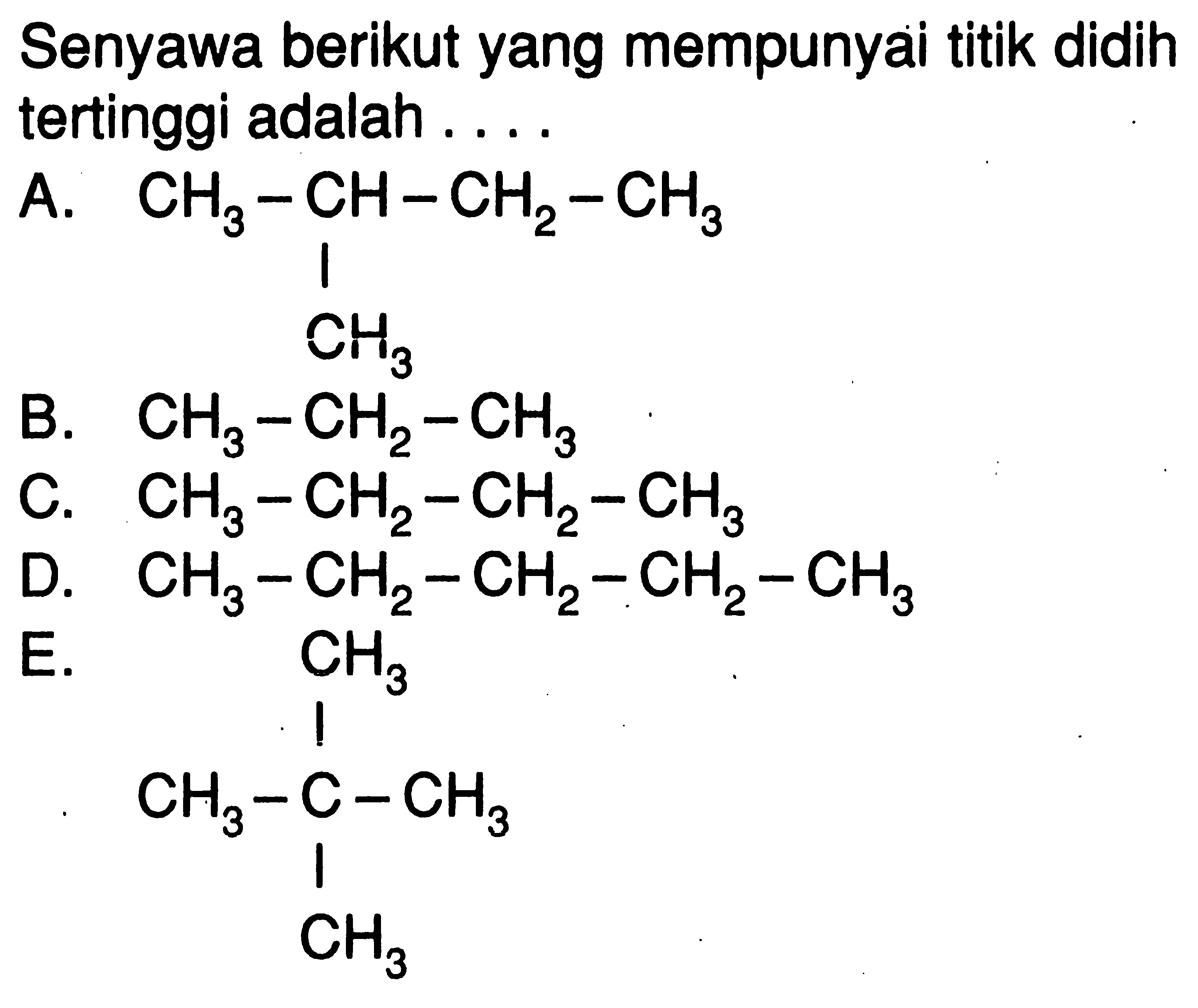
Senyawa berikut yang mempunyai titik didih tertinggi adal...
Tetapan Hasil Kali Kelarutan atau Ksp dapat didefiniskan sebagai hasil kali konsentrasi ion-ion dari larutan yang sukar larut larut dalam pelarut tertentu. hubungan Kelarutan (s) dengan Tetapan Hasil Kali Kelarutan (Ksp) yaitu semakin kecil nilai kelarutan suatu zat maka zat tersebut semakin sukar larut dalam pelarutnya, sehingga nilai Ksp-nya.
Di Antara Senyawa Berikut Ini Yang Kelarutannya Paling Besar Di Dalam My XXX Hot Girl
Kelarutan dan Hasil Kali Kelarutan. Berikut ini beberapa garam dan Ksp nya: (1) Cu (OH)2, Ksp=2,6 x 10^ (-19) (2) Fe (OH)2, Ksp=8,0 x 10^ (-16) ; (3) Pb (OH)2, Ksp=1,4 x 10^ (-20) ; dan (4) Mg (OH)2, Ksp=1,8 x 10^ (-11) . Urutan kelarutan senyawa tersebut dari yang kecil ke besar adalah..

Tabel kelarutan garam dalam air 2021
Mengutip e-modul Kimia: Peranan Elektrolit dalam Tubuh (2017) yang diterbitkan Kemdikbud, definisi larutan adalah campuran homogen yang tersusun dari pelarut dan zat terlarut. Secara umum larutan kerap dikenal dalam bentuk zat cair. Namun, sebenarnya larutan juga bisa berbentuk gas dan padat. Contoh larutan berupa gas adalah gas nitrogen.

Diketahui harga hasil kali kelarutan (Ksp) dari senyawas...
Jadi, urutan kelarutan senyawa dari yang besar ke yang kecil adalah 2, 3, 4, dan 1 (B). Soal Kelarutan dan Hasil Kali Kelarutan UN 2013 Sebanyak 100 mL larutan MgCl 2 0,4 M ditambahkan ke dalam 100 mL larutan Na 2 CO 3 0,4 M. Besarnya massa zat yang mengendap jika diketahui K sp MgCO 3 = 3 × 10 −8 dan A r Mg = 24, C = 12, O =16 adalah..

Contoh Contoh Unsur Senyawa Dan Campuran
Di artikel kali ini, Quipperian akan diajak untuk mempelajari kelarutan suatu senyawa, mulai dari senyawa larut sampai terjadinya endapan. Daftar Isi Sembunyikan. Kelarutan Garam. Pengertian Kelarutan (s) Tetapan Hasil Kali Kelarutan (Ksp) Hubungan antara Kelarutan dan Tetapan Hasil Kelarutan. Contoh soal 1. Pengaruh Ion Senama pada Kelarutan.

Kelarutan dan ksp soal kimia SMA YouTube
47 Urutan tingkat kepolaran pelarut organik. Tabel Urutan Tingkat Kepolaran Pelarut Organik No. Pelarut Rumus Kimia Tingkat Kepolaran Densitas (g/mL) 1. Sikloheksana C6H12 0,006 0,7739 2. Pentana C5H12 0,009 0,626 3. Heksana C6H14 0,009 0,659 4. Heptana C7H16 0,012 0,684 5. Karbon Tetraklorida CCl4 0,052 1,594 6. Karbon Disulfida CS2 0,065 1,594 7. p-Silena C8H10 0,074

Mengurutkan Gambar Dari Kecil Kebesar
Multiple Choice. 2 minutes. 1 pt. Berikut ini beberapa garam dan Ksp nya: (1) Cu (OH) 2, Ksp = 2,6 × 10 −19. (2) Fe (OH) 2, Ksp = 8,0 × 10 −16. (3) Pb (OH) 2, Ksp = 1,4 × 10 −20; dan. (4) Mg (OH) 2, Ksp = 1,8 × 10 −11. Urutan kelarutan senyawa tersebut dari yang kecil ke besar adalah.

Diberikan beberapa larutan garam dan K_( {spnya sebagai...
Pengertian Kelarutan. Sebelum masuk ke apa itu kelarutan, elo harus tahu dulu yang dimaksud dengan larutan. Larutan merupakan campuran homogen yang terdiri dari dua atau lebih. Zat ini dinamakan sebagai zat terlarut dan pelarut. Nah, contohnya adalah garam dan air. Garam merupakan zat terlarut, sedangkan air adalah pelarut.

Alkana Tergolong Senyawa Hidrokarbon Senang Belajar
Pahami bahasan kelarutan. Molekul air (H 2 O) memiliki struktur yang tidak biasa sehingga mirip dengan magnet. Salah satu ujung memiliki muatan positif, sementara ujung lainnya bermuatan negatif. Apabila senyawa ionik dimasukkan ke dalam air, "magnet" air akan mengelilinginya dan mencoba untuk menarik serta memisahkan ion-ion positif dan negatif.

Berdasarkan Gambar Nama Senyawa Yang Dihasilkan Dari Reaksi Tersebut Adalah
Hubungan Antara Kelarutan dan Ksp. Pada larutan jenuh senyawa ion A x B y, konsentrasi zat di dalam larutan sama dengan harga kelarutannya dalam satuan mol/L. Senyawa A x B y yang terlarut akan mengalami ionisasi dalam sistem kesetimbangan. Jika harga kelarutan dari senyawa A x B y sebesar s M, maka di dalam reaksi kesetimbangan tersebut konsentrasi ion-ion dan ionnya adalah sebagai berikut :

Rumus Kelarutan S My XXX Hot Girl
Tabel di bawah ini memberikan informasi tentang variasi kelarutan berbagai zat dalam air (kebanyakan senyawa anorganik), berdasarkan variasi temperatur, pada tekanan 1 atmosfer.Satuan kelarutan dinyatakan dalam gram per 100 mililiter air (g/100 mL), kecuali disebutkan lain. Zat-zat tersebut tercantum sesuai urutan abjad. Isi

Pengertian dan Contoh Senyawa Tata Cara Penulisan Senyawa Contoh Senyawa dan Manfaatnya
Kelarutan Garam. Garam merupakan senyawa ionik yang umumnya dihasilkan dari reaksi netralisasi asam-basa. Garam terdiri dari kation (ion bermuatan positif) selain H + dan anion (ion bermuatan negatif) selain OH − dan O 2−. Kelarutan dari garam berbeda-beda tergantung pada jenis ion penyusunnya. Ada garam yang mudah larut dalam air seperti.