
Contoh Asam Basa Menurut Bronsted Lowry Berbagai Contoh Riset
Merupakan senyawa yang terbentuk dari reaksi asam dan basa. Reaksi pembentukan garam adalah: Asam + basa → garam + air HCl + KOH → KCl + H2O Garam dapur (NaCl) diperoleh dari air laut yang mengalami penguapan dan kristalisasi. Untuk menjadikannya garam beryodium, harus diproses iodisasi (garam kalium/KI). Sifat-sifat atau ciri-ciri garam:

tuliskan nama yang tepat sesuai dengan aturan tata nama IUPAC untuk senyawasenyawa berikut
Cara Membedakan Asam dan Basa. Senyawa asam dapat dengan mudah ditemukan pada buah-buahan, seperti jeruk dan lemon. Selain itu, bisa juga ditemukan pada bahan makanan, seperti cuka. Bahkan, senyawa asam juga banyak digunakan sebagai bahan pengawet makanan lho, misalnya asam benzoat yang dimanfaatkan sebagai pengawet jus buah dan selai.

Pasangan persamaan reaksi hidrolisis yang bersifat basa adalah Universityku
1. Apa yang kamu ketahui tentang larutan basa! Jawaban: Senyawa basa adalah senyawa yang memiliki tingkat keasaman atau pH di atas 7. pH adalah singkatan dari Power of Hydrogen, yang merupakan sebuah derajat keasaman untuk mengukur tingkat keasaman suatu larutan. Senyawa basa mengandung ion OH- dan adanya ion OH- inilah yang menyebabkan sabun.

15+ Contoh Soal Tata Nama Senyawa Asam Dan Basa Contoh Soal Terbaru
Sementara basa adalah zat yang menghasilkan ion hidroksida (OH-) dalam larutan. Asam dan basa dapat bereaksi menghasilkan air serta senyawa ionic garam. Reaksi itu disebut reaksi netralisasi. Asam dan basa merupakan dua jenis larutan yang kerap digunakan dalam kehidupan sehari-hari manusia. Asam dan basa ada yang memiliki sifat kuat dan juga lemah.

Spesi berikut yang berperan sebagai basa Lewis adalah.
Sementara basa adalah semua zat yang jika dilarutkan dalam air akan menghasilkan ion OH-, misalnya pada senyawa natrium hidroksida NaOH akan terurai menjadi Na+ dan OH-. Jika basa bereaksi dengan asam, maka dihasilkan senyawa 'garam'. Definisi basa menurut Arrhenius adalah senyawa yang jika dilarutkan dalam H2O atau air maka akan terurai jadi ion OH- (ion hidroksida).

Pasangan persamaan reaksi hidrolisis yang bersifat basa adalah Universityku
Sedangkan, basa lemah adalah senyawa yang apabila dilarutkan di dalam air akan sulit melepaskan ion OH- dan mengalami disosiasi dalam larutan.. Contoh Asam dan Basa. Berikut ini adalah beberapa contoh asam dan contoh basa: Asam. Asam klorida (HCl) Asam nitrat (HNO 3) Asam sulfat (H 2 SO 4) Asam fosfat (H 3 PO 4) Asam borat (H 3 BO 3)

Senyawa Hidrokarbon Alifatik Jenuh Memiliki Rumus Molekul ? Blog Ilmu Pengetahuan
Ini Dia Daftar Senyawa yang Bersifat Asam. Seperti yang telah sobat ketahui, senyawa elektrolit adalah senyawa yang bisa menghantarkan arus listrik. Terdapat dua jenis senyawa elektrolit yaitu elektrolit kuat dan elektrolit lemah. Untuk sifat dari senyawa elektrolit sendiri dibagi menjadi tiga macam yaitu asam, basa, dan garam.

Cara Menentukan Senyawa Bersifat Asam Basa Atau Netral Digunakan
Dijelaskan dalam Jurnal UNY, teori Arrhenius menyimpulkan: 1. Asam: zat/senyawa yang dapat menghasilkan H+ dalam air. HCl (aq) à H+ (aq) + Cl - (aq) 2. Basa: zat/senyawa yang dapat menghasilkan OH- dalam air. NaOH (aq) à Na+ (aq) + OH - (aq) • Reaksi netralisasi adalah reaksi antara asam dengan basa yang menghasilkan garam:

Cara Menentukan Senyawa Bersifat Asam Basa Atau Netral Digunakan
Terner. Ba (OH)2. Barium hidroksida. Kuat. Terner. Demikian postingan mafia online mengenai daftar senyawa basa. Jika ada penulisan rumus kimia, nama senyawa, kekuatan basa maupun jenis senyawa yang keliru, tolong diberitahukan dengan cara berkomentar. Jika anda menemukan senyawa basa selain yang ada di dalam tabel di atas tolong diberitahu juga.

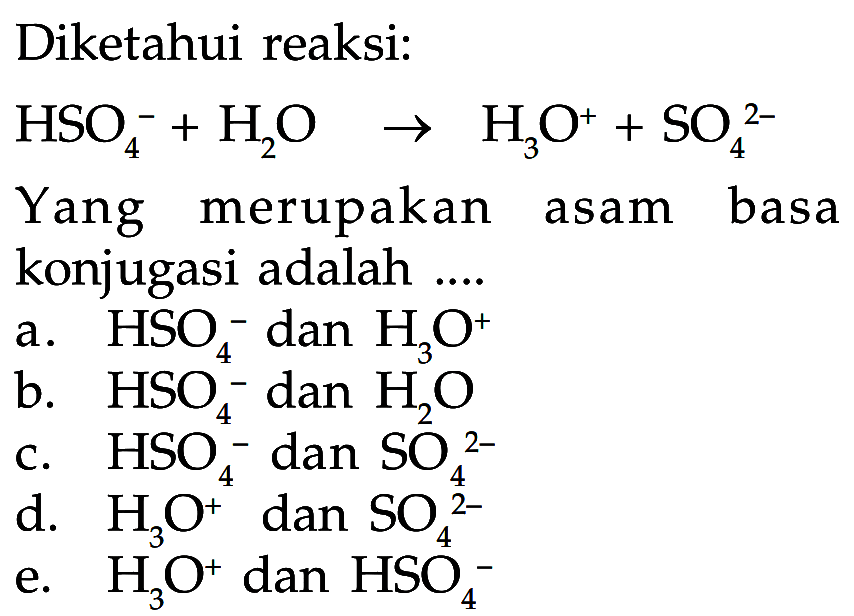
LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Untuk masing-masing ulasan mengenai basa kuat dan basa lemah akan dijelaskan dalam daftar senyawa bersifat basa berikut ini. Daftar Senyawa Bersifat Basa Kuat. Sebelum menginjak pembahasan mengenai daftar senyawa yang bersifat basa kuat secara lengkap, alangkah baiknya jika sobat mengetahui apa itu basa kuat. Basa kuat adalah sebuah senyawa.

Perhatikan rumus struktur senyawa hidrokarbon berikut!CH3...
Pengertian zat amfoter. Istilah amfoter berasal dari Bahasa Yunani "amphoteros" atau "amphoteroi" yang berarti "masing-masing" atau "keduanya". Istilah tersebut digunakan karena zat atau senyawa amfoter adalah senyawa yang dapat bersifat asam sekaligus basa. Dilansir dari Encyclopedia Britannica, zat amfoter adalah suatu zat.

Teori Asam Basa
Jika senyawa oksida basa direaksikan dengan air akan dihasilkan basa: Na2O + H2O --> 2NaOH. K2O + H2O --> 2KOH. CaO + H2O --> Ca (OH)2. Meskipun dari semua oksida basa ada hidroksidanya, namun yang dapat bereaksi langsung dengan air hanyalah Na2O, K2O, CaO, SrO, dan BaO. Berikut disajikan tabel oksida basa.
Senyawa berikut ini yang merupakan contoh asam poliprotik...
Senyawa basa memiliki nilai derajat keasaman (pH) lebih dari 7. Sifat-sifat Basa. Sebagaimana halnya sifat asam, maka basa pun memiliki beberapa sifat yang dapat digunakan untuk pengidentifikasian. Berikut ini adalah beberapa sifat basa dan penjelasannya. 1. Pahit dan terasa licin di kulit. Mengapa sabun terasa licin ketika disentuh? Rasa licin.

Berikut ini adalah contoh senyawa basa menurut Arrhenius,...
Alkaloid adalah sebuah golongan senyawa basa bernitrogen yang. untuk menyebut berbagai senyawa yang diperoleh dari ekstraksi tumbuhan yang bersifat basa (pada waktu itu sudah dikenal, misalnya, morfina, striknina, serta solanina). Hingga sekarang dikenal sekitar 10.000 senyawa yang tergolong alkaloid dengan struktur sangat beragam, sehingga.

Teori Asam Basa
Basa kuat adalah adam love Valen sederhana yang dapat mendeprotonasi asam sangat lemah di dalam reaksi asam-basa. Contoh paling umum dari basa kuat adalah hidroksida dari logam alkali dan logam alkali tanah seperti NaOH dan Ca(OH) 2. Berikut ini adalah daftar basa kuat: Kalium hidroksida (KOH) Barium hidroksida (Ba(OH) 2) Cesium hidroksida (CsOH)

Contoh Asam Organik Dan Contoh Senyawa Basa Dan Contoh Riset
Basa = penerima H+. Reaksi kimia yang bisa dijadikan contoh berdasarkan teori Bronsted-Lowry misalnya pada asam klorida (HCL) dan air (H2O) berikut ini: HCl + H2O ⇌ H3O+ + Cl-. Penjelasannya seperti mengutip pada emodul Kemdikbud: HCL bersifat asam karena itu ia mendonorkan ion H+ nya kepada H20. H20 bersifat basa karena ia menerima donor H+.