
Firstwisnu Media Kenaikan Titik Didih Dan Penurunan Titik Beku Larutan Reverasite
Dapatkan Modul, Rumus, & Soal Sifat Koligatif Larutan lengkap di Wardaya College.. Demikian pula pada penurunan titik beku larutan, tekanan uap larutan juga lebih rendah daripada tekanan uap pelarut murni. Sehingga agar larutan membeku, harus didinginkan ke suhu yang lebih rendah akibatnya titik beku larutan lebih rendah dari titik beku.
Larutan berikut yang memiliki titik beku paling tinggi ad...
1. Titik Beku (Tf) Jadi begini , proses pembekuan itu terjadi ketika suatu zat telah mencapai titik beku. Titik beku ( Tf) akan tercapai apabila temperatur saat tekanan uap zat padat, sama dengan tekanan uap zat cair. Jika kalian mengetahui bahwa titik beku air sebesar 0ºC, itu artinya tekanan uap air dalam bentuk cair pada temperatur 0ºC.

Kenaikan Titik Didih Larutan Pengertian Dan Rumus Materiipa Com My XXX Hot Girl
Ket: ΔT f = penurunan titik beku larutan (°C) m = molalitas (m) K f = tetapan penurunan titik beku molal (°C m-1) n = jumlah ion elektrolit α = derajat ionisasi/disosiasi. 3. Kenaikan Titik Didih (ΔT b). Sederhananya seperti ini. Saat zat pelarut (misalnya air) dipanaskan hingga menguap, partikel pelarut tersebut bergerak sangat cepat hingga berubah menjadi face gas.

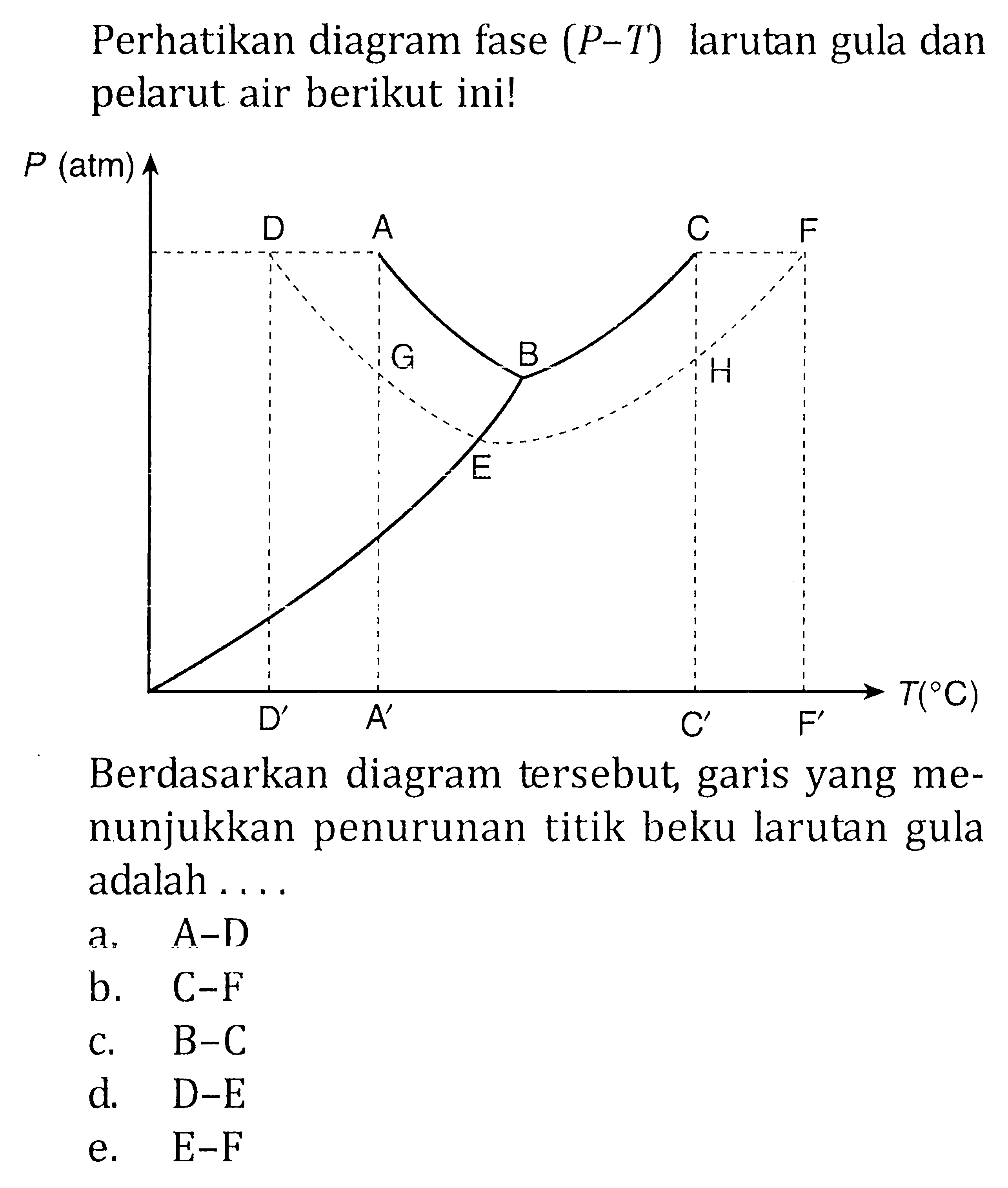
Perhatikan diagram PT air, larutan urea 0,1 m dan NaC...
Pengertian dan Rumus Penurunan Titik Beku Menurut Rananda Vinsiah dalam Fenomena Sifat Koligatif Larutan Kimia Kelas XII (2020, hlm. 19), titik beku merupakan kondisi ketika tekanan uap suatu cairan sama dengan tekanan padatannya. Pada kondisi seperti itu, cairan akan mulai membeku. Seandainya ada suatu zat terlarut yang dicampurkan ke pelarut murni, akan tercipta larutan baru.

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Penurunan titik beku adalah selisih antara titik beku pelarut dengan titik beku larutan. Penurunan titik beku ini termasuk salah satu sifat koligatif larutan. Dalam perhitungan kimia, penurunan titik beku disimbolkan dengan ΔT f (f berasal dari kata freeze) atau ΔT b . Peristiwa penurunan titik beku ini sering diterapkan pada negara-negara.

Penurunan Titik Beku Larutan Definisi Dan Penyebabnya Reverasite
Rumus dan Perhitungan Penurunan Titik Beku. Perhatikan bahwa dalam kasus senyawa kovalen atau molekul non-elektrolit, nilai faktor van't Hoff (i) biasanya adalah 1, karena senyawa ini tidak mengionisasi dalam larutan.. Sebagai hasil dari penurunan titik beku, larutan non-elektrolit akan memiliki titik beku yang lebih rendah daripada titik.

Menentukan Rumus Molekul Senyawa dari Penurunan Titik Beku YouTube
Contoh Soal Penurunan Titik Beku - Membahas mengenai perhitungan suatu proses kimia terkait zat berbentuk larutan. Dimana reaksi penurunan titik beku tersebut terjadi pada saat suatu larutan saat ditambahkan senyawa lain. Jika dilihat dari sudut pandang ilmu kimia, larutan mempunyai berbagai sifat baik dalam bentuk sifat kimia ataupun sifat fisis.. Dimana salah satu materi sifat fisis.

Berikut disajikan data percobaan tentang titik beku beber...
Misalnya, titik beku normal air adalah 0 o C. Akan tetapi, dengan adanya zat terlarut pada suhu 0 o C, air bisa mejadi belum membeku. Selisih titik beku pelarut (Tf o) dengan titik beku larutan (Tf) yang kemudian disebut penurunan titik beku (ΔTf). Berikut rumus penurunan titik beku: ΔTf = Tf° - Tf

Rumus titik beku larutan
Artinya, penurunan titik beku adalah sifat koligatif larutan di mana titik bekunya lebih rendah daripada pelarut murni. Rumus penurunan titik beku. Besar penurunan titik beku didapat dari selisih antara titik beku pelarut dan titik beku larutan sebagai berikut: Dengan, ΔTf: penurunan titik beku Tf0: titik beku pelarut murni Tf: titik beku larutan

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Mengenal Rumus dan Contoh Soal Hukum Hess. ∆Tf = Tf (pelarut) - Tf (larutan) ∆Tf = m . Kf. Keterangan: ∆Tf = penurunan titik beku (freezing point depression) m = molalitas. Kf = tetapan penurunan titik beku (ºC kg/mol) Untuk mengaplikasikan rumus di atas, Anda bisa menyimak contoh soal di bawah ini agar meningkatkan pemahaman.

Contoh Soal Perbandingan Penurunan Titik Beku (Sifat Koligatif Larutan Elektrolit) YouTube
Rumus Perhitungan Penurunan Titik Beku. Penurunan titik beku (ΔTb) pada suatu larutan dapat dihitung menggunakan Rumus Colligative Properties, yang terkait dengan penambahan zat terlarut. Rumus ini didasarkan pada hukum Raoult dan dapat dinyatakan sebagai: ΔTb=i⋅Kb⋅mΔTb=i⋅Kb⋅m. Di mana:

Cara Menghitung Tetapan Penurunan Titik Beku Larutan (Kf) (UN Kimia 2018 No. 24) YouTube
Larutan yang dihasilkan atau campuran padatan-padatan tersebut memiliki titik beku lebih rendah daripada pelarut atau padatan murninya. Fenomena inilah yang menyebabkan air laut , (campuran garam [dan lainnya] dalam air) tetap cair pada suhu di bawah 0 °C (32 °F), titik beku air murni.

Larutan yang memiliki titik beku paling rendah adalah.
Penurunan titik beku larutan elektrolit. Rumus penurunan titik beku larutan elektrolit sebagai berikut: ΔT f = K f. m . {1 + (n - 1) α} Keterangan: n = jumlah ion; α = derajat ionisasi; Contoh soal dan pembahasan. Contoh soal 1. Sebanyak 2,4 gram urea (Mr = 60) dilarutkan dalam 50 gram air. Jika Kf air = 1,86 °C/m, tentukanlah titik beku.

Ppt Pembentukan Larutan Dan Konsentrasi Larutan Powerpoint Riset
tentukan titik didih dan titik beku larutan yang mengandung 18 gram glukosa , Mr 180 dalam 500 gram air. jika kb dan kf diketahui. sifat koligatif larutan..

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Non Elektrolit) YouTube
Meskipun sifat koligatif melibatkan larutan, sifat koligatif tidak bergantung pada interaksi antara molekul pelarut dan zat terlarut, tetapi bergatung pada jumlah zat terlarut yang larut pada suatu larutan. Sifat koligatif terdiri dari penurunan tekanan uap, kenaikan titik didih, penurunan titik beku, dan tekanan osmotik. 1. Penurunan Tekanan Uap.
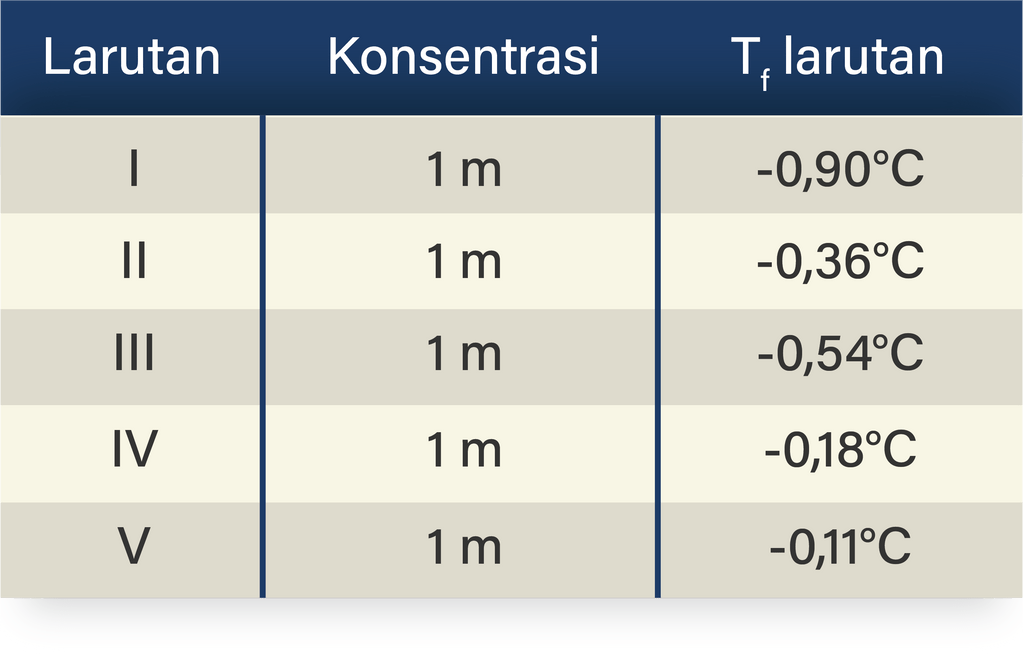
Berikut ini data titik beku beberapa larutan dalam...
Penurunan titik beku larutan bisa kamu cari dengan rumus ΔTf = m x Kf, dimana ΔTf adalah penurunan titik beku, m adalah molalitas larutan, dan Kf adalah tetapan penurunan titik beku molal. Kenaikan titik didih larutan selalu memiliki nilai yang lebih tinggi dari titik didih pelarut murninya. Hal ini disebabkan karena partikel dalam zat.