
PPT PEMBENTUKAN LARUTAN dan KONSENTRASI LARUTAN PowerPoint Presentation ID5586096
Hitung banyak air yang dibutuhkan dengan menggunakan rumus. V 1 × M 1 = (V 1 + X)M 2. 0,1 × 3 = (0,1 + X)0,5. 0,3/0,5 = 0,1 + X. 0,6 - 0,1 = X. 0,5 = X. Cara Konfigurasi Elektron Lambang Gas Mulia Beserta Contoh Soal. Jadi banyak air pelarut yang ditambahkan ke larutan sebanyak 0,5 Liter atau 500mL. Setelah mengetahui perhitungan banyak zat.

Perhitungan Konsentrasi Larutan Baku dan Larutan Uji yang Dibuat pada Prosedur GC YouTube
Setelah diencerkan, volumenya menjadi V2 liter, konsentrasi larutan M2 molar, dan mol zat terlarut = V2.M2 mol. Baca juga: Jenis Reaksi Kimia dalam Larutan Elektrolit. Rumus pengenceran larutan. Dikutip dari buku Rumus Lengkap Kimia SMA (2008) oleh Anwar Santoso, karena mol zat terlarut pada pengenceran tidak berubah, maka berlaku:
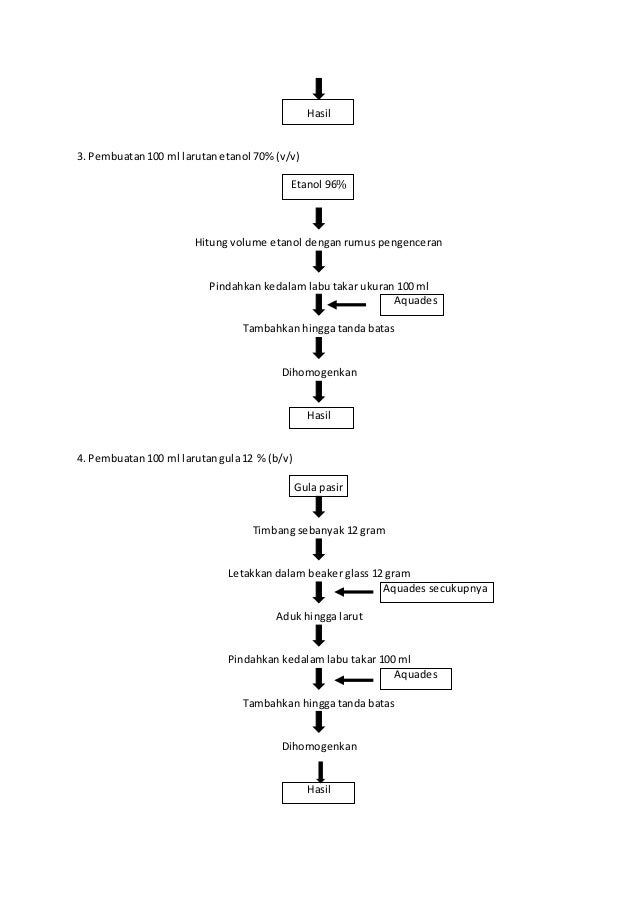
Diagram Alir Pembuatan dan Pengenceran Larutan
Kamu dapat menggunakan rumus pengenceran larutan untuk menghitung jumlah larutan yang perlu ditambahkan untuk mencapai konsentrasi yang diinginkan. Dengan memahami rumus ini, kamu dapat membuat larutan dengan konsentrasi yang tepat dan menghindari kesalahan dalam percobaan kimia. Semoga artikel ini bermanfaat dan sampai jumpa kembali di artikel.

Menghitung Pengenceran Larutan V1 M1 V2 M2 YouTube
Di soal tertulis bahwa larutan gula 2 M akan dijadikan 0,25 M. Artinya, ada penambahan air ke dalam larutan tersebut. Dengan rumus pengenceran, volume larutan setelah diencerkan dirumuskan sebagai berikut. Dengan demikian, volume air yang harus ditambahkan adalah sebagai berikut.

Molaritas Pengertian, Rumus, Pembuatan, Pengenceran Larutan Dan Contohnya Lengkap BprsKu.Co.Id
Rumus Pengenceran Larutan. Mengutip Buku Siswa Kimia SMA/MA Kelas 10 karya Sudono S.Pd., rumus pengenceran larutan adalah: Keterangan: ADVERTISEMENT. Jika sudah menemukan perhitungan yang tepat, Anda hanya perlu menuangkan jumlah pelarut yang dibutuhkan ke dalam zat yang akan dilarutkan atau diencerkan. Agar lebih mudah memahaminya, perhatikan.

PENGENCERAN LARUTAN RUMUS & LATIHAN SOAL MK Kimia Dasar YouTube
Penyelesaian: V1 x M1 = V2 x M2. 10 x 5 = V2 x 0,2. V2 = (10 x 5) : 0,2. V2 = 250ml. Berdasarkan penyelesaian di atas, untuk memperoleh larutan H2SO4 0,2M, sebanyak 10ml H2SO4 5M harus ditambahkan air sampai volumenya menjadi 250ml. Demikian penjelasan mengenai rumus pengenceran larutan beserta penjelasan konsep, contoh dan penyelesaian soalnya.

CARA KERJA DAN MENGHITUNG pH LARUTAN PENYANGGA SETELAH PENAMBAHAN ASAM, BASA, ATAU AIR
Pengenceran juga bisa diartikan sebagai penurunan suhu pH suatu bahan kimia yang dapat berupa gas, uap, atau larutan, melansir situs Byjus . 2. Rumus pengenceran. Nah, setelah tahu pengertian pengenceran kini kita bisa beralih mempelajari rumus pengenceran. Namun, sebelum itu, ada hal yang harus dicatat baik-baik.
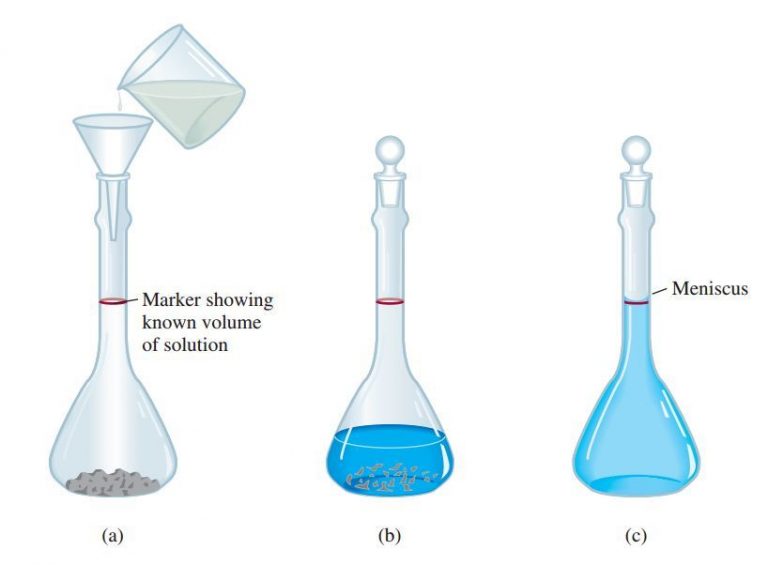
Pengertian, Rumus dan Contoh Soal Molaritas, Pembuatan Larutan dan Pengenceran Lengkap
Tulislah rumus untuk menghitung pengenceran. Kapan pun Anda siap untuk mengencerkan sebuah larutan, Anda dapat menggunakan rumus C 1 V 1 = C 2 V 2. Hal ini berarti konsentrasi larutan awal x volume awal = konsentrasi larutan pengenceran x volume pengenceran. Kita mengetahuinya karena konsentrasi x volume = jumlah asam, dan jumlah asam akan.

Contoh Soal Rumus Pengenceran Contoh Soal Dan Pembahasan Larutan Riset
1. Pengenceran sederhana. Pengenceran ini dilakukan dengan menambahkan pelarut ke larutan pekat hingga mencapai volume dan konsentrasi yang diinginkan. Rumus pengenceran sederhana adalah V1 x M1 = V2 x M2, di mana V1 dan M1 adalah volume dan konsentrasi larutan pekat, dan V2 dan M2 adalah volume dan konsentrasi larutan encer.
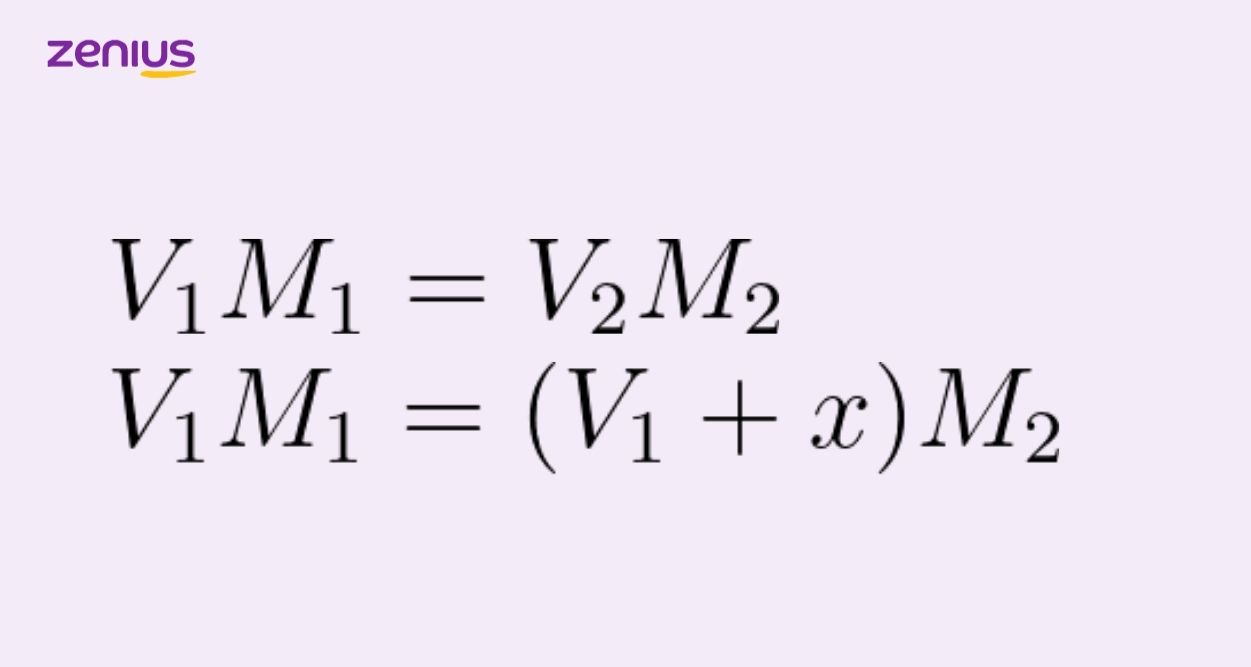
Rumus Pengenceran Larutan dan Contoh Soal Materi Kimia Kelas 11
Disini kita akan sedikit belajar mengenai cara mengencerkan larutan yang bisa dilakukan oleh semua orang baik di rumah sekalipun. Sebelum praktek akan diperlukan pengetahuan atau teori tentang pengenceran larutan. Dalam pengenceran larutan, rumus yang dipakai ialah V1.M1 = V2.M2. V1=Volume awal larutan. M1= Konsentrasi Awal Larutan
PEMBUATAN LARUTAN 1000 ML Na2S2O3 0,1 N DARI PADATAN Na2S2O3 5H2O
Ukur volum aquadest tersebut dan siapkan di dalam gelas kimia. Karena sifat zat cair pekat maka lakukan pengenceran larutan di ruang asam. Gunakan pelindung seperti jas lab, masker, sarung tangan, dan kacamata pelindung. Pada saat pencampuran/pelarutan segera alirkan perlahan cairan pekat lewat batang pengaduk ke dalam gelas kimia yang sudah.

XI.4.b. Rumus Pengenceran Larutan (Teori) YouTube
1. rumus persentase kadar zat & % massa volume Ar Mr #https://youtu.be/dvnk2b1YAPw2. rumus Ar Mr Nomor massa atom molekul relatif #https://youtu.be/FHrmZC5y.

Farmasetika Part 5. Pengenceran Larutan (Membuat Larutan dengan Rumus Pengenceran) YouTube
Normalitas =gram zat terlarutmassa ekuivalen x liter larutan. Rumus normalitas pengenceran. Jika kamu ingin menghitung normalitas pada proses pengenceran larutan, maka rumus normalitas yang digunakan adalah: N 1. V 1 = N 2. V 2. Keterangan: V 1 = volume larutan sebelum pengenceran.

Rumus Pengenceran Larutan Dan Contoh Soal Materi Kimia Kelas 11 52 Riset Riset
Faktor pengenceran adalah bilangan yang menunjukkan berapa kali suatu larutan pekat harus diencerkan untuk mendapatkan konsentrasi yang diinginkan. Rumus faktor pengenceran sangat sederhana, yaitu: Faktor Pengenceran = Volumen Larutan Peat / Volumen Larutan Hasil Pengenceran. Contoh: jika kita ingin membuat larutan 0,1 M NaCl sebanyak 100 mL.

Kumpulan Soal Konsentrasi Larutan
Rumus Pengenceran Larutan. Jadi gini, suatu larutan itu kan ada partikel zat terlarut dan pelarutnya. Ketika larutan tersebut ditambahkan air, maka volume larutan akan bertambah. Tapi, partikel-partikel di dalamnya tetap, dengan kata lain gak bertambah dan gak berkurang. Biar gak bingung, coba lo perhatikan ilustrasi berikut ini.
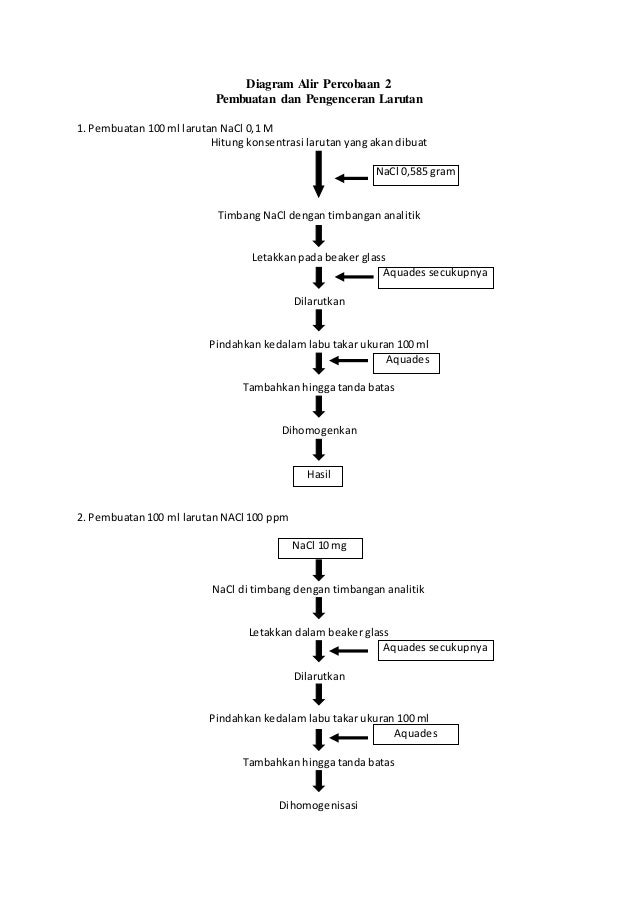
Diagram Alir Pembuatan dan Pengenceran Larutan
Pengenceran ini perlu dilakukan kalau elo cuma punya larutan dengan konsentrasi pekat sementara elo membutuhkan larutan berkonsentrasi encer. Sama kayak sirup yang kemanisan tadi. Elo harus mengencerkan sirupnya supaya rasa manisnya berkurang. Baca Juga: Larutan Asam: Materi Kimia Kelas 11.