Penjelasan Mengenai Kalorimetri ( Termokimia Part IV ) Panduan Kimia + Riset
1. Asas Black. Menurut hukum kekekalan energi, bahwa energi tidak dapat diciptakan atau dimusnahkan, yang terjadi hanyalah perubahan bentuk energi yang satu ke bentuk energi yang lain. Kita ambil contoh, sebuah benda A massa m1, suhu T1 dan kalor jenisnya c1. Kemudian kita masukkan ke dalam air B yang massanya m2, suhu T2, dan kalor jenis c2.

Kalorimeter Pengertian Jenis dan Contoh Soal
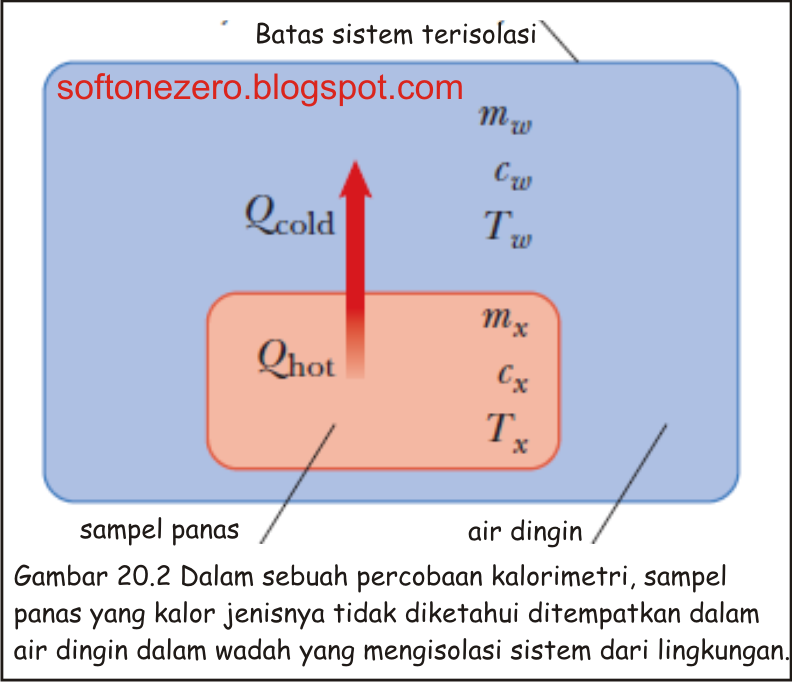
Kalorimetri merupakan suatu sistem terisolasi sehingga tidak memungkinkan terjadinya pertukaran energi dan materi antara sistem dengan lingkungan.. Proses pengukuran kalor reaksi dengan kalorimeter dinamakan kalorimetri. Rumus yang berlaku untuk menentukan besar (jumlah) kalor dalam kalorimetri, yaitu: q larutan = m×c×ΔT ; q kalorimeter.

PENENTUAN ENTALPI REAKSI DENGAN KALORIMETER YouTube
Kalorimetri. Selain memiliki energi kinetik dan energi potensial, setiap materi juga memiliki energi berupa panas/kalor. Hal ini dapat dibuktikan dengan adanya suhu yang dimiliki oleh setiap materi. Suhu yang dimiliki oleh setiap materi mengindikasikan jumlah kalor yang dimiliki oleh materi tersebut. Jika suatu materi memiliki suhu yang tinggi.

KALORIMETER Menghitung Perubahan Entalpi dengan Kalorimetri Kimia kelas XI YouTube
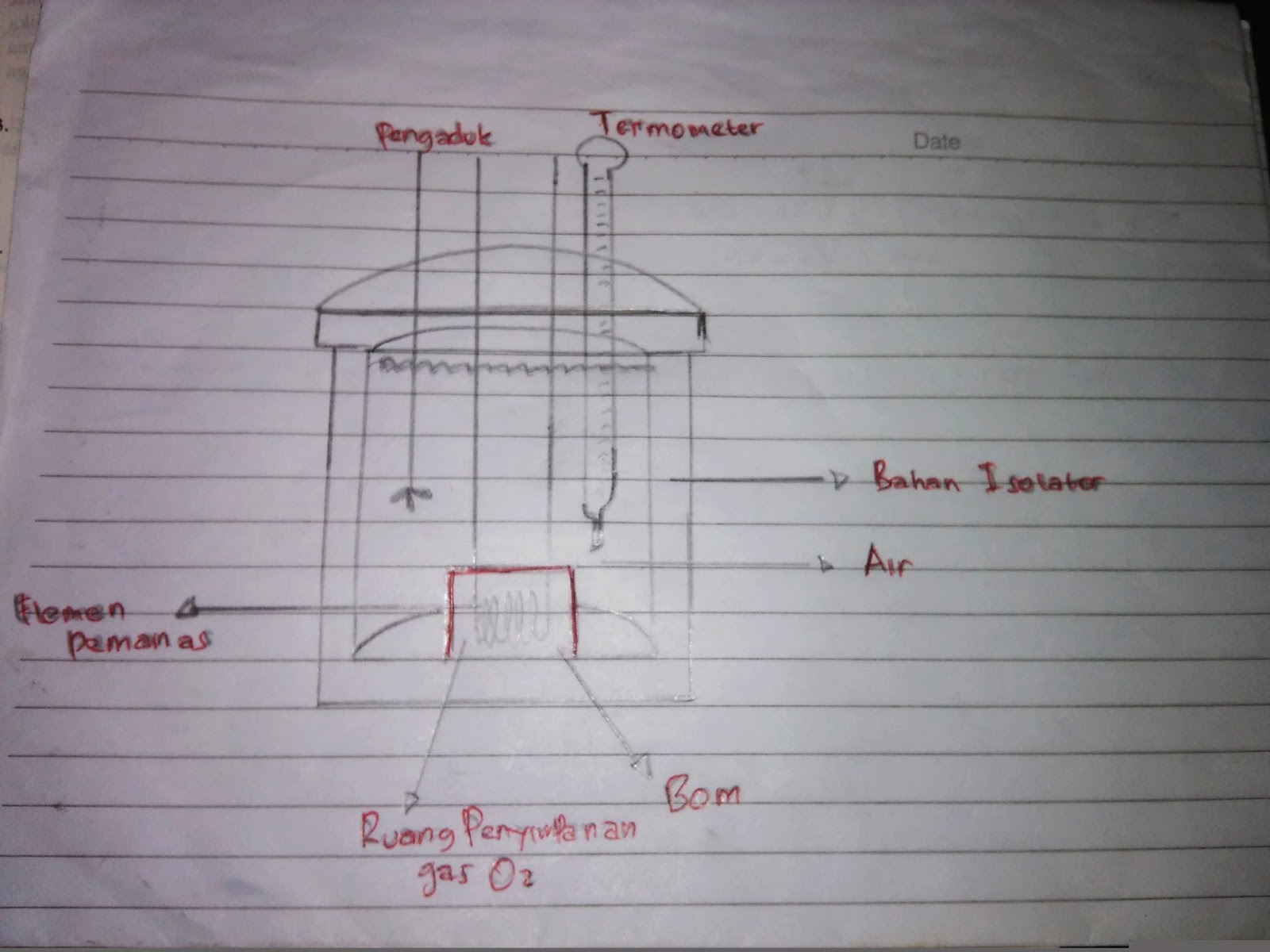
Menemukan dan memahami rumus kalorimeter bom yang penting untuk mengukur enerji dalam proses pembakaran secara akurat dan efisien. Pelajari konsep, komponen, dan langkah-langkah yang terlibat dalam perhitungan kalorimeter bom, serta signifikasinya dalam berbagai bidang seperti industri, penelitian, dan ilmu pengetahuan. Dengan memperoleh pemahaman yang baik tentang rumus ini, Anda akan dapat.

KALORIMETRI KIMIA KELAS XI Lely`s Channel Pembelajaran Ilmu Kimia SMA YouTube
Rumus yang digunakan untuk menghitung jumlah kalor bila kalor dari kalorimeter diabaikan adalah sebagai berikut. q larutan = m × c × ΔT. Dengan keterangan: q = perubahan kalor reaksi (J) m = massa zat (g) c = kalor jenis zat (J/g C) ΔT = perubahan suhu ( o C) Namun, bila kalor dari kalorimeter diperhitungkan, rumusnya menjadi: q kalorimeter.

Rumus Kebutuhan Kalori Cara Menentukan Jumlah Kalori yang Dibutuhkan Tubuh Contoh Soal dan
Dalam rumus m = massa air, q = kalor air spesifik dan Δt = variasi suhu. Mengetahui semua ini, jumlah kalor yang dilepaskan oleh reaksi eksoterm kemudian dapat dihitung.. Gambar menunjukkan bagian-bagian pompa kalorimetri; Namun, dapat dilihat bahwa ia memiliki termometer dan pengaduk, elemen umum dalam beberapa kalorimeter.

PPT TERMOKIMIA PowerPoint Presentation ID5603224
Joseph Black, adalah seorang kimiawan Skotlandia yang mendukung teori tentang panas, yaitu bahwa suhu merupakan konsentrasi kalori dalam suatu benda. Ia kemudian menemukan ilmu baru yang disebut kalorimetri. Ketika menyelidiki tentang panas (kalori), ia mengira bahwa kapasitas panas merupakan jumlah panas yang dapat ditampung oleh suatu benda.

KELAS 11 LIHAT INI MENGHITUNG KALOR REAKSI SECARA KALORIMETRI KIMIA INDUSTRI
Inilah praktek yang dilakukan di industri, dimana rumus kimia bahan bakar tsb tidak penting, yang penting hanya kalornya saja. Misalnya batu bara atau minyak bumi yang dipakai untuk boiler.. Kalorimetri *Kalorimetri adalah metode untuk mengukur efek atau perubahan panas dari suatu reaksi, yang bisa meliputi perubahan fisik maupun perubahan.

MENGHITUNG PERUBAHAN ENTALPI MENGGUNAKAN KALORIMETRI YouTube
Rumus Kalorimeter. Kalorimetri merupakan merupakan sistem yang dimana tidak ada perpindahan materi dan energi dengan lingkungan di luar kalorimeter tersebut. Kalorimeter ini ada dua jenis, yaitu kalorimeter bom dan sederhana. Kalorimeter bom adalah alat yang digunakan untuk mengukur jumlah kalor yang dilepaskan saat pembakaran sempurna.

Kalorimeter Rumus Brain
Adapun fungsi dari kalorimeter antara lain: Mengetahui kalor suatu perubahan dalam reaksi kimia. Mengukur jumlah kalor pada perubahan reaksi kimia. Menghitung jumlah kalor suatu perubahan reaksi kimia. Mendeteksi suh pada suatu kalor. Alat peneliti percobaan pada kalor. Pada dasarnya fungsi utama dari kalorimeter yakni mengukur kalor yang.

Dalam suatu kalorimeter direaksikan 100 cm3 larutan NaOH 1 M dengan 100 cm3 larutan HCI 1 M
Rumus kalorimetri tersebut adalah: Q = m x c x ΔT. Q = jumlah kalori. m = massa makanan dalam gram. c = kalor jenis makanan. ΔT = selisih suhu awal dan akhir makanan. Contoh Penggunaan Rumus Kalorimetri. Sebagai contoh, misalnya kita ingin menghitung jumlah kalori dalam satu porsi nasi. Kita tahu bahwa: m = 100 gram. c = 1 kalori/gram/derajat.
TERMODINAMIKA Kalor Jenis dan kalorimetri
Dalam kalorimetri, penerapan kalorimeter sangat banyak. Kalorimeter dapat digunakan untuk melakukan studi biologi, melakukan pengendalian kualitas atau bahkan memeriksa laju biologis. Bagian dari kalorimeter. Mengingat pengertian kalorimeter, maka bagian-bagian kalorimeter pada umumnya akan dijelaskan di bawah ini:

Kalorimeter
Persamaan Rumus Termokimia.. Kalorimetri. Kalorimetri merupakan cara penentuan kalor reaksi dengan kalorimeter, yaitu sistem terisolasi (tidak ada perpindahan materi dan energi dengan lingkungan). Jika dianggap keseluruhan kalorimeter adalah sistem, maka q sistem = 0.

KELAS 11 LIHAT INI MENGHITUNG KALOR REAKSI SECARA KALORIMETRI KIMIA INDUSTRI
Kalorimetri adalah ilmu dalam pengukuran panas dan reaksi kimia atau perubahan fisik. Pada kalorimetri ini dapat melakukan pengukuran perubahan kalor yang bergantung pada pemahaman tentang kalor jenis dan kapasitas kalor. Dengan demikian kita dapat mengetahui suhu pada suatu ruangan atau benda-benda lainnya. pengukuran panas ini sangat.

Contoh Soal Kalorimeter Beserta Jawabannya Terbaru
1. Penentuan dengan kalorimetri Kalorimetri yaitu cara penentuan energi kalor reaksi dengan kalorimeter. Kalorimeter yaitu suatu sistem terisolasi, sehingga semua energi yang dibutuhkan atau dibebaskan tetap berada dalam kalorimeter. Dengan mengukur perubahan suhu, kita bisa menentukan jumlah energi kalor reaksi berdasarkan rumus: Keterangan :

Contoh Soal Kalorimeter Dan Pembahasan
Latihan Soal Penentuan Entalpi Kalorimeter (Sedang) Pertanyaan ke 1 dari 5. Pada percobaaan kalorimetri, 32 gram metanol dibakar. 55% energi yang dilepas diserap oleh 1,2 L air sehingga terjadi kenaikan suhu dari 15 ∘ C menjadi 85 ∘ C. Kalor jenis air 4, 2 J − 1g − 1K − 1.