
Hukum Raoult untuk kesetimbangan uapcair (VLE) sistem biner YouTube
Adapun bunyi Hukum Raoult yang berkaitan dengan penurunan tekanan uap adalah sebagai berikut :. Rumus Perhitungan Tekanan Uap. Untuk menghitung penurunan tekanan uap larutan, ketahui dulu rumus perhitungannya yang dibuat oleh Marie Francois Raoult (1878) dari eksperimen yang pernah dilakukan, seperti:.

Raoult's Law YouTube
Hukum Raoult merupakan hukum yang dicetuskan oleh seorang ahli kimia-fisika berkebangsaan Perancis bernama François-Marie Raoult (1830-1901), dimana hukum ini mempelajari sifat-sifat serta hubungan antara tekanan uap larutan dan zat pelarut. Dikutip dari buku Prinsip-Prinsip Kimia Modern karya David W. Oxtoby (2001: 165 - 166), Hukum Raoult.

Apakah hukum raoult berlaku dalam semua larutan pada seluruh selang konsentrasi Desain Grafis
Hukum Raoult Raoult adalah seorang ahli kimia dari Perancis, ia mengamati bahwa pada larutan ideal yang dalam keadaan seimbang antara larutan dan uapnya, maka perbandingan antara tekanan uap salah satu komponennya ( misal A) P A /P A o sebanding dengan fraksi mol komponen (X A) yang menguap dalam larutan pada suhu yang sama.

Modified Raoult's Law Equation Raoult's law Wikipedia, the free encyclopedia TranquilDerm
Hukum Raoult tentang Campuran Ideal. Bunyi dari hukum Raoult adalah: "tekanan uap larutan ideal dipengaruhi oleh tekanan uap pelarut murni dan fraksi mol zat pelarut yang terkandung dalam larutan tersebut". Secara matematis, hukum Raoult untuk satu komponen dalam larutan ideal ditulis sebagai: =, dengan adalah tekanan uap parsial komponen pada campuran gas, adalah tekanan uap komponen.

Modified Raoult's Law Equation Raoult's law Wikipedia, the free encyclopedia TranquilDerm
Raoult's law is independent of the nature of the solute; the only parameter is the mole fraction of the solvent (or solute, if written as $\Delta p = \chi_\mathrm{solute} \cdot p^\circ$). Henry's law, on the other hand, depends on the nature of both solute and solvent (i.e. the Henry's constant is different for different solvents).

Hukum Raoult PDF
Hukum Raoult ini menyatakan kalau tekanan uap larutan dipengaruhi oleh tekanan uap pelarut murni dan fraksi mol zat pelarut. Dari Hukum Raoult pun didapatkan persamaan: Rumus tekanan uap larutan (Arsip Zenius) Surprisingly, ada berbagai contoh penurunan tekanan uap dalam kehidupan sehari-hari. Kalo elo pernah masak air gula dan bingung kenapa.

Bunyi Hukum Raoult, Rumus, Contoh Soal, Tekanan Uap Jenuh Larutan, Kimia
Hukum Raoult Hukum Raoult adalah hukum yang dicetuskan untuk mempelajari sifat-sifat tekanan uap larutan yang mengandung zat pelarut yang bersifat nonvolatil, serta membahas mengenai aktivitas air. Francois M. Raoult, pencetus Hukum Raoult Hukum Raoult tentang Campuran Ideal Bunyi dari hukum Raoult adalah: "tekanan uap larutan ideal dipengaruhi oleh tekanan uap pelarut dan fraksi mol zat.
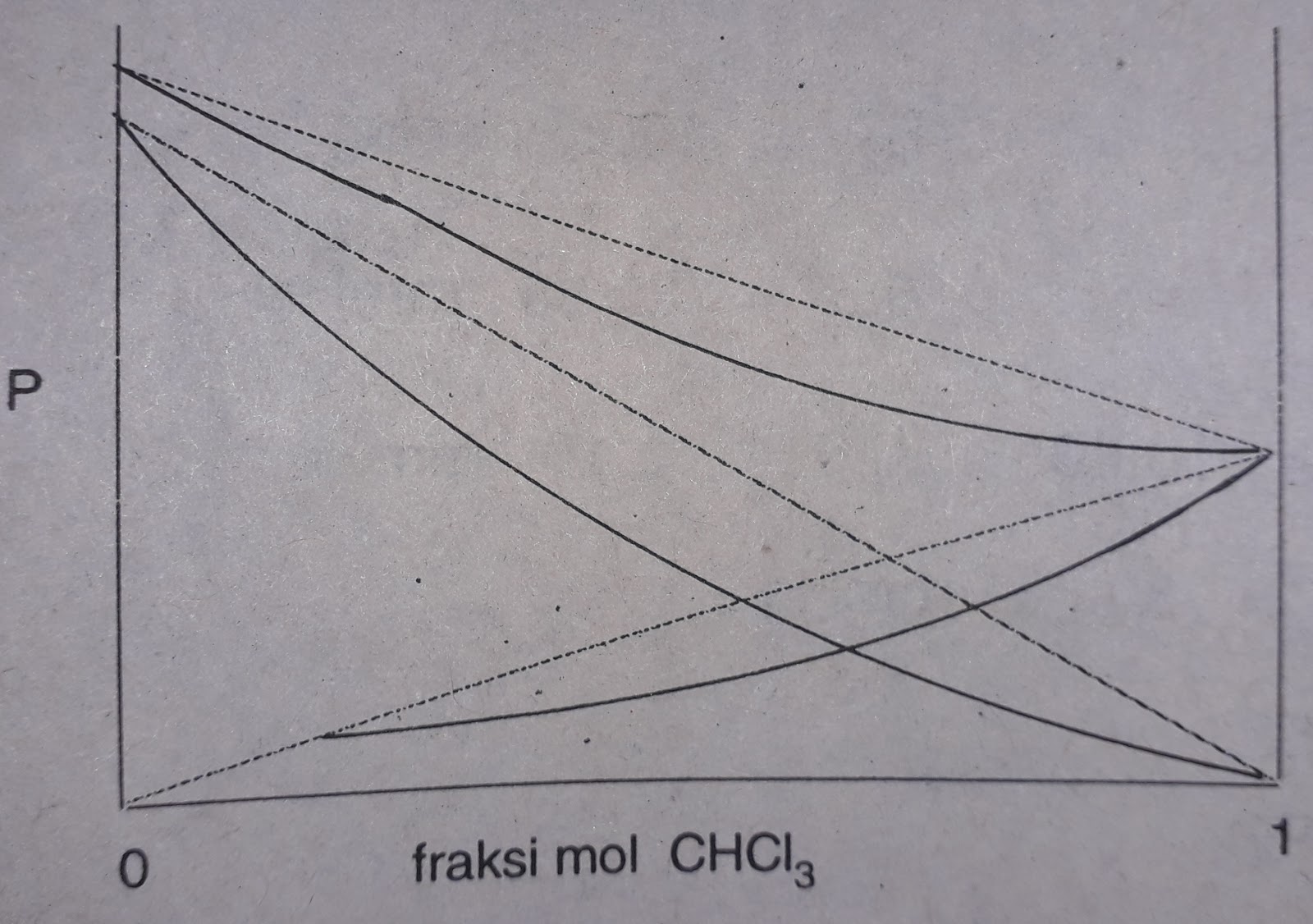
Hukum Raoult dan Sifat Larutan Nonelektrolit Sains Pedia
Dapatkan Modul, Rumus, & Soal Kapasitas Kalor dan Sistem Fasa lengkap di Wardaya College.. (Hukum Raoult) Hukum ini akan dipenuhi bila komponen-komponen dalam larutan mempunyai sifat yang mirip atau interaksi antar larutan besarnya sama dengan interaksi di dalam larutan. Campuran ideal memiliki sifat-sifat $\Delta H_{mix}=0,\Delta V=0,$ dan

Vapor Liquid Equilibrium (VLE) Part 2 Dew Point and Fitting VLE Data (Hukum Raoult's) YouTube
Hukum Raoult dapat digunakan untuk menyatakan hubungan tekanan uap larutan yang mengandung pelarut volatil dan nonvolatil. Hukum Raoult dinyatakan dengan. P larutan = pelarut P 0 pelarut dimana. P larutan adalah tekanan uap larutan. pelarut adalah fraksi mol pelarut P. 0 pelarut adalah tekanan uap pelarut murni.

HUKUM RAOULT PDF
Hukum Raoult berfungsi untuk mempelajari sifat-sifat tekanan uap larutan yang mengandung zat pelarut yang bersifat nonvolatil, serta membahas mengenai aktivitas air. Rumus penurunan tekanan uap terbagi menjadi dua, yakni untuk non-elektrolit dan elektrolit.

PPT DISTILASI /PENYULINGAN PowerPoint Presentation, free download ID4048941
Hukum Raoult adalah hukum kimia yang menyatakan bahwa tekanan uap larutan bergantung pada fraksi mol zat terlarut yang ditambahkan ke larutan. Hukum Raoult dinyatakan dengan rumus: P larutan = pelarut P 0 pelarut. dimana. P larutan adalah tekanan uap larutan pelarut. adalah fraksi mol pelarut P 0 pelarut adalah tekanan uap pelarut murni Jika.

Modified Raoult's Law Equation Raoult's law Wikipedia, the free encyclopedia TranquilDerm
ΔP = P ∘ − P. Tekanan uap larutan ideal dapat dihitung berdasar hukum Raoult yang berbunyi: "Tiap komponen dalam suatu larutan melakukan tekanan yang sama dengan fraksi mol kali tekanan uap dari komponen (pelarut) murni". P = Xt ⋅ P ∘ dan P = Xp ⋅ P ∘.
Modified Raoult's Law Equation Raoult's law Wikipedia, the free encyclopedia TranquilDerm
Hukum Raoult Tentang Larutan dan Gas Sebelum mempelajari tentang Hukum Raoult dan apa yang memberi tahu kita tentang larutan, kita perlu memperkenalkan dan meninjau beberapa istilah kembali. Hukum Raoult adalah semua tentang hubungan antara larutani dan bagaimana hal itu mempengaruhi gas pada larutan. Jadi, kita perlu merujuk kembali ke tekanan parsial gas dan meninjau apa

Raoult's Law How To Calculate The Vapor Pressure of a Solution YouTube
Hukum Raoult dinyatakan dengan persamaan tekanan uap: P larutan = pelarut P 0 pelarut dimana P larutan adalah tekanan uap larutan pelarut adalah fraksi mol pelarut P 0 pelarut adalah tekanan uap pelarut murni Ketika dua atau lebih banyak larutan yang mudah menguap dicampur, setiap komponen tekanan dari larutan campuran ditambahkan bersama untuk menemukan tekanan uap total.

Hukum Raoult (Kimia SBMPTN, UN, SMA) YouTube
Hukum Raoult adalah hukum yang dicetuskan oleh Francois M. van Raoult untuk mempelajari sifat-sifat tekanan uap larutan yang mengandung zat pelarut yang bersifat nonvolatil, serta membahas mengenai aktivitas air.. Rumus penurunan tekanan uap jenuh dengan memakai faktor Van't Hoff adalah sebagai berikut. = P 0. 2. Kenaikan Titik Didih.

PPT DISTILASI /PENYULINGAN PowerPoint Presentation, free download ID4048941
P = PA + PB (1) Hukum Dalton dan Raoult merupakan pernyataan matematis yang dapat menggambarkan apa yang terjadi selama distilasi, yaitu menggambarkan perubahan komposisi dan tekanan pada cairan yang mendidih selama proses distilasi. Uap yang dihasilkan selama mendidih akan memiliki komposisi yang berbeda dari komposisi cairan itu sendiri.