
Perubahan Wujud Zat Yang Disertai Pelepasan Kalor Adalah Lengkap
Artikel ini membahas tentang macam-macam perubahan wujud zat yakni perubahan fisika, kimia, menyerap kalor dan melepaskan kalor lengkap dengan penjelasan, contoh dan percobaannya. Blog IPA SMP Pages. Home. Contoh perubahan wujud yang memerlukan kalor antara lain sebagai berikut.

PPT KALOR DAN PERPINDAHAN KALOR PowerPoint Presentation, free download ID3967348
Dalam fisika, menyublim adalah proses perubahan wujud zat dari padat menjadi gas yang disebabkan oleh sejumlah kalor yang diserap oleh zat padat tersebut. Dalam kehidupan sehari-hari, peristiwa menyublim bisa kita lihat contohnya pada habisnya sebutir kapur barus (kamper) setelah beberapa saat disimpan di tempat terbuka.
Suhu dan Kalor Kalor
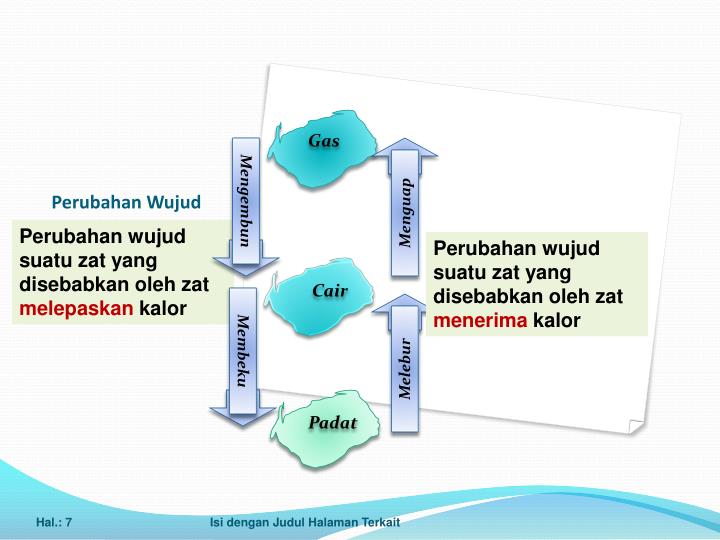
Apabila suatu zat menerima atau melepaskan kalor, maka wujudnya dapat berubah menjadi wujud lain. Misalnya, es yang menerima kalor dari lingkungan akan berubah menjadi cair dan air yang menerima kalor dari hasil pemanasan akan berubah menjadi uap atau gas. Ketika suatu zat berubah menjadi wujud lain, diperlukan atau dilepaskan sejumlah kalor.
PPT Kalor PowerPoint Presentation ID4474635
Ada konduksi, konveksi, dan radiasi. Yuk, kita bahas satu per satu! 1. Konduksi. Perpindahan kalor secara konduksi adalah proses perpindahan kalor yang terjadi pada suatu zat tanpa disertai perpindahan partikel-partikel dari zat tersebut. Konduksi umumnya terjadi pada zat padat terutama yang bersifat konduktor.
Kelompok perubahan wujud yangmembebaskan kalor ada...
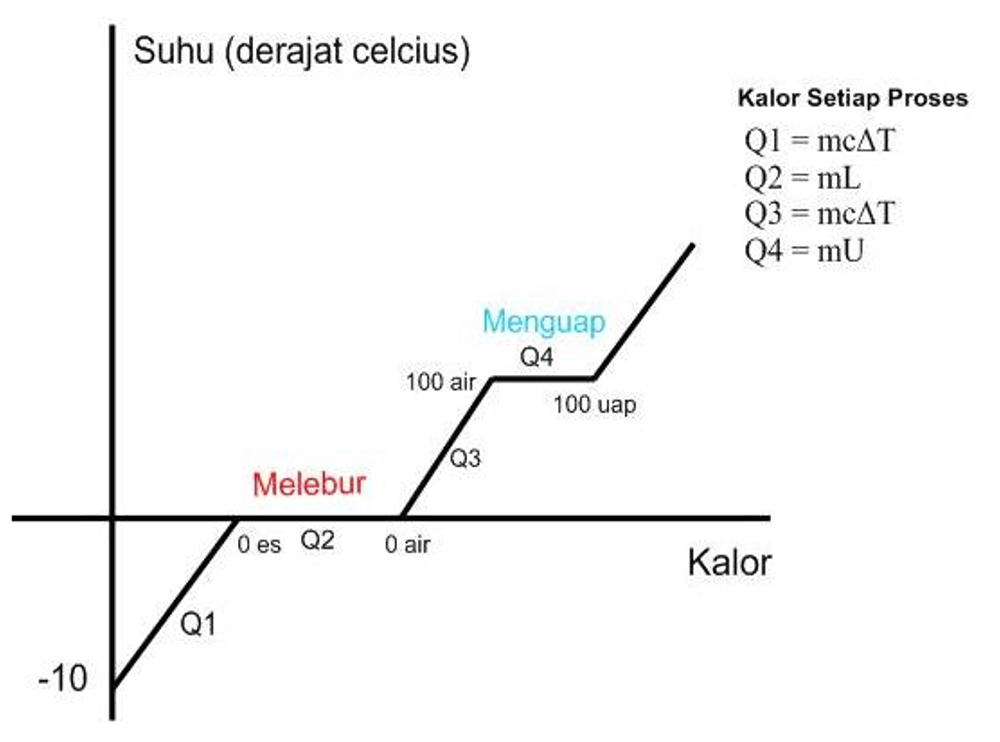
Qterima: adalah jumlah dari kalor yang diterima oleh zat. Baca juga: Perpindahan Kalor: Rumus, Jenis, Macam, dan Contohnya. Grafik perubahan wujud zat. Grafik perubahan wujud zat menunjukkan wujud zat pada suhu tertentu. Berikut rumus untuk menghitung kalor (Q1, Q2, Q3 dan Q4), yaitu: Q1 adalah kalor untuk menaikkan suhu es dari < 0°C menjadi 0°C
Contoh Perubahan Wujud Zat
Selamat datang di artikel kami yang membahas tentang contoh perubahan wujud yang menyerap kalor. Dalam artikel ini, RintikSedu akan membahas dan menjelaskan beberapa contoh perubahan wujud yang memiliki sifat menyerap kalor. Sebagai ahli dalam bidang ini, saya akan memberikan informasi yang berguna bagi pembaca..

BAB 5 Kalor pada Perubahan Wujud Benda IPA Kelas 7 YouTube
Kalor pada Perubahan Wujud Benda. Terjadinya perubahan wujud benda dapat diamati dalam kehidupan sehari-hari. Salah satu contoh yang sering dijumpai adalah pada air mendidih yang berbuih dan berubah jadi asap saat dipanaskan.. Namun, setiap benda dapat memancarkan dan menyerap radiasi kalor, yang besarnya bergantung pada suhu benda dan warna.

Perubahan Wujud Zat Yang Menyerap Kalor Adalah Gambaran
2. Kalor Bisa Mengubah Wujud Zat. Pada beberapa jenis zat benda jika diberikan kalor dalam satuan tertentu, maka zat benda tersebut akan mengalami perubahan. Misalnya es yang dipanaskan atau diberi kalor maka akan terjadi perubahan wujud dari yang semula padat menjadi cair atau bentuk gas.

Blog Belajar IPA SMP Kalor pada Perubahan Wujud Benda
Kalau yang ini rumusnya beda, guys. Coba perhatikan gambar berikut. Untuk menghitung kapasitas kalor atau yang dilambangkan dengan huruf C kapital, kita bisa menggunakan dua rumus di atas. Nanti, kamu lihat aja di contoh soal, kira-kira rumus mana yang bisa kamu gunakan berdasarkan nilai-nilai apa saja yang diketahui dari soal.
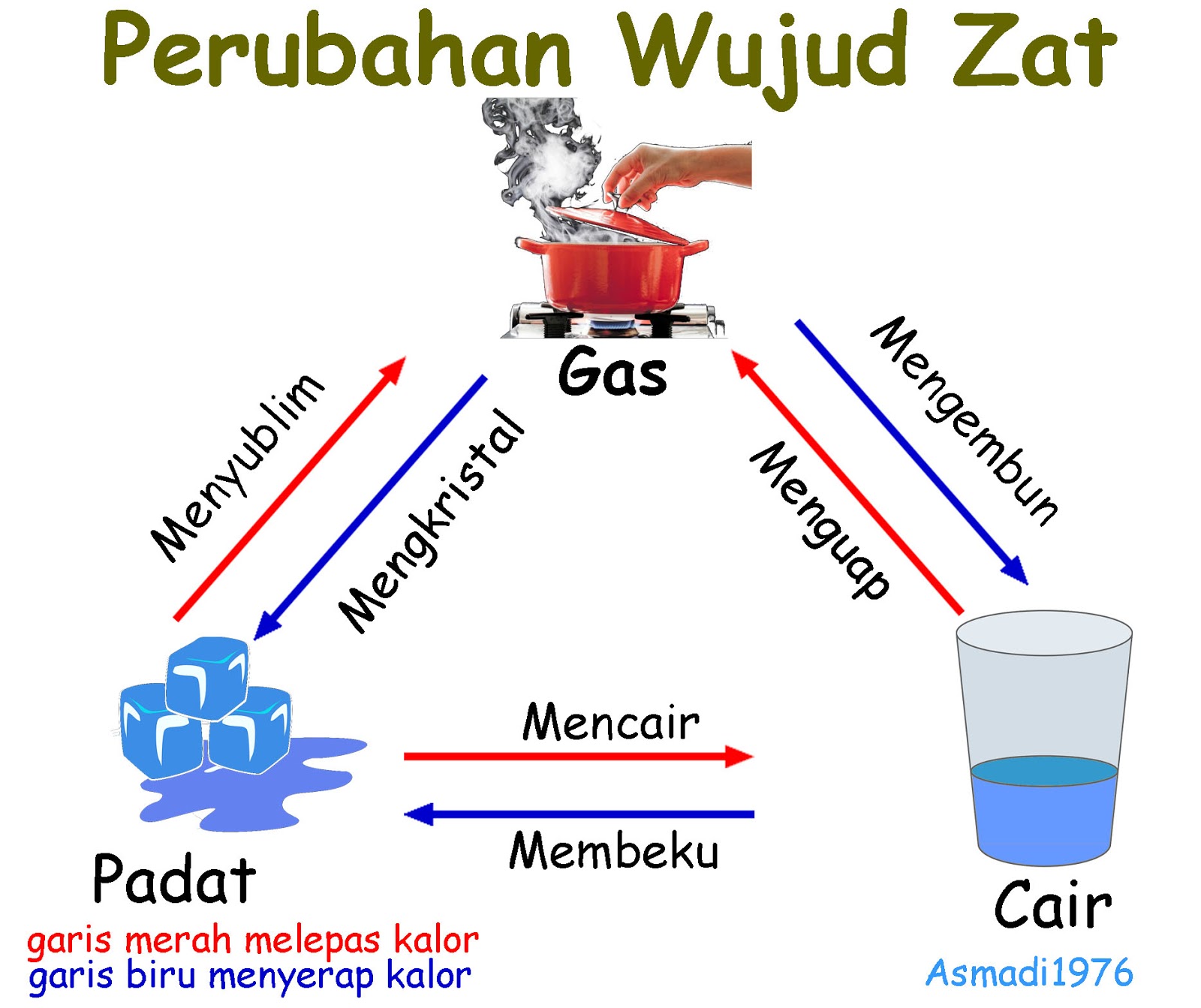
Jika Sebongkah Es Menyerap Kalor Dari Lingkungan Maka Blog Yuri
Untuk menentukan besarnya kalor jenis tiap zat, Quipperian bisa menggunakan persamaan berikut. Keterangan: Q = energi kalor (J); c = kalor jenis (J/kg oC); m = massa (kg); dan. ∆T = perubahan suhu (oC). Untuk kalor jenis beberapa zat yang sudah diketahui, bisa Quipperian lihat di tabel berikut ini.

Perubahan Wujud Zat Yang Menyerap Kalor
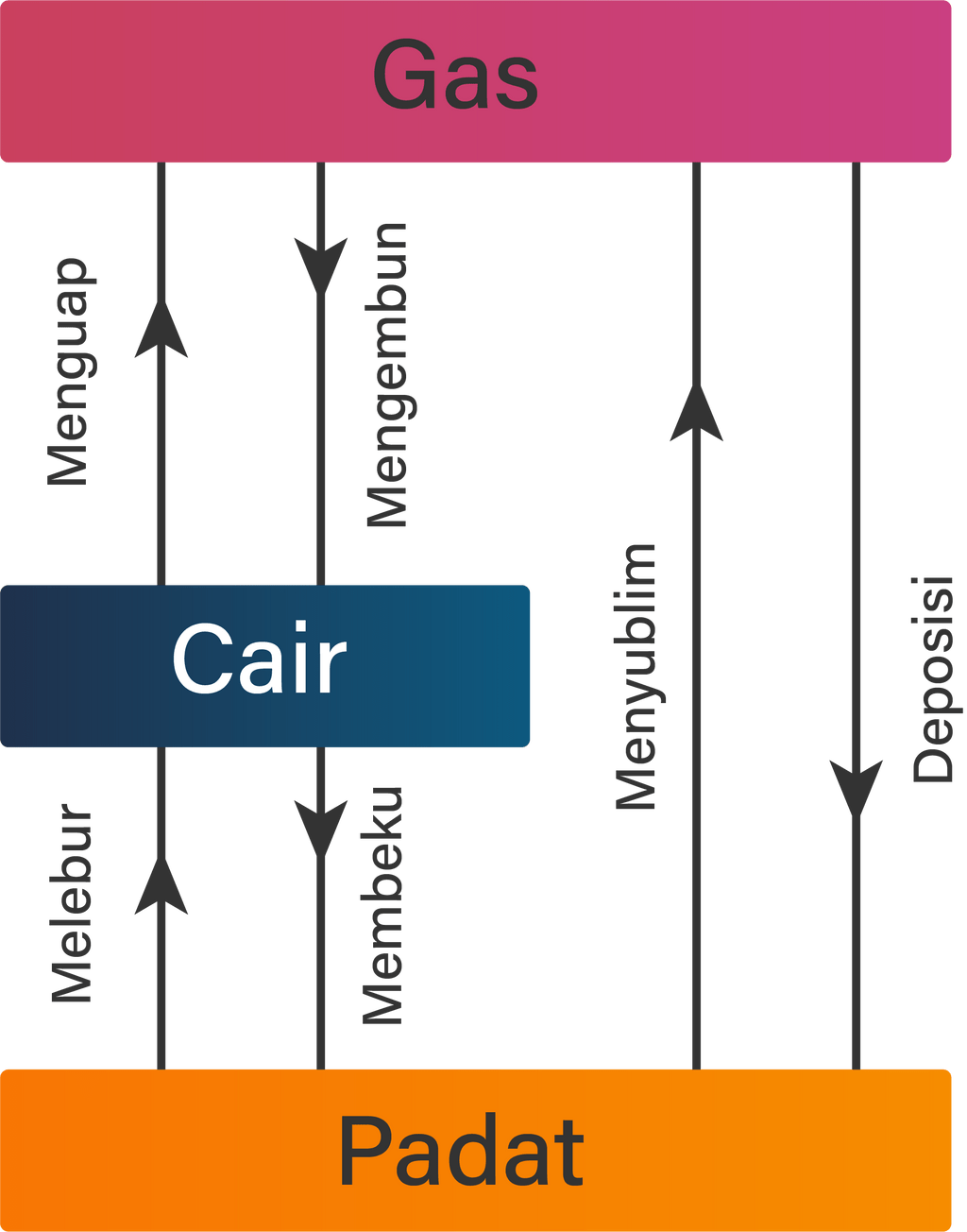
Peristiwa perpindahan kalor dalam kehidupan sehari-hari Kalor dapat berpindah dari satu benda ke benda lainnya, hingga dapat mengubah wujud benda, demikian laman rumahbelajar.id menulis. Terdapat enam macam perubahan wujud zat yang disebabkan perpindahan kalor yaitu: Menguap: dari cair ke gas (prosesnya adalah menyerap kalor)

Perubahan benda yang memerlukan kalor adalah
Perubahan wujud zat ini bisa terjadi karena peristiwa pelepasan dan penyerapan kalor.Perubahan wujud zat terjadi ketika titik tertentu tercapai oleh atom/senyawa zat tersebut yang biasanya dikuantitaskan dalam angka suhu. Semisal air untuk menjadi padat harus mencapai titik bekunya dan air menjadi gas harus mencapai titik didihnya.

pelajaran IPA kelas 4 SD perubahan wujud zat
Selain rumus, kamu juga perlu memahami tentang jenis-jenis kalor yang dikategorikan berdasarkan proses bekerjanya pada zat tertentu. Berikut adalah beberapa jenis kalor, di antaranya yaitu: ∆Hf (kalor pembentukan) → Dibutuhkan untuk membuat 1 mol senyawa dalam unsurnya. Contohnya seperti C 12, O 2, Br 2, dan H 2.
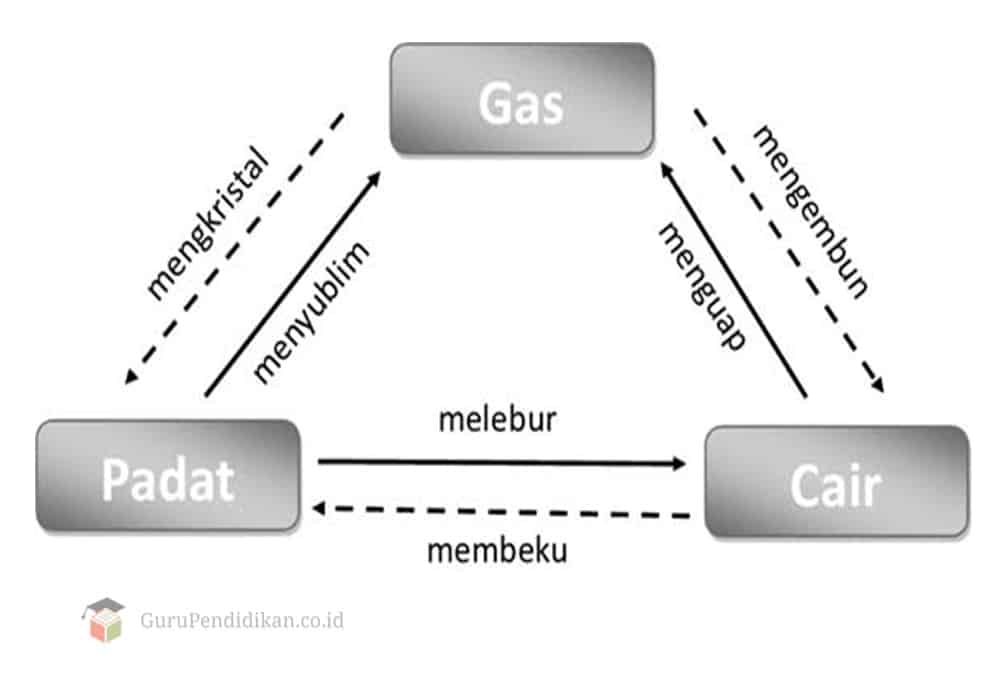
•Perubahan Wujud Zat Oleh Kalor Epicologi Epicologi
Dalam pembelajaran tentang energi kalor, rumus tersebut berguna untuk menghitung jumlah kalor yang diserap atau dilepaskan ketika suatu benda mengalami perubahan suhu. Dikutip dari Modul Pembelajaran SMA Fisika Kelas XI (2020), berikut rumus energi kalor yang dapat dinyatakan melalui rumus perpindahan kalor. Q=m⋅c⋅ΔT.

Perhitungan Perunahan Kalor (GRAFIK PERUBAHAN WUJUD ZAT) YouTube
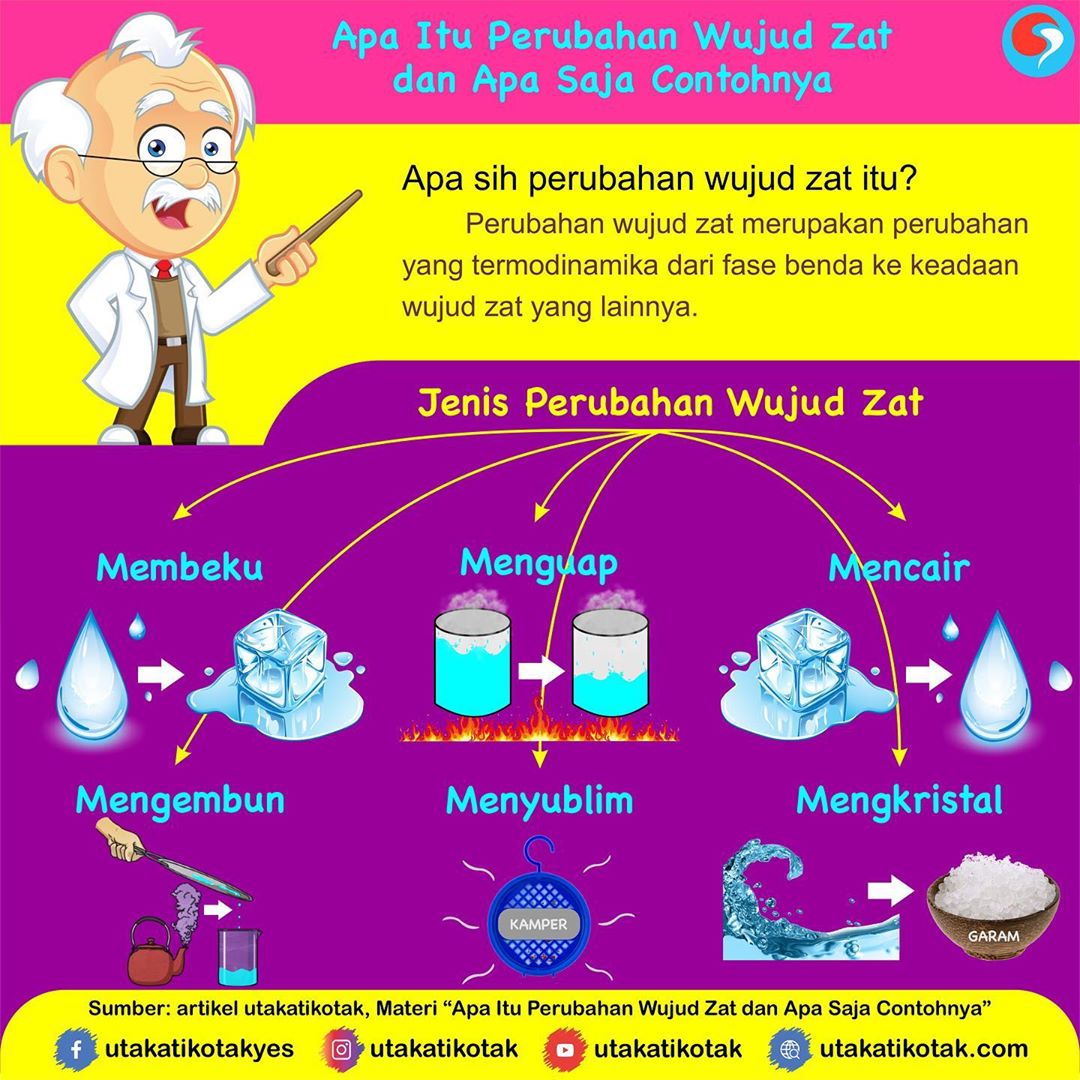
Pembahasan Di antara proses-proses perubahan wujud zat, terdapat tiga proses yang menyerap kalor atau memerlukan kalor. Ketiga proses tersebut adalah: menyublim: perubahan wujud dari padat menjadi gas (huruf S) mencair/melebur: perubahan wujud dari padat menjadi cair (huruf P) menguap: perubahan wujud dari cair menjadi gas (huruf T) Dengan demikian, proses-proses yang menyerap kalor.
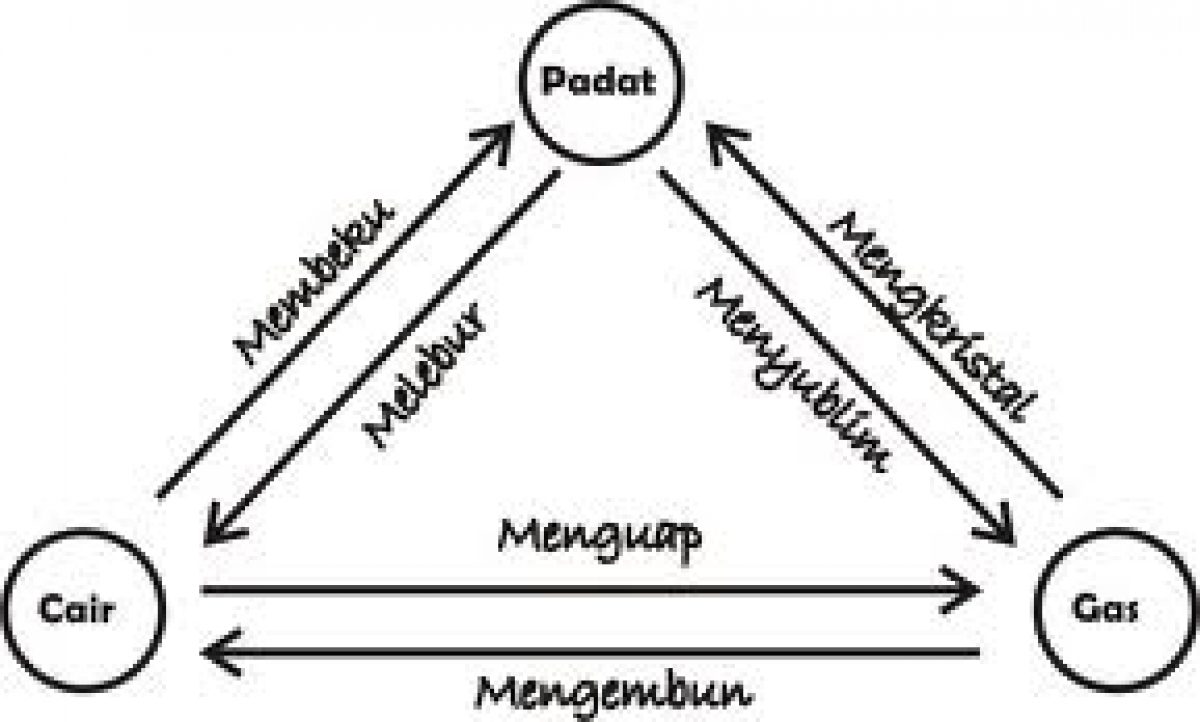
Perubahan Wujud Zat Yang Memerlukan Kalor
Pada peristiwa perubahan wujud ini, es bersuhu 0 o C berubah menjadi air bersuhu 0 o C. Jadi, tidak ada perubahan suhu pada saat es mencair, tetapi dibutuhkan kalor untuk mengubah wujud es tersebut. Pada dasarnya, kalor adalah perpindahan energi kinetik dari satu benda yang bersuhu lebih tinggi ke benda yang bersuhu lebih rendah.