
3 Ways to Calculate Atomic Mass wikiHow Chemistry Class 12, Chemistry Classroom, Teaching
Tetapi, yang menentukan massa atom hanyalah proton dan netron. Dilansir dari Encyclopedia Britannica, hal tersebut dikarenakan proton dan neutron memiliki massa sekitar 1.836 kali lebih besar daripada massa elektron. Sehingga, massa elektron dapat dianggap tidak ada karena terlalu kecil. Baca juga: Massa Atom Relatif dan Massa Molekul Relatif.

Contoh Soal Nomor Atom Dan Nomor Massa Homecare24
Neutron udah diketahui, yaitu 28. Sedangkan, nomor atom besi (Fe) berdasarkan sistem periodik adalah 26. Nomor massa menunjukkan jumlah neutron dan proton, sehingga 28 + 26 = 54. Jadi, nomor massa atom besi yang mempunyai 28 neutron adalah 54. Baca Juga: Materi Kimia: Rumus Massa Atom Relatif dan Aplikasinya.

Lengkapi tabel berikut. Nomor massa Nomor atom Jumlah Pro...
Massa Atom Hanya Dihitung dari Massa Proton dan Neutron Karena.. Massa atom hanya dihitung dari massa proton dan neutron karena massa elektron yang sangat kecil dan tersebar di sekitar nukleus tidak memberikan kontribusi yang signifikan pada massa atom secara keseluruhan. 2. Apakah massa elektron tidak penting dalam menghitung massa atom?
.jpg)
Rumus Massa Atom Relatif (Ar) dan Cara Menghitungnya 2023
Massa atom hanya dihitung dari massa proton dan neutron karena massa elektron terlalu kecil. Jika dibandingkan massa elektron lebih kecil 1/1.836 dari massa proton dan lebih kecil 1/1.839 dari massa neutron.. Konfigurasi di atas menggunakan nomor atom karena melambangkan jumlah elektron dalam atom. Konfigurasi elektronnya berakhir di sub.

Proton, Elektron, Neutron, Nomor Atom, dan Nomor Massa pada Komposisi Atom YouTube
Walaupun demikian, elektron memiliki massa yang sangat kecil (9.109 × 10 ^ -28 gram) sehingga kontribusi massanya hampir diabaikan dalam menghitung massa atom. Inti atom terdiri dari proton dan neutron, yang memiliki massa yang relatif lebih besar (1,67 × 10 ^ -24 gram untuk proton; 1,68 × 10 ^ -24 gram untuk neutron).

Nomor Atom, Nomor Massa, dan Konfigurasi Elektron YouTube
Kumpulan Soal Pilihan Ganda + Pembahasan Materi Struktur Atom Dan Sistem Periodik Unsur (Part 2)11. Teori atom Thomson yang menyatakan bahwa atom merupakan b.
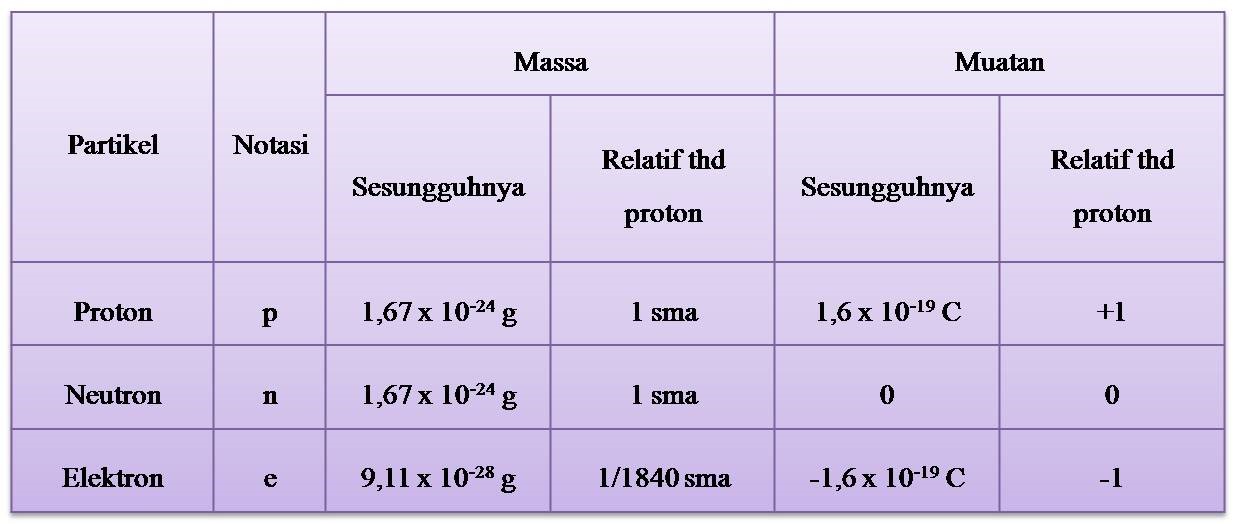
Partikel Dasar Atom
Jumlah proton dan neutron ternyata dapat menentukan massa dari atom. Hal ini terjadi karena massa proton dan neutron sangat besar, jika dibandingkan dengan elektron. Sehingga elektron dianggap tidak bermassa. Makin banyak jumlah proton dan neutron menandakan bahwa makin besar massa dari suatu atom. Jadi, jawaban yang tepat adalah opsi C.
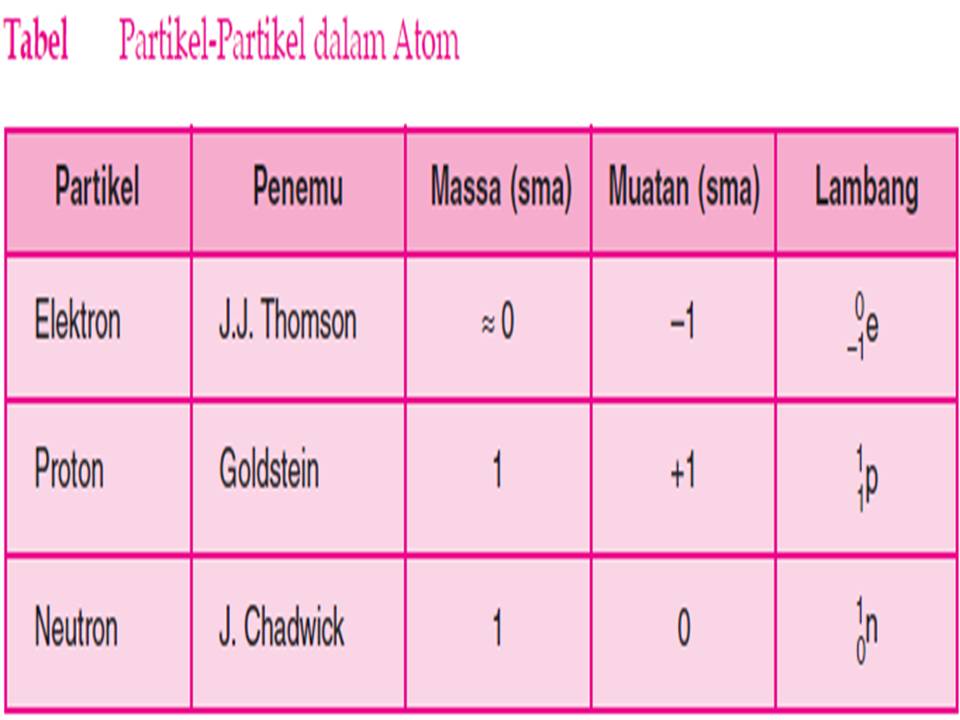
Massa dan Muatan Proton Elektron Neutron Sinau Online
Massa atom adalah seberapa berat satu atom dalam satuan massa atom. Massa atom sendiri hanya dihitung dari jumlah massa proton dan neutron di dalam inti atom. Baca artikel ini untuk mengetahui lebih jelas mengenai massa atom.

Massa inti atom 4 2 He=4,0026 sma, massa proton =1,0078 s...
Di alam, suatu unsur bisa memiliki lebih dari satu isotop sehingga massa atom relatif berfungsi sebagai nilai rata-rata dari setiap massa isotop. Untuk menghitung massa atom relatif dari unsur yang memiliki lebih dari satu isotop adalah sebagai berikut. Ar X = (% kelimpahan X1 . Ar X1) + (% kelimpahan X2. Ar X2) + dst100 %.

Cara Menghitung Proton Elektron Dan Neutron Ujian
Massa atom suatu isotop yang langka dapat berbeda dari bobot atom standar sebesar beberapa satuan massa. Atom litium -7 memiliki 3 proton, 4 neutron, dan 3 elektron. Atom ini bermassa 7,016 u. Litium-6 yang langka dan bermassa 6,015 u hanya memiliki 3 neutron, membuat bobot atom (massa atom relatif) litium menjadi 6,941 u.
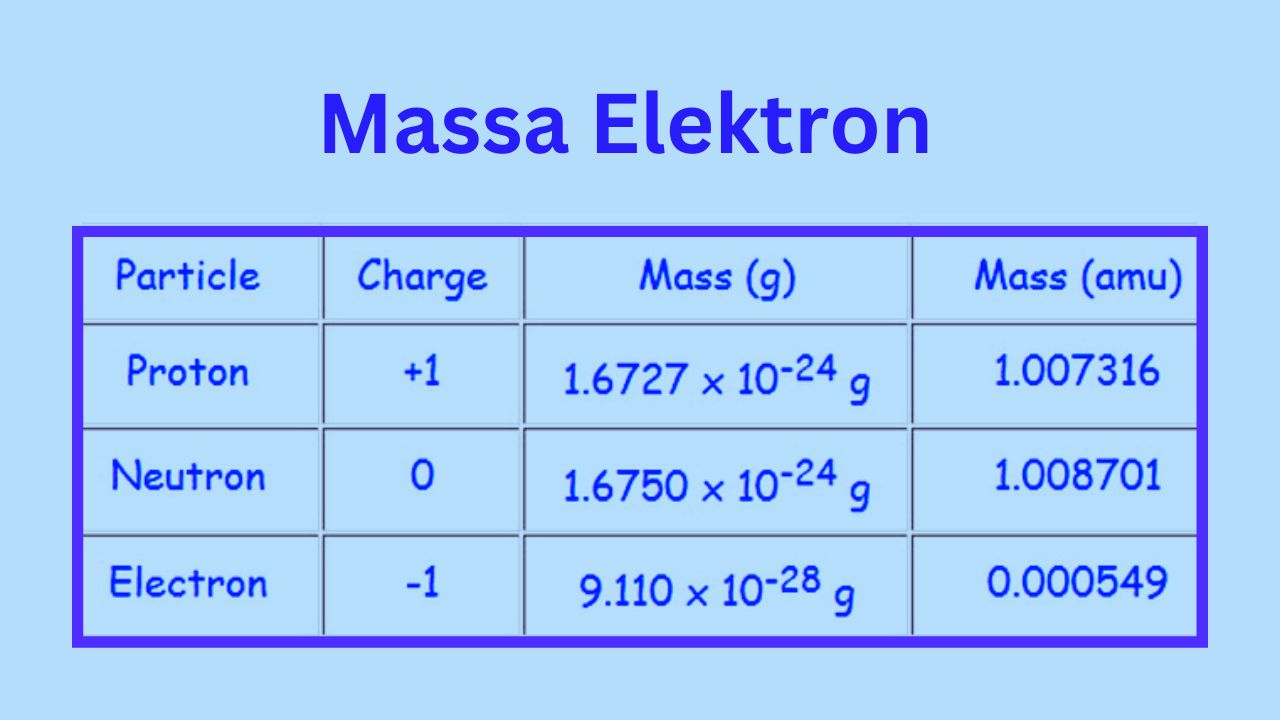
Elektron Pengertian, Penemu, Massa, Konfigurasi, Contoh Thecityfoundry
Untuk menghitung massa atom suatu atom tunggal suatu unsur, jumlahkan massa proton dan neutron. Contoh: Temukan massa atom dari isotop karbon yang memiliki 7 neutron . Anda dapat melihat dari tabel periodik bahwa karbon memiliki nomor atom 6, yang merupakan jumlah protonnya. Massa atom atom adalah massa proton ditambah massa neutron, 6 + 7.

Nomor Atom dan Nomor Massa Kimia CoLearn
Karena dalam soal sudah memakai s.m.a, Jadi kalian tinggal masukin aja deh massa atom C-12 dengan satuan s.m.a. Nah, akhirnya dapet deh jawabannya sebesar 35 s.m.a, tapi biasanya dalam soal kalian akan disuguhkan dalam satuan metrik seperti kilogram atau gram, sehingga kalian harus menghitungnya dengan teliti dan cermat!

CARA MENENTUKAN JUMLAH PROTON, ELEKTRON, NEUTRON UNSUR Na KIMIA KELAS X SMA YouTube
Massa atom adalah jumlah semua proton, neutron, dan elektron dalam satu atom atau molekul tunggal. Massa sebuah elektron sangatlah kecil sehingga dapat diabaikan dan tidak dimasukkan ke dalam perhitungan. Meskipun secara teknis salah, istilah massa atom juga sering kali digunakan untuk merujuk pada massa atom rata-rata dari semua isotop suatu unsur.

Partikel Bermuatan Positif Yang Terdapat Dalam Inti Atom Adalah kabarmedia.github.io
Karena atom C-12 ini digunakan sebagai standar, maka satu satuan massa atom didefinisikan sebagai suatu massa yang besarnya tepat sama dengan seperdua belas massa satu atom C-12. Nah, seperti sudah dibahas di infografik tadi, massa 1 atom hidrogen adalah 1,67 x 10 -27 kg , alias 1/12 dari massa atom C-12.

Relative Atomic Mass, Here's an explanation, formula, and how to calculate it World Today News
Semakin ke kanan, kamu juga akan melihat bahwa nomor massa setiap atom bertambah besar. Artinya, kamu dapat memahami berat unsur walaupun hanya dengan melihat letaknya pada tabel. Semakin ke kanan atau ke bawah, massa atom unsur akan bertambah karena massa atom dihitung dengan menjumlahkan proton dan neutron di setiap atom unsur.
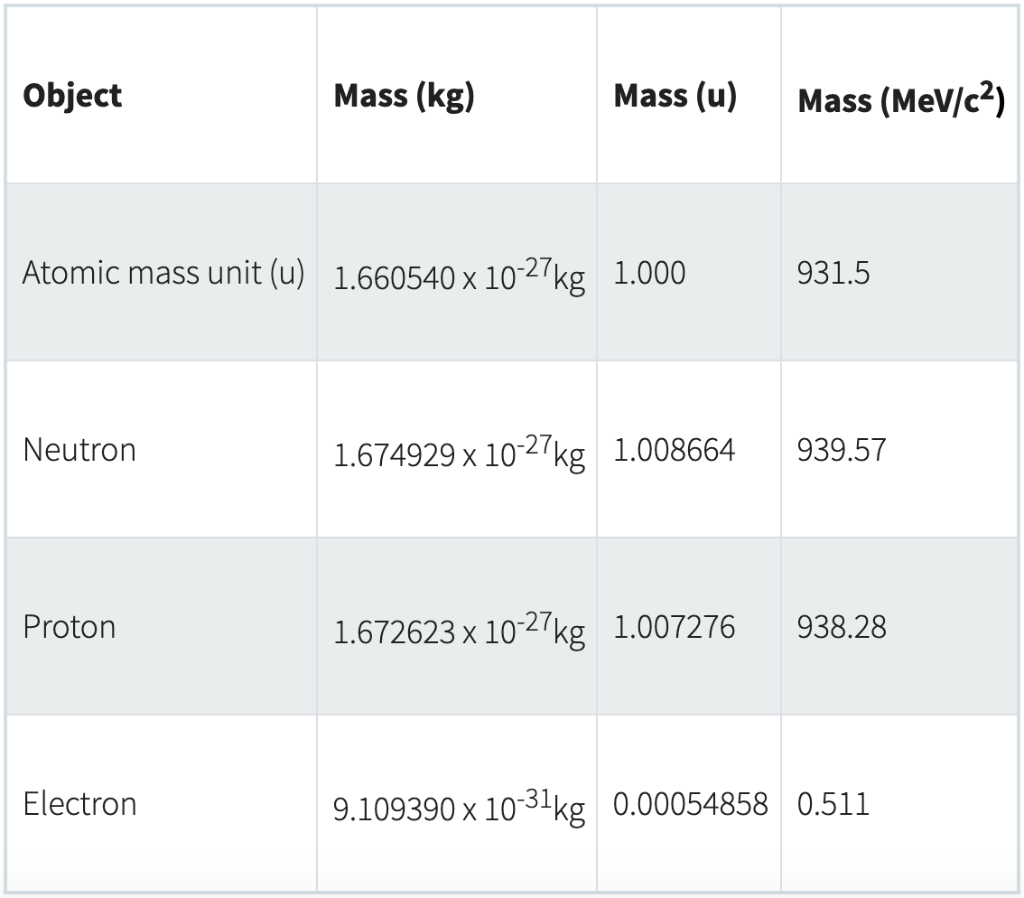
38+ how to calculate the mass of a proton RakeshTosia
Nomor atom (Z) = jumlah proton (p) = jumlah elektron (e) 2. Nomor massa. Jumlah proton dan jumlah neutron dalam suatu atom disebut dengan nomor massa. Nomor massa sebuah atom hanya dapat ditentukan oleh banyaknya massa proton dan neutron. Massa elektron sangat kecil (kurang dari 1 atm), sehingga massa elektron dabaikan.