
Suatu Larutan Dapat Menghantarkan Arus Listrik Apabila Mengandung YPHA.OR.ID
Baca juga: Perbedaan Elektrolit Kuat dan Lemah. Contoh larutan yang dapat menghantarkan arus listrik adalah: Larutan garam atau natrium klorida (NaCl) Larutan natrium hidroksida (NaOH) Larutan hidrogen bromida (HBr) Larutan asam sulfat (H2SO4) Larutan hidrogen klorida (HCl)

30 Contoh Larutan Elektrolit dan Non Elektrolit
suatu larutan elektrolit dapat menghantarkan arus listrik karena.. mengandung unsur logam. larutan tersebut larutan homogen. 1 pt. berikut yang merupakan larutan elektrolit adalah.. H 2 O. HCl. HNO 3. Urea. gula. 7. Multiple Choice. 30 seconds. 1 pt. Larutan asam sulfat dapat menghantarkan arus listrik karena.. Merupakan larutan elektrolit.

Larutan Asam Sulfat Dapat Menghantarkan Arus Listrik Karena Neofotografi
Larutan asam dan basa adalah larutan elektrolit karena kedua larutan tersebut dapat menghantarkan arus listrik. Selain itu, larutan asam dan basa juga memiliki sifat asam basa yang lain yaitu sebagai berikut. D. Sifat Asam. Sifat asam diantaranya yaitu: Memiliki rasa masam; Korosif; Dalam air terurai menjadi hidrogen (H +) dan sisa asam (ion.

Pasangan Larutan Berikut Yang Dapat Menghantarkan Arus Listrik Adalah YPHA.OR.ID
Karena terdapat beberapa larutan yang dapat menghantarkan arus listrik adalah NaOH (soda api), H2SO4 (asam sulfat), HCl (asam klorida), dan KCl, yang semuanya juga termasuk elektrolit kuat. Larutan Elektrolit Lemah yaitu elektrolit yang tidak terurai sempurna menjadi ion atau mengalami ionisasi sebagian sehingga jumlah zat yang terurai menjadi.

Larutan Asam Sulfat Dapat Menghantarkan Arus Listrik Karena Neofotografi
Ia ditemukan terlarut dalam air laut (yaitu 0,04% kalium berdasarkan berat [5] [6] ), dan merupakan bagian dari banyak mineral . Kalium secara kimiawi sangat mirip dengan natrium, unsur sebelumnya pada golongan 1 tabel periodik. Mereka memiliki energi ionisasi pertama yang sama, yang memungkinkan setiap atom melepaskan satu-satunya elektron.

MENGUJI LARUTAN MANA KAH YANG BISA MENGHANTARKAN LISTRIK YouTube
Raksa ( bahasa Inggris : mercury) adalah sebuah unsur kimia dengan lambang Hg dan nomor atom 80. Ia juga dikenal sebagai air raksa dan dulunya bernama hydrargyrum ( haɪˈdrɑːrdʒərəmHY-drar-JƏR-əm) dari kata Yunani hydro (air) dan argyros (perak). [5] Merupakan sebuah unsur blok-d yang berat dan keperakan, raksa adalah satu-satunya unsur.

Pada elektrolisis larutan tembaga(II) sulfat dengan arus
Menurut Arrhenius, asam sulfat mempunyai sifat asam karena dapat melepaskan ion H+ dalam air. Sehingga nantinya konsentrasi H+ dalam air akan bertambah. Reaksi ionisasinya dapat dilihat sebagai berikut:. Larutan yang bersifat asam adalah larutan yang bisa menghantarkan arus listrik atau disebut sebagai larutan elektrolit. Kekuatannya.

Larutan H_(2) SO_(4) dapat menghantarkan listrik karena...
Larutan elektrolit adalah larutan yang dapat menghantarkan arus listrik. Contoh larutan elektrolit adalah larutan asam sulfat, natrium hidroksida, garam dapur, asam cuka dan lainnya. Larutan elektrolit dapat menghantarkan arus listrik karena zat elektrolit dalam larutannya terurai menjadi ion-ion bermuatan listrik dan ion-ion tersebut selalu.
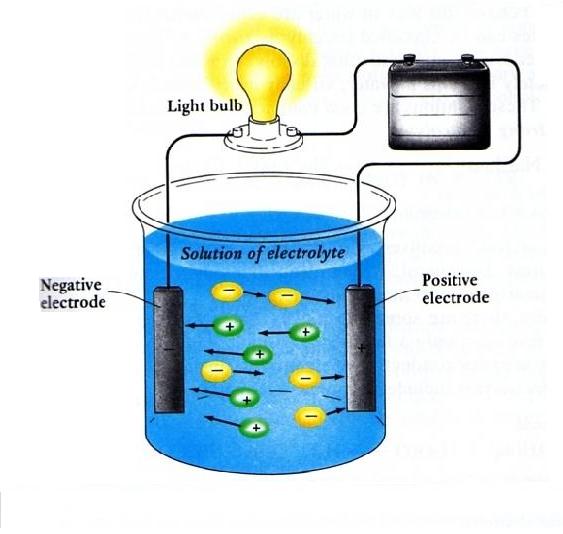
Life Is Beautiful Mengapa Larutan Elektrolit Dapat Menghantarkan Arus Listrik???
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Larutan asam sulfat dapa.

Senyawa berikut yang dapat menghantarkan arus listrik ada...
Kelebihan Larutan Asam Sulfat Dapat Menghantarkan Arus Listrik Karena. 1. Digunakan dalam industri kimia; 2. Penggunaan dalam bidang pertanian; 3. Digunakan dalam bidang farmasi; 4. Berguna dalam industri besi dan baja; 5. Mampu membersihkan noda pada pakaian

Larutan Elektrolit Dapat Menghantarkan Arus Listrik Karena Terdapat cara mengatasi kaki pegal
Larutan asam sulfat dianggap sebagai larutan elektrolit kuat karena mengalami disosiasi ionik sepenuhnya dalam air. Molekul asam sulfat ( H 2 S O 4 H₂SO₄ ) terionisasi menjadi dua ion hidrogen (H⁺) dan satu ion sulfat ( S O 4 2 − SO₄²⁻ ), sehingga dapat menghantarkan arus listrik

Contoh Asam Sulfat Dalam Kehidupan Sehari Hari Berbagai Contoh Riset
Dengan demikian, larutan elektrolit dapat menjadi media yang penting dalam menghantarkan arus listrik. 1. Larutan elektrolit adalah bahan yang dapat melepaskan ion ke dalam larutan. 2. Ion-ion yang bebas bergerak di dalam larutan dapat mengikat dan melepaskan muatan listrik, sehingga dapat menghantarkan arus listrik. 3.

Larutan Yang Dapat Menghantarkan Arus Listrik Disebut PDF
Semakin banyak jumlah ion, semakin kuat daya hantarnya. Sedangkan larutan yang tidak dapat menghantarkan arus listrik disebabkan karena zat-zat tersebut tetap berwujud molekul-molekul netral yang tidak bermuatan. Berdasarkan daya hantarnya larutan elektrolit terbagi menjadi dua, yaitu elektrolit kuat dengan daya hantar yang besar. Contohnya.

Asam sulfat dapat dibuat dengan bahan dasar belerang, uda...
Contoh elektrolit kuat adalah asam sulfat (air aki) dan natrium klorida (garam dapur). Larutan elektrolit lemah, merupakan elektrolit yang punya kekuatan daya hantar listrik lemah, hal ini disebabkan karena hanya sebagian kecil molekulnya saja yang terurai menjadi ion-ion. Nilai α pada larutan ini berada diantara 0 dan 1 (0 < α < 1).
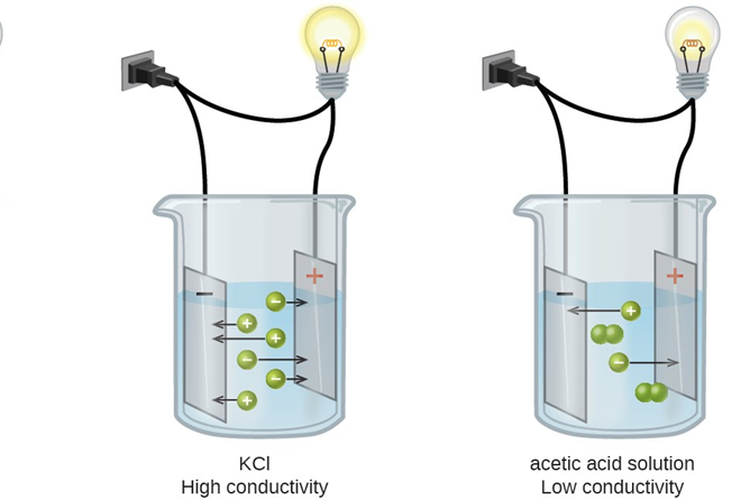
Contoh Larutan yang Dapat Menghantarkan Arus Listrik
Beberapa zat kimia yang dapat menghantarkan arus listrik melalui larutan antara lain garam, asam klorida, asam borat dan asam sulfat. Garam, misalnya natrium klorida, adalah kombinasi asam klorida dan natrium hidroksida, dengan masing-masing menyumbang satu ion, yaitu ion klorida dan ion natrium.

Reaksi Pembuatan Asam Sulfat Melalui Proses Kontak Anak Sekolah
Logam berat umumnya didefinisikan sebagai logam dengan densitas, berat atom, atau nomor atom tinggi. Kriteria yang digunakan, dan jika metaloid disertakan, bervariasi tergantung pada penulis dan konteksnya. Dalam metalurgi, misalnya, logam berat dapat didefinisikan berdasarkan kerapatan, sedangkan pada fisika, kriteria pembeda adalah nomor atom, sementara kimiawan kemungkinan akan lebih.