
Untuk menentukan molaritas larutan H2 SO4 dilakukan den...
Molaritas larutan urea bisa dihitung dengan cara : Jumlah mol urea, n = gram/Mr = 3/60 = 0,05 mol Molaritas larutan, M = n/V = 0,05/0,25 = 0,2 molar Maka molaritas larutan urea yaitu 0,2 molar atau 0,2 mol/liter. Contoh perhitungan molalitas larutan. Misalnya 10 gram natrium hidroksida (NaOH) dilarutkan dalam 2 kg air. Massa molekul relatif.

Molaritas Larutan dan cara membuat larutan dengan molaritas tertentu YouTube
Mol juga digunakan untuk menyatakan jumlah atom, ion, atau entitas elementer lainnya dalam sampel zat tertentu. Konsentrasi larutan umumnya dinyatakan sebagai molaritas, yang didefinisikan sebagai jumlah mol zat terlarut per liter larutan. Jumlah molekul per mol dikenal sebagai bilangan Avogadro, dan didefinisikan sebagai massa satu mol zat.
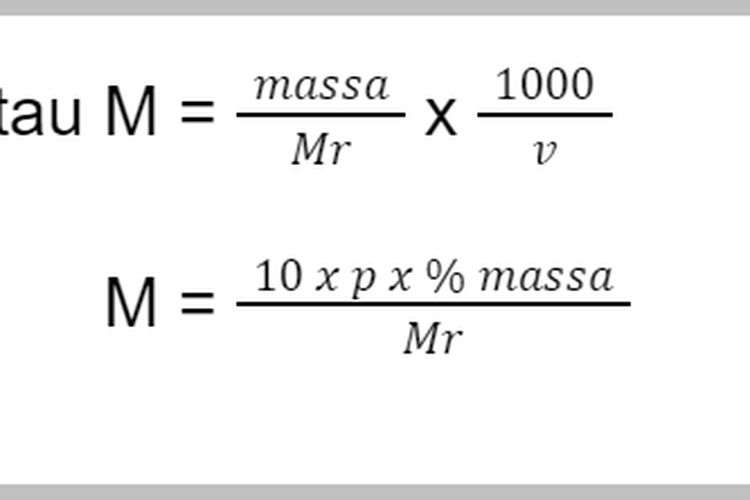
Pahami Rumus Molaritas, Contoh Soal, dan Pembahasannya Berikut Ini
Rumus normalitas kimia adalah N = n x a /V, yang menyatakan nilai normal (N) yang sama dengan satu mol ekivalen/liter. Dalam kimia, terdapat beberapa besaran yang dapat digunakan untuk menyatakan suatu konsentrasi zat terlarut dalam sebuah larutan antara lain yaitu molaritas, molalitas, normalitas dan fraksi mol.

firstwisnu media Konsentrasi Larutan
Dalam perhitungan molaritas, kuantitas larutan didasarkan pada volume.. Larutan yang dibuat dari 1 mol NaCl yang dilarutkan dalam 1.000 g air dinyatakan sebagai larutan 1 molal dan diberi lambang 1 m NaCl. Molalitas didefinisikan dengan persamaan berikut. Rumus atau Persamaan Perhitungan Molalitas. Keterangan: m = molalitas (mol/kg)
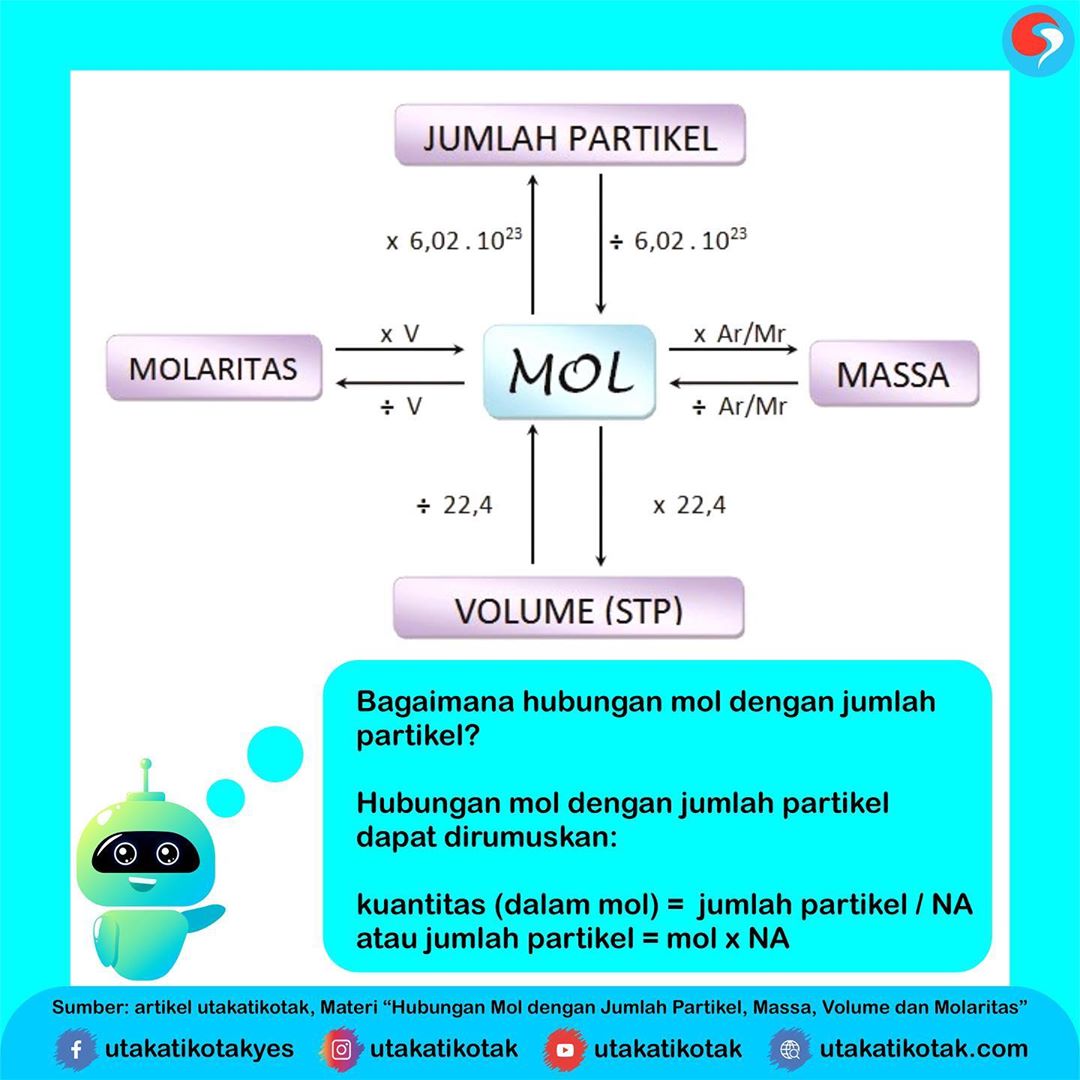
Hubungan Mol dengan Jumlah Partikel, Massa, Volume dan Molaritas
Molalitas, disebut pula sebagai konsentrasi molal, adalah ukuran konsentrasi dari suatu zat terlarut di dalam suatu larutan dalam hal jumlah zat dalam sejumlah massa tertentu dari pelarut.Hal ini berbeda dengan definisi molaritas yang berdasarkan pada volume tertentu larutan.. Satuan yang umum digunakan untuk molalitas dalam kimia adalah mol/kg.Suatu larutan dengan konsentrasi 1 mol/kg juga.

Perbedaan Molaritas Dan Molalitas Riset
What determines the concentration of a solution? Learn about the relationships between moles, liters, and molarity by adjusting the amount of solute and solution volume. Change solutes to compare different chemical compounds in water.

Menghitung Molaritas Bab Sifat Koligatif Larutan YouTube
Pengertian molaritas. Molaritas adalah ukuran yang mengemukakan konsentrasi suatu larutan. Dilansir dari Chemistry LibreText, molaritas adalah jumlah mol zat terlarut dalam satu liter larutan. Molaritas disimbolkan sebagai M dan memiliki satuan mol per liter (mol/L) atau molar, sehingga molaritas juga kerap disebut sebagai konsentrasi molar.
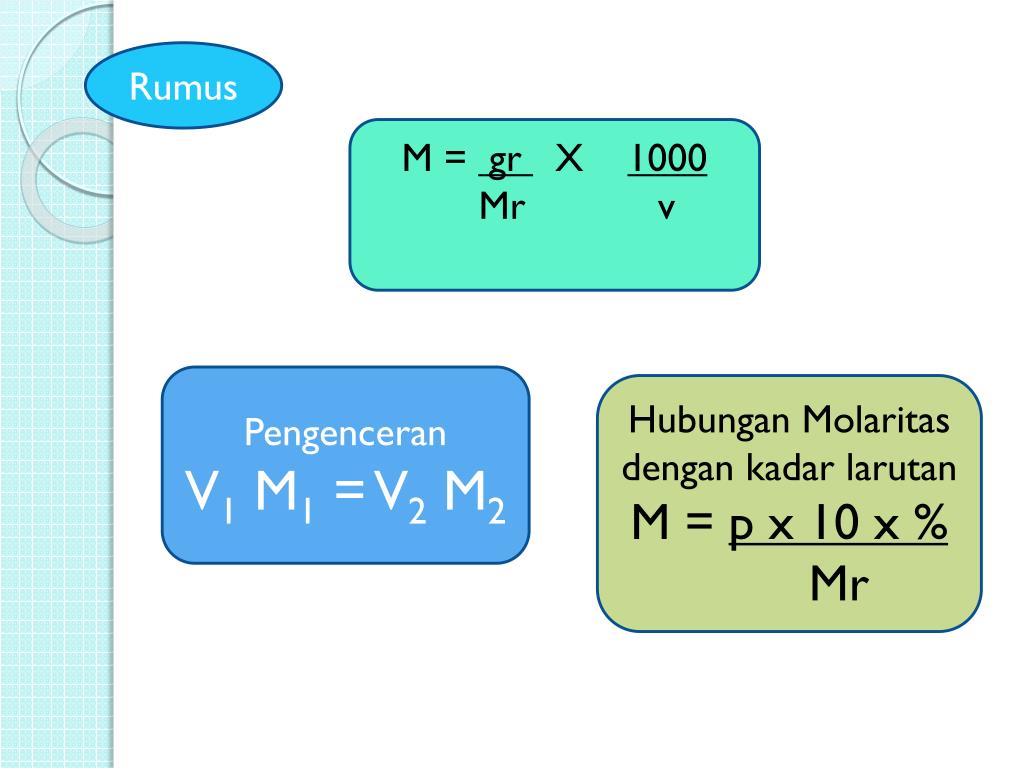
PPT MolaRitas PowerPoint Presentation, free download ID5565192
Konsentrasi Larutan: Pengantar, Persen Massa, Molaritas, Molalitas, Fraksi Mol [Lengkap+Contoh Soal] Ditulis oleh Husnul Khatimah • 17 Februari 2024. Banyaknya zat terlarut dalam larutan dinyatakan dengan konsentrasi larutan yang terdiri dari persen massa, molaritas, molalitas, dan fraksi mol. Pada artikel ini akan membahas materi konsentrasi.

KONSENTRASI LARUTAN MOLARITAS, MOLALITAS, DAN FRAKSI MOL YouTube
Molaritas (juga disebut konsentrasi molar, konsentrasi jumlah, atau konsentrasi zat) adalah ukuran konsentrasi dari spesies kimia, khususnya zat terlarut dalam larutan, dalam hal jumlah zat per satuan volume larutan. Dalam kimia, satuan molaritas yang paling umum digunakan adalah jumlah mol per liter, yang memiliki lambang satuan mol/L atau mol/dm 3 dalam satuan SI.

cara menghitung molaritas dan contoh soal brighto.my.id
Salah satu satuan konsentrasi larutan yang sering digunakan dalam materi kimia adalah molaritas/kemolaran dengan lambang M. Dalam Video ini akan dijelaskan t.

Menghitung Molalitas Larutan Jika Diketahui Molaritas dan Kerapatan Larutannya YouTube
Dikutip dari modul Guru Pembelajar IPA Terapan Kemdikbud yang disusun oleh Euis Siskaningrum, molaritas adalah jumlah mol zat terlarut dalam satu liter larutan. Molaritas dinyatakan dengan lambang M. Satuan dari molaritas adalah mol/liter atau molar (M). Molaritas sama dengan jumlah mol zat terlarut dibagi dengan volume larutan dalam liter.

PPT MolaRitas PowerPoint Presentation, free download ID5565192
Lambang konsentrasi molaritas adalah M. Sebagai contoh, jika terdapat 1 mol garam dalam 1 liter air, maka konsentrasi molaritasnya adalah 1 M. Fraksi Mol (x) Fraksi mol (x) adalah konsentrasi yang dinyatakan dalam perbandingan jumlah mol zat terlarut dengan jumlah total mol zat terlarut dan pelarut. Lambang konsentrasi fraksi mol adalah x.

Perbedaan Molaritas Dan Molalitas Riset
Dalam bidang kimia ada beberapa satuan yang sering digunakan untuk menyatakan konsentrasi larutan ( banyaknya zat terlarut dalam sejumlah pelarut ). Beberapa satuan konsentrasi itu antara lain : mol, molalitas, molaritas, normalitas, ppm, persen massa, persen volum. Berikut akan saya jelaskan pengertian dan rumus dari satuan-satuan di atas : 1.

Cara mudah mencari molaritas atau konsentrasi larutan soal kimia SMA YouTube
Jadi, fraksi mol masing - masing adalah : X A = 0,25. X B = 0,5. X C = 0,25. Dari ketiga fraksi mol di atas, jika dijumlahkan harus menghasilkan 1 sesuai rumus : X A + X B + X C = 1. 0,25 + 0,5 + 0,25 = 1. Demikian pembahasan dari kami, semoga bermanfaat dan menambah wawasan serta pengetahuan kalian. Sekian terima kasih.

Kimia 12 Molaritas Molalitas dan Fraksi Mol YouTube
Lambang dari molaritas yakni notasi M (besar) dengan satuan molar yang setara dengan mol/liter. Baca: Asam Basa. Rumus Molaritas.. Istilah 'molaritas' dan 'molalitas' seringkali membuat beberapa orang kebingungan karena penulisan dan lafalnya yang mirip. Walaupun sama-sama digunakan untuk mengukur konsentrasi larutan, keduanya.

Pengertian Dan Rumus Molaritas Dan Contoh Soal Molaritas Lengkap Riset Riset
Konsentrasi larutan yang biasa dipakai pada laboratorium, yaitu Molaritas, Molalitas, Normalitas, Fraksi Mol, Konsentrasi dalam Persen, Parts per Million (ppm) dan Parts per Billion (ppb), dan Keformalan.. Lambang: Nama: Rumus %W/W: Persen berat: gram zat terlarutgram larutan x 100 %V/V: Persen volume: mL zat terlarutmL larutan x 100 %W/V: