
Is CO(NH2)2 (Urea) Polar or NonPolar? YouTube
Jumlah dari muatan ion positif dan ion negatif akan sama sehingga muatan ion-ion dalam larutan netral. Ion-ion inilah yang kemudian menghantarkan arus listrik.. Urea = CO (NH2)2; Glukosa = C6H12O6; Sukrosa = C12H22O11; Etanol = C2H2OH; Contoh reaksi larutan non-elektrolit

Sebanyak 1.200 kg pupuk urea, CO(NH2)2, disebar secara merata pada 10 hectare Soal OSNP Kimia
Transformasi geometri. Contoh soal sifat koligatif larutan nomor 1 Sebanyak 84 gram KOH (Ar K = 39 g/mol, Ar O = 16 g/mol, Ar H = 1 g/mol) dilarutkan dalam 750 g air. Konsentrasi larutan adalah.A. 2,0 MB. 1,5 MC. 1,0 MD. 2,0 mE. 1,5 m Pembahasan Dengan menggunakan rumus molalitas diperoleh hasil sebagai berikut. m.

Nama ion kompleks [Co(H2O)2 (NH3)4]^(3+) adalah ion....
NH2 anion. Formula: H 2 N -. Molecular weight: 16.0231. CAS Registry Number: 17655-31-1. Information on this page: Notes. Other data available: Reaction thermochemistry data. Gas phase ion energetics data.

Share Center Larutan Urea CO(NH2)2
The number of moles and the mass (in kg) of copper(II) carbonate needed to decompose in order to produce 1.500 kg of copper(II) oxide, where CO 2 is the other product. The number of moles and mass (in grams) of C 2 H 4 required to react with water to produce 9.55 g C 2 H 6 O.

Nh2 Functional Group KierrahasAtkins
A compound (CO(NH2)2), formed in the liver from ammonia produced by the deamination of amino acids. It is the principal end product of protein catabolism and constitutes about one half of the total urinary solids.

Sebanyak 1.500 gram urea (CO(NH2)2) dibuat berdasarkan re...
M r CO(NH2)2 = = = Ar C+Ar O+(2×Ar N)+(4×Ar H) 12 +16 +(2×14)+(4× 1) 60 g mol−1. nO = = = M r CO(NH2)2Ar O × nCO(NH2)2 6016 × 0,2 0,053 mol. Jumlah atom O = = = n× 6,02 ×1023 0,053×6,02× 1023 3,2×1022 atom. Oleh karena itu, jumlah atom oksigen yang terdapat dalam 0,2 mol urea adalah 3,2×1022 atom. Jadi, jawaban yang tepat yaitu 3.

Is NH2 polar or nonpolar? Techiescientist
n merupakan jumlah ion dalam larutan elektrolit. Karena konsentrasi larutan sama sehingga untuk menentukan titik didih yang sama bisa ditentukan melalui jumlah ion : reaksi ionisasi KOH : reaksi ionisasi MgCl 2: reaksi ionisasi : jumlah ion KOH dan NaBr sama sehingga akan memiliki titik didih yang sama. Jadi, jawaban benar adalah C.

Co Nh2 2 Molar Mass Lillian Bailey
Tentukan molalitas dari 90 gram urea CO(NH2)2 dalam 500 gram air. Penyelesaian: Diket: Ar C = 12 Ar H = 1 Ar 0 = 16 Ar N = 14 Massa urea = m = 90gram Massa air = p = 500gram.. Dari persamaan diatas, jumlah ion OH- adalah 1 sehingga valensi KOH adalah 1. Valensi = 1. Tentukan normalitas larutan KOH. N = M x valensi N = 2 x 1 N = 2N.

Molecular Model of Urea (CO(NH2)2) Molecule. Vector Illustration Stock Vector Image & Art Alamy
[Fe(CN)6]4-= ion heksasiona ferat (II) [Cu(OH)4]2-= ion tetrahidrokso cuprat (II) [Co(Br)6]3-= ion heksabromo kobaltat (III) Bilangan koordinasi merupakan jumlah ligan yang diikat oleh atom pusat. Muatan ion kompleks merupakan jumlah ion dari muatan ion pusat dan muatan ligan-ligan yang diikatnya. Baca juga: Tata Nama Senyawa Ion . Referensi.
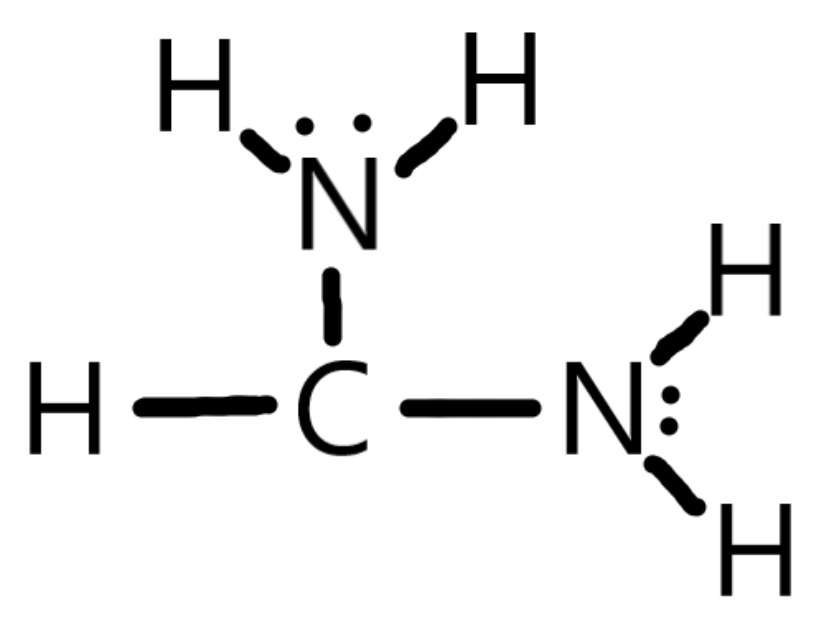
CH(NH2)2+ Lewis Structure Name Formal Charge
1. CO(NH2)2 0,1 M Urea adalah larutan non elektrolit Tb = Kb x m Tb = 0,1 M x 0,52^c/mol Tb = 0,052 2. CH3COOH 0,2 M CH3COOH adalah larutan elektrolit lemah yang nilai faktor vant hoffnya lebih dari 0 namun kurang dari 1. Jika faktor vant hoff CH3COOH dianggap 0,5 Tb = Kb x m x i Tb = 0,2 M x 0,5 x 0,52^c/mol Tb = 0,052 3.

Molecular Model of Urea (CO(NH2)2) Molecule. Vector Illustration Stock Vector Image & Art Alamy
n = jumlah ion; α = derajat ionisasi; Contoh soal dan pembahasan. Contoh soal 1. Sebanyak 2,4 gram urea (Mr = 60) dilarutkan dalam 50 gram air. Jika Kf air = 1,86 °C/m, tentukanlah titik beku larutan.. Jika Mr CO(NH2)2 = 60 dan Mr NaCl = 58,5 serta derajat inonisasi NaCl = 1, besarnya tetapan penurunan titik beku molal dari kedua percobaan.

How to Find the Number of Atoms in CO(NH2)2 (Urea) YouTube
Urea adalah senyawa organik yang tersusun dari unsur karbon, hidrogen, oksigen dan nitrogen dengan rumus CON 2 H 4 atau (NH 2) 2 CO.. Urea juga dikenal dengan nama carbamide yang terutama digunakan di kawasan Eropa. Nama lain yang juga sering dipakai adalah carbamide resin, isourea, carbonyl diamide, dan carbonyldiamine.Senyawa ini adalah senyawa organik sintesis pertama yang berhasil dibuat.

NH2 Molecular Geometry, Bond Angles (and Electron Geometry) YouTube
Elektrolit lemah jumlah ion yang terionisasi sedikit sedangkan elektrolit kuat hampir seluruh molekulnya terionisasi. 4. Dengan menguji elektrolit, elektroda dimasukkan ke dalam asam klorida.. CO(NH 2) 2 (aq) c. CH 3 COOH (aq) d. NH 4 OH (aq) e. C 6 H 12 O 6 (aq) Jawaban: A. Pembahasan : HBr merupakan elektrolit kuat. 8.
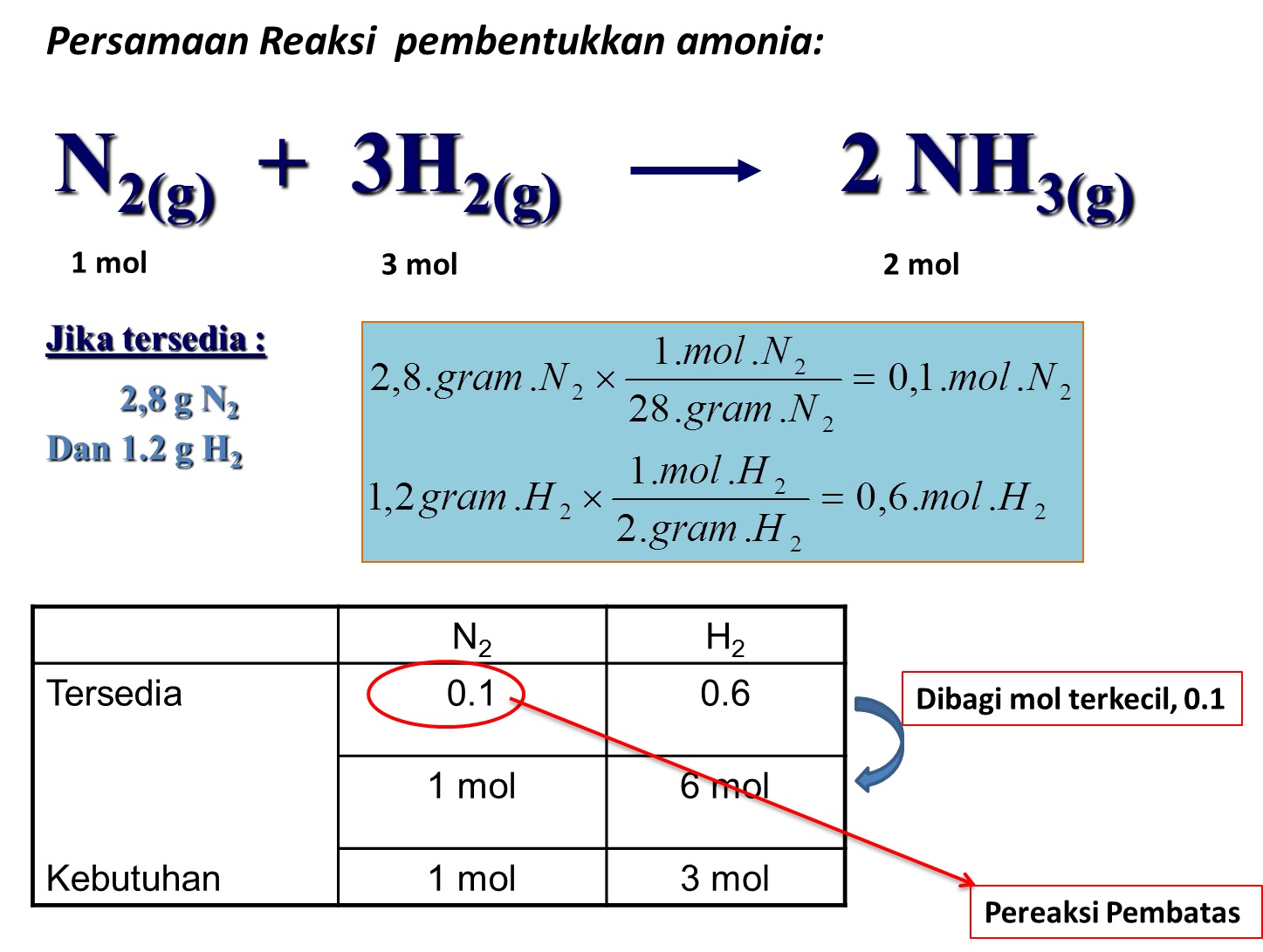
pengertian pereaksi pembatas MateriKimia
5. Tentukan jumlah ion elektrolit-elektrolit dari CaCO 3 adalah… A. 1 B. 3 C. 2 D. 4 E. 5. Pembahasan: CaCO 3 Ca 2+ + CO 3 2-Jumlah Ca 2+ adalah 1 Jumlah CO 3 2- adalah 1 Jumlah ion adalah 2 (elektrolit biner). Jadi, jawabannya adalah C. 6. Larutan natrium hidroksida mempunyai derajat ionisasi 1, artinya… A. Tidak Terionisasi B. Terionisasi.
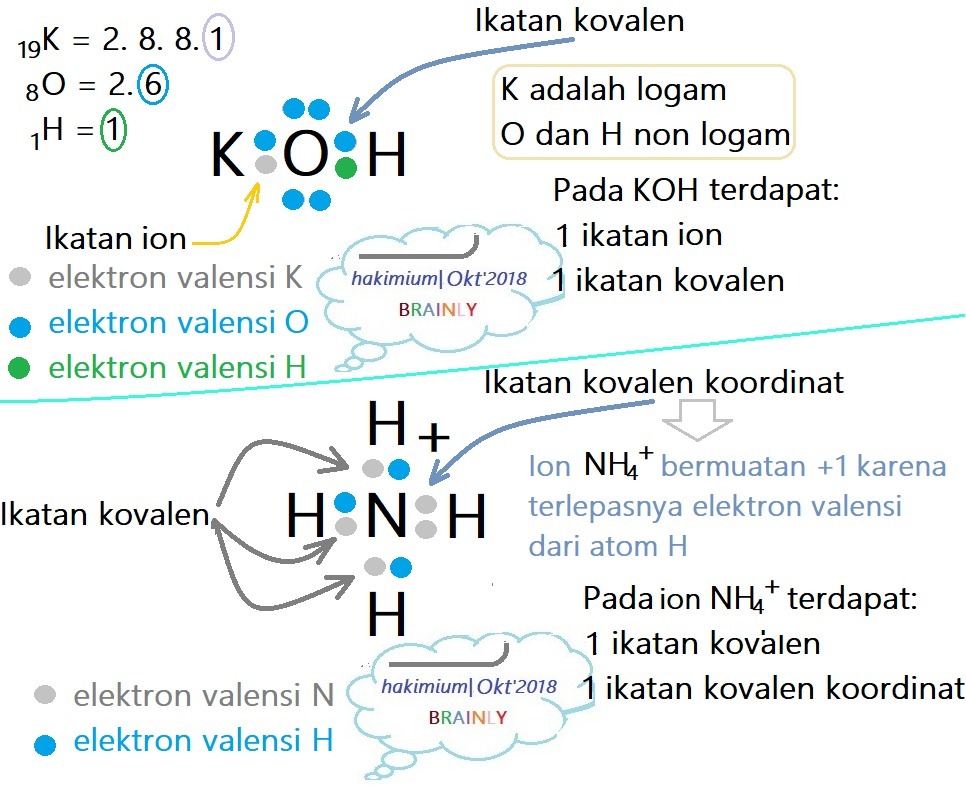
Pembahasan Soal Senyawa dan Ion yang Mempunyai Ikatan Kovalen dan Ikatan Ion Sekaligus MateriKimia
4.CO(NH2)2 atau urea adalah senyawa kovalen non polar jika dilarutkan dalam air tidak terjadi reaksi ionisasi 20. Tentukan massa dari CO(NH2)2 yang terdapat pada 500 mL larutan CO(NH2)2 0,2 M. Diketahui Mr CO(NH2)2 = 60. Massa CO(NH₂)₂ yang harus dilarutkan adalah 6 gram. Massa tersebut dapat ditentukan menggunakan rumus kemolaran.
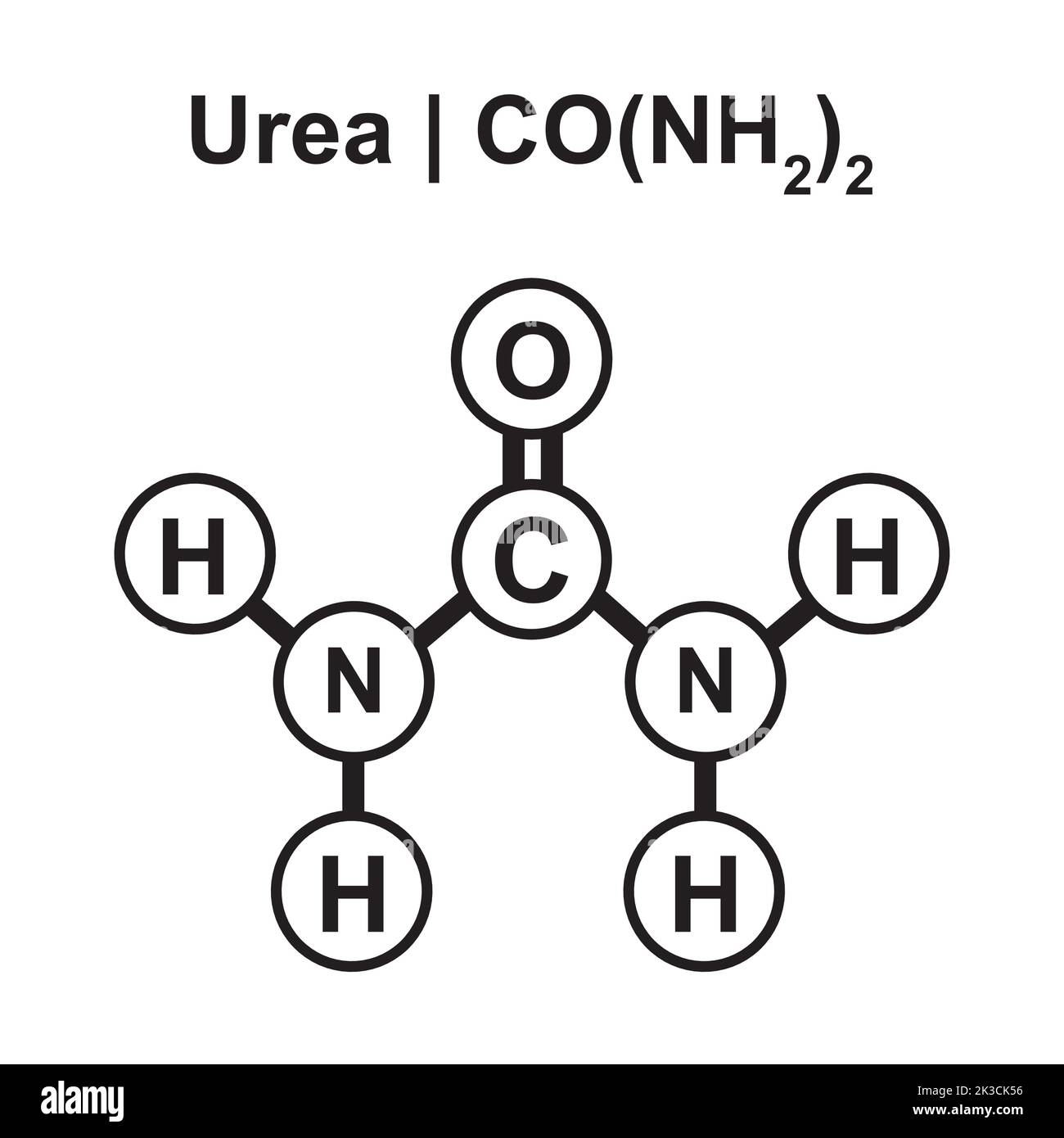
Co(nh2)2 Lewis Structure
Molekul Senyawa - Ketika duduk di bangku sekolah, Grameds pasti sudah pernah mendapatkan penjelasan mengenai materi atom dan molekul dong, terutama pada mata pelajaran kimia?Yap, atom, molekul, ion, dan senyawa ini menjadi beberapa pembahasan pokok dalam pembelajaran kimia yang mana merupakan partikel-partikel terkecil dari suatu benda dan tidak dapat dilihat dengan mata telanjang.