
Cara Menentukan Senyawa Bersifat Asam Basa Atau Netral Digunakan
1. Memiliki persamaan dengan teori Bronsted dan Lowry, yaitu dapat menjelaskan sifat asam, basa dalam pelarut lain maupun tidak mempunyai pelarut. 2. Teori asam basa Lewis mampu menjelaskan sifat asam basa molekul atau ion yang mempunyai pasangan elektron bebas atau yang dapat menerima pasangan elektron bebas.

Konsep Mudah Belajar Teori Asam Basa LewisKimia SMA YouTube
Menurut Lewis, asam merupakan akseptor pasangan elektron dan basa merupakan pendonor pasangan elektron. Teori ini juga diklaim memiliki kelebihan dalam mengidentifikasi reaksi asam-basa yang berada dalam benda padat, gas, dan medium pelarut lain (bukan air biasa), serta tidak melibatkan transfer proton (teori Bronsted-Lowry).
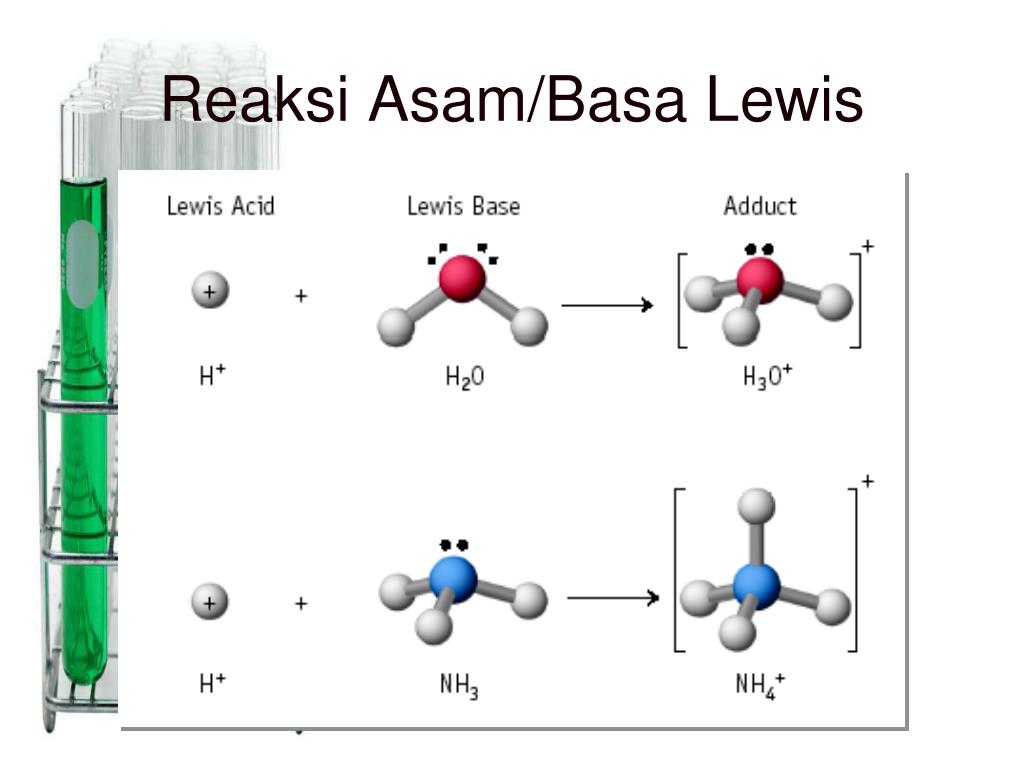
PPT teori asam basa PowerPoint Presentation, free download ID78826
asam adalah senyawa yang jika dilarutkan dalam air melepaskan ion H +. basa adalah senyawa yang jika dilarutkan dalam air melepaskan ion OH −. Gas asam klorida (HCl) yang sangat larut dalam air tergolong asam Arrhenius, sebagaimana HCl dapat terurai menjadi ion H + dan Cl − di dalam air.
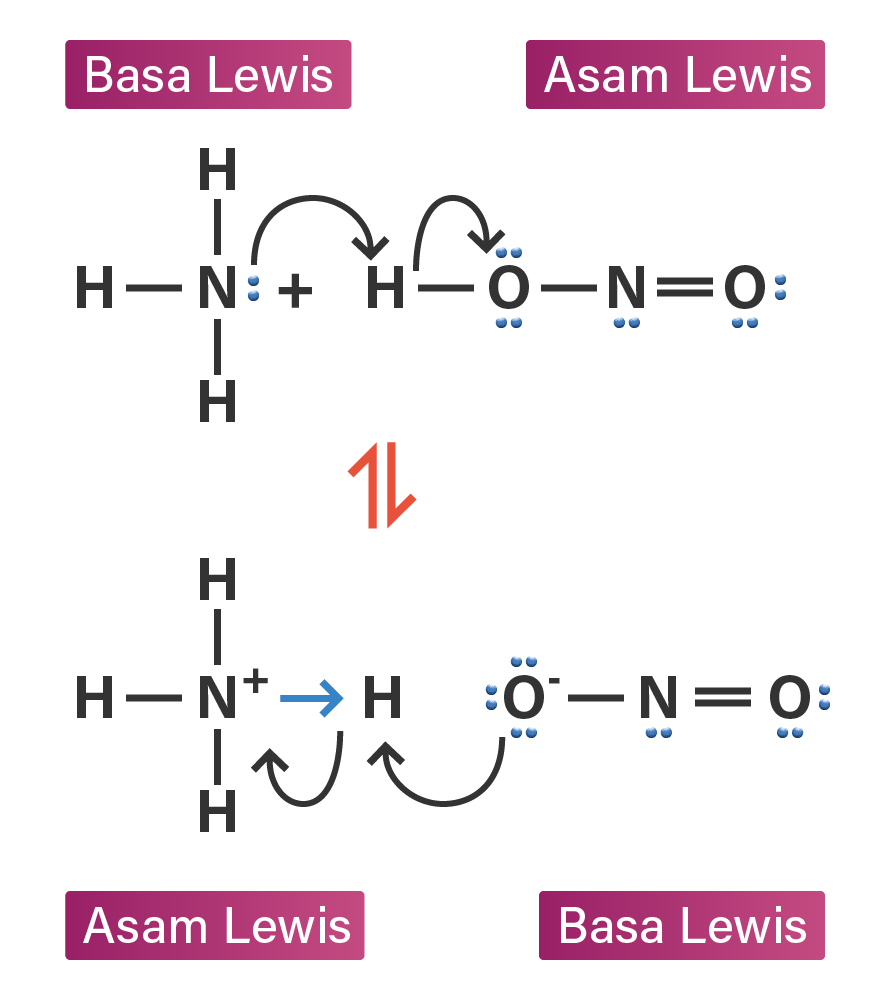
tuliskan pasangan asam basa lewis dari reaksi beri...
Asam Basa Lewis - Dalam pelajaran kimia pastinya kita mengenal apa itu asam dan basa. Keduanya merupakan golongan zat kimia yang sangat mudah ditemui di sekitar kita. Contoh asam yang ada di sekeliling kita adalah cuka, asam sitrun ataupun asam dalam lambung kita. Sedangkan yang tergolong basa misalnya adalah kapur sirih atau soda api.

Pengertian Asam Basa Menurut Lewis cara menghemat air
Pengertian asam menurut ilmu kimia berarti sebuah senyawa kimia atau zat yang bisa dilaturkan dalam air dan akan menghasilkan larutan dengan pH yang lebih kecil dari 7 serta yang bisa memberikan proton [ion H+] pada zat lain atau senyawa lain yang dinamakan dengan basa.
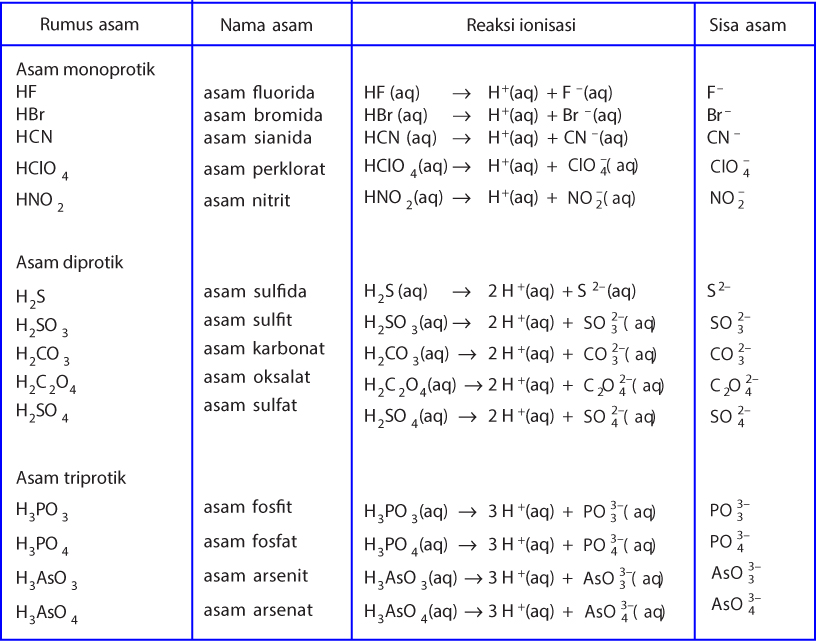
Teori Asam Dan Basa Menurut Arrhenius, BronstedLowry, dan Lewis ezy blog
Brønsted-Lowry: Menurut definisi ini, asam adalah pemberi proton kepada basa. Asam dan basa bersangkutan disebut sebagai pasangan asam-basa konjugat.. Lewis: Menurut definisi ini, asam adalah penerima pasangan elektron dari basa. Definisi yang dikemukakan oleh Gilbert N. Lewis ini dapat mencakup asam yang tak mengandung hidrogen atau proton.

studying chemistry belajar kimia Teori Asam Basa Lewis
Asam dan basa adalah larutan elektrolit dengan ciri khas tersendiri. Secara kimia, asam dapat juga diartikan sebagai zat elektrolit yang apabila dilarutkan dalam air akan menghasilkan ion hidrogen (H+). Sementara itu, basa adalah zat elektrolit yang dapat menghasilkan ion hidroksida (OH-) di dalam air.

Teori Asam Basa
1. Teori Asam Basa Arhennius Arhennius berhasil mengemukakan teori asam basa usai mengembangkan teori dissosiasi elektrolit. Dalam teori asam basa, Arhennius menjelaskan bahwa asam adalah senyawa yang mengandung hidrogen dan melepaskan ion hidrogen jika dilarutkan dalam air.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Teori Lewis (1923) menjelaskan bahwa asam adalah senyawa yang bersedia untuk berbagi pasangan elektron dengan atom atau molekul lain, dan basa adalah senyawa yang bersedia untuk menerima pasangan elektron dari atom atau molekul lain. Teori Lewis ini lebih menekankan pada aspek elektronik daripada aspek proton.

Konsep Mudah Belajar Teori Asam Basa BronstedLowry Kimia SMA YouTube
1. Teori Asam Basa Arrhenius Teori pertama asam bas aini dicetuskan pertama kali oleh seorang ahli kimia berasal dari Swedia bernama Svante Arrhenius. Teori ini menghubungkan sifat keasaman dengan ion hidrogen atau H+ dan pertama kali dicetuskan pada tahun 1884.
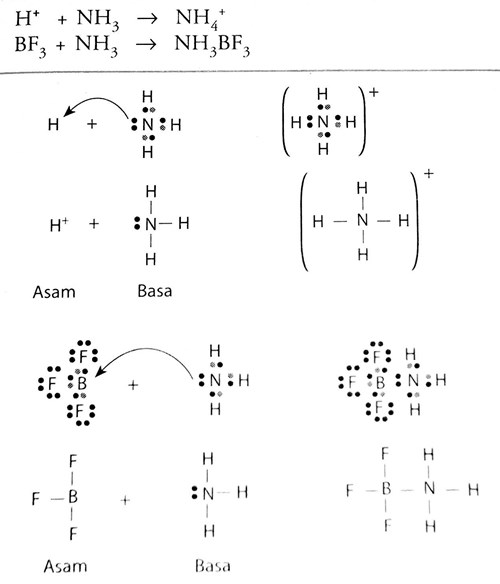
Teori AsamBasa Lewis
Mereka adalah Svante Arrhenius, Bronsted-Lowry, dan Lewis. Berikut ini penjelasan mengenai teori-teori yang mereka kemukakan: 1. Asam Basa Menurut Arrhenius. Menurut Arrhenius, asam adalah zat yang menghasilkan ion hydronium (H+) saat dimasukkan ke dalam air. Sedangkan basa, menghasilkan zat lain yang berupa ion hidroksida (OH-).

Teori Asam Basa
Lalu didalam Teori Asam Basa menurut Lewis ini bahwa Asam merupakan suatu Senyawa Kimia (Zat) yang bisa menerima Pasangan Elektron dari Senyawa (Zat) lain atau bisa dikatakan Akseptor pasangan Elektron, sedangkan Basa Menurut Teori Asam Basa Lewis ialah suatu Senyawa Kimia (Zat) yang bisa memberikan pasangan Elektron kepada Senyawa yang lain ata.
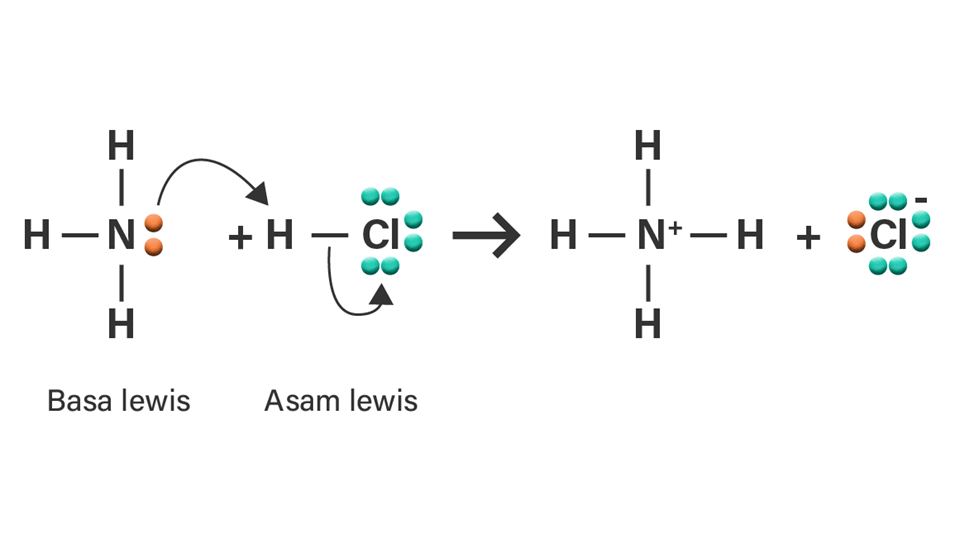
Tentukan asam dan basa menurut Lewis dari NH3
Dilansir dari Chemguide, menurut Arrhenius, asam adalah zat yang menghasilkan ion hidrogen (H+) dalam larutan sedangkan basa adalah zat yang menghasilkan ion hidroksida (OH-) dalam larutan. Asam dan basa dapat bereaksi menghasilkan air dan senyawa ionic garam, reaksi tersebut disebut dengan reaksi netralisasi.

LENGKAP ‼️ Teori Asam Basa Lewis Latihan Soal dan Pembahasan YouTube
Asam dan basa adalah larutan elektrolit yang dikenal dengan ciri khasnya, seperti asam yang memiliki rasa masam dan basa yang memiliki rasa pahit. Asam dan basa pengertian menurut Kamus Besar Bahasa Indonesia (KBBI), asam adalah zat yang dapat memberikan proton, zat yang dapat membentuk ikatan kovalen dengan menerima sepasang elektron.
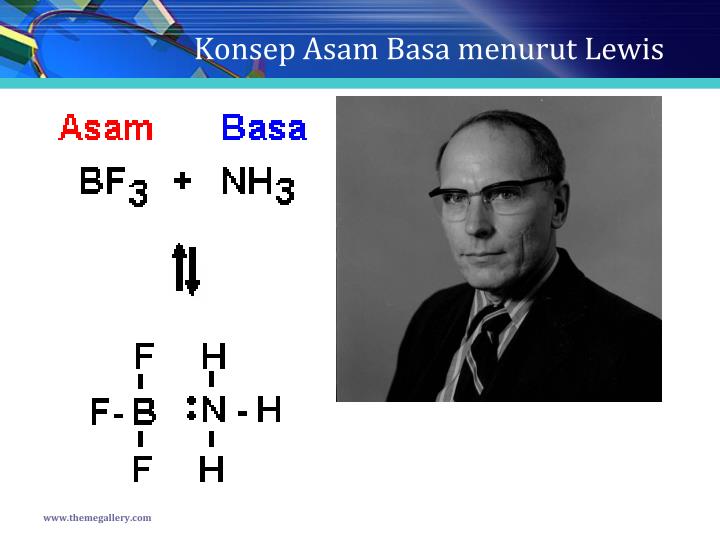
Konsep Asam Basa Menurut Lewis Pengertian Dan Contohnya Jempol Kimia Riset
Trimetilborana (Me 3 B) adalah suatu asam Lewis karena mampu menerima pasangan elektron sunyi. Dalam suatu aduk Lewis, asam dan basa Lewis berbagi pasangan elektron yang dilengkapi oleh basa Lewis, membentuk ikatan koordinasi. [1] Dalam konteks reaksi kimia tertentu antara NH 3 dan Me 3 B, pasangan elektron sunyi dari NH 3 akan membentuk ikatan.

XI.6.q. Teori Asam Basa Lewis (Teori) YouTube
Menurut Arrhenius, definisi dari asam dan basa, yaitu: Asam adalah senyawa yang bila dilarutkan dalam air melepaskan ion H+. Baca juga: Pakaian Adat Jawa Timur: Penjelasan Lengkap beserta Gambarnya Basa adalah senyawa yang bila dilarutkan dalam air melepaskan ion OH−. Misalnya asam klorida (HCl) dan asam asetat (CH 3 COOH).