Memahami Senyawa Koordinasi dari Ikatan Kovalen dan Ikatan NonKovalen
Gaya dipol permanen atau cukup disebut sebagai 'gaya dipol' adalah gaya intermolekuler yang dimiliki molekul polar. Gabungan gaya dipol dan gaya dispersi disebut sebagai gaya Van der Waals.. Diantara semua gaya intermolekuler, ikatan hidrogen adalah yang paling kuat. Perhatikan bahwa istilah 'ikatan' disini tidak sama dengan ikatan.

Animasi Gaya DipolDipol atau Gaya Keesom YouTube
Selanjutnya, dipol sesaat dan dipol imbasan ini akan menimbulkan gaya tarik menarik yang menghasilkan gaya London.. Jenis gaya antar molekul yang bertanggung jawab atas keberadaan molekul DNA ini adalah ikatan hidrogen. 2. Pembentukan gelembung pada sabun. Gelembung sabun terdiri dari molekul sabun dan molekul air. Air adalah molekul polar.

gaya interaksi dipoldipol!!!!. YouTube
KOMPAS.com - Gaya antarmolekul adalah gaya yang terjadi di antara atom-atom sehingga dapat membentuk molekul ataupun senyawa tertentu.. Gaya antarmolekul terdiri dari gaya London atau dipol-dipol, gaya Van der Waals, dan ikatan hidrogen.Simak penjelasannya seperti dikutip dari Encyclopaedia Britannica:. Gaya London. Gaya london adalah gaya tarik menarik antaratom karena adanya dipol sesaat.
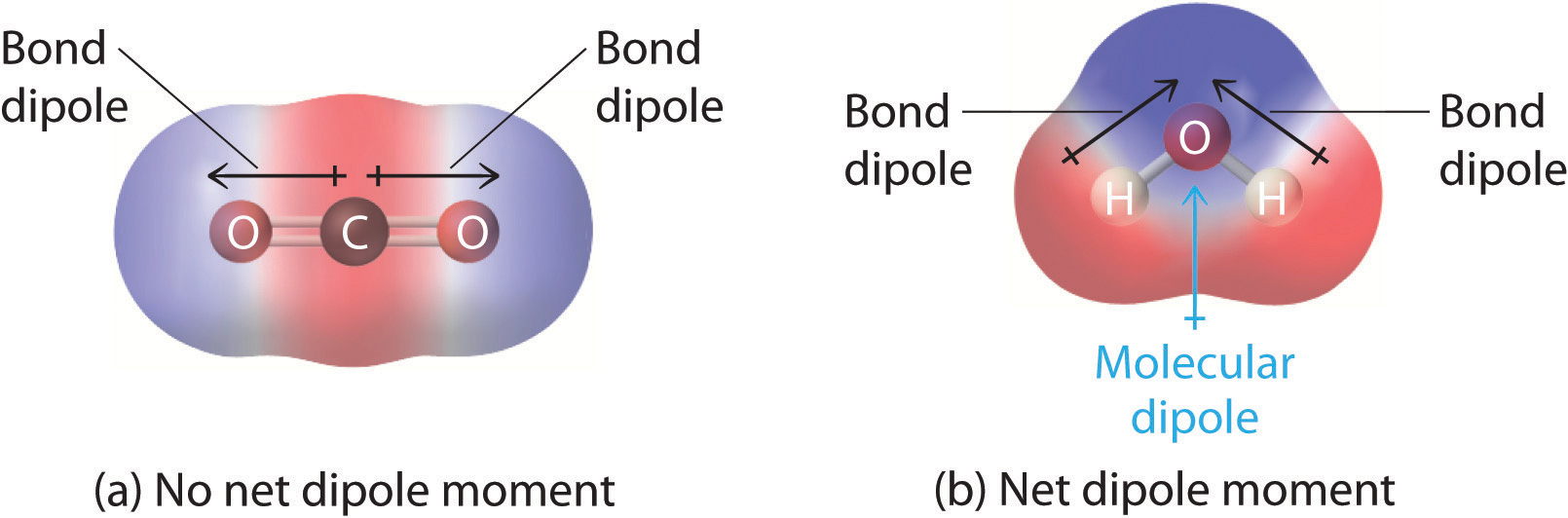
2.2 Polar Covalent Bonds Dipole Moments Chemistry LibreTexts
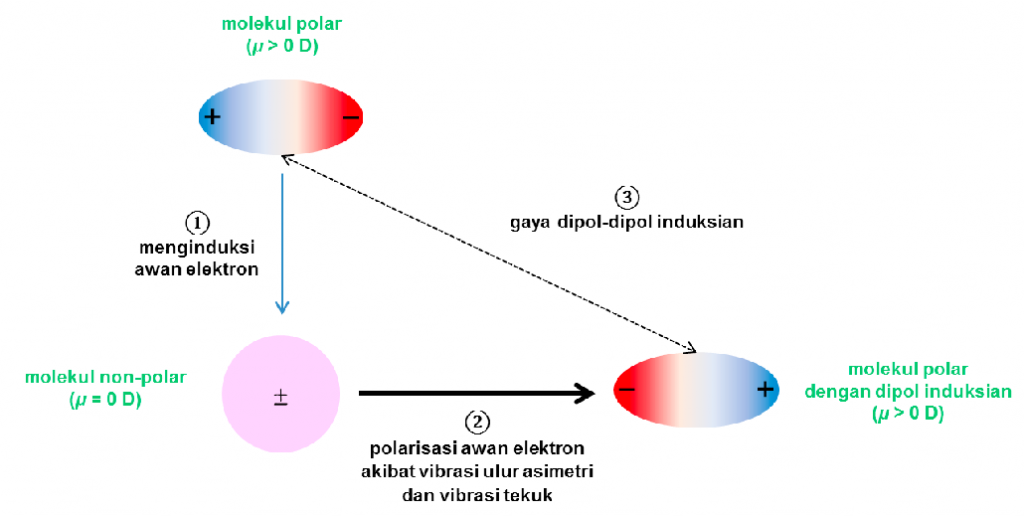
Interaksi ini terjadi antara ion dan dipol terinduksi. Ikatan ini relatif lemah karena kepolaran molekul terinduksi relatif kecil daripada dipol permanen. Interaksi dipol-dipol terinduksi;. Bisa dikatakan juga bahwa gaya ini adalah yang terlemah dibandingkan dengan gaya lainnya. Gaya ini pertama kali ditemukan oleh ahli fisika asal Jerman.
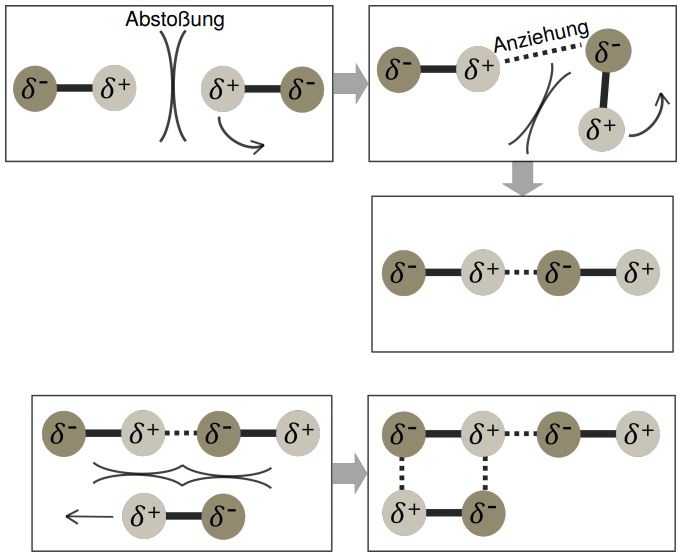
Zwischenmolekulare Wechselwirkungen StudyHelp OnlineLernen
8.3 Dipol seketika ke dipol terimbas (van der Waals) 8.4 Interaksi kation-pi. 9 Elektron pada ikatan kimia. 10 Fenomena.. Ikatan kimia adalah sebuah proses fisika yang bertanggung jawab dalam interaksi gaya tarik menarik antara dua atom atau molekul yang menyebabkan suatu senyawa diatomik atau poliatomik menjadi stabil.

(DOC) Gaya DipolDipol Juliantari Dewi Academia.edu
Namun, ikatan ini dibedakan secara khusus karena kekuatan gaya interaksinya relatif lebih kuat dibanding gaya dipol-dipol umumnya. Hal ini dikarenakan atom hidrogen tidak memiliki elektron inti yang dapat melindungi (shielding) inti atom dan ukurannya cukup kecil sehingga dapat lebih didekati oleh molekul-molekul lain dan jarak antara hidrogen.

Soal Kimia Gaya Antar Molekul Latihan Soal Yuk
Gaya Antarmolekul : Gaya London, Gaya Tarik Dipol, dan Ikatan Hidrogen. Gurubagi.com. Gaya antar molekul adalah gaya yang terjadi antara atom-atom, sehingga dapat membentuk molekul tertentu yang memiliki ikatan sesuai dengan kekuatan atom-atom tersebut. Gaya tarik antarmolekul berkaitan dengan sifat-sifat fisik zat, seperti titik leleh, titik.

INTERAKSI IONDIPOL YouTube
Dipol sesaat ini kemudian akan menginduksi terbentuknya dipol sesaat pada molekul lainnya, sehingga hasilnya adalah suatu gaya tarik-menarik antarmolekul yang lemah, seperti digambarkan pada diagram berikut: Kekuatan gaya dispersi suatu molekul tergantung kepada: 1. Luas permukaannya.

(PDF) CONTOH INTERAKSI DIPOLDIPOL PADA ANTAR MOLEKUL POLAR Hanif Ratih Academia.edu
Urutan kekuatan gaya antarmolekul berdasarkan kekuatan dari yang terlemah hingga yang terkuat adalah sebagai berikut. 1. Gaya Van der Waals. Gaya Van der Waals merupakan gaya antarmolekul yang sangat lemah. Gaya Van der Waals dikemukakan oleh Diderik Van der Waals pada awal abad ke- 20. Gaya Van der Waals dibagi menjadi dua, yaitu gaya London.
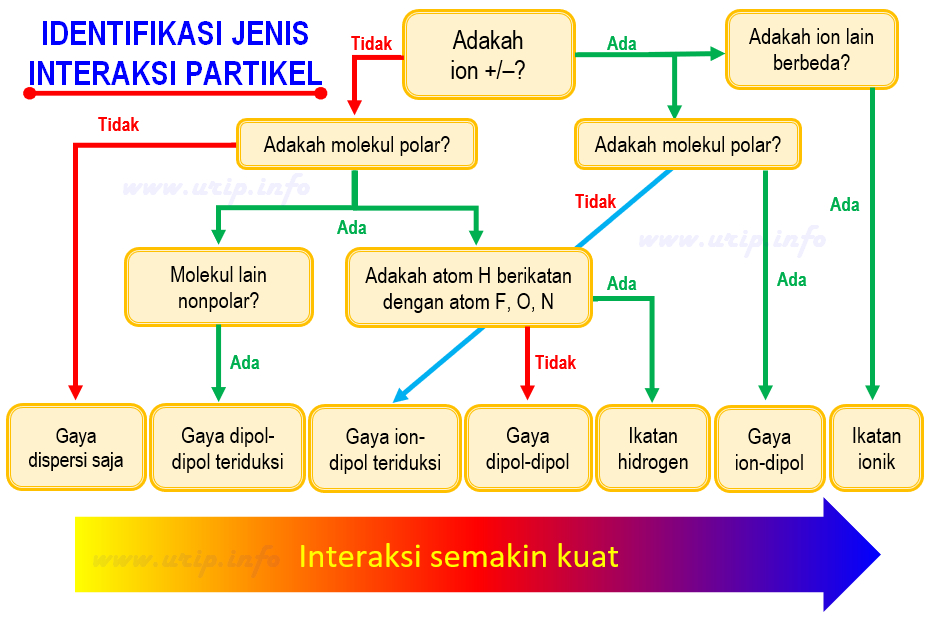
Cara Mengidentifikasi Jenis Gaya Antarmolekul (Antarpartikel) Serba Ada
Dalam kimia, dipol biasanya mengacu pada pemisahan muatan dalam molekul antara dua atom yang terikat secara kovalen atau atom yang berbagi ikatan ion. Misalnya, molekul air (H 2 O) adalah dipol. Sisi oksigen dari molekul membawa muatan negatif bersih, sedangkan sisi dengan dua atom hidrogen memiliki muatan listrik positif bersih.
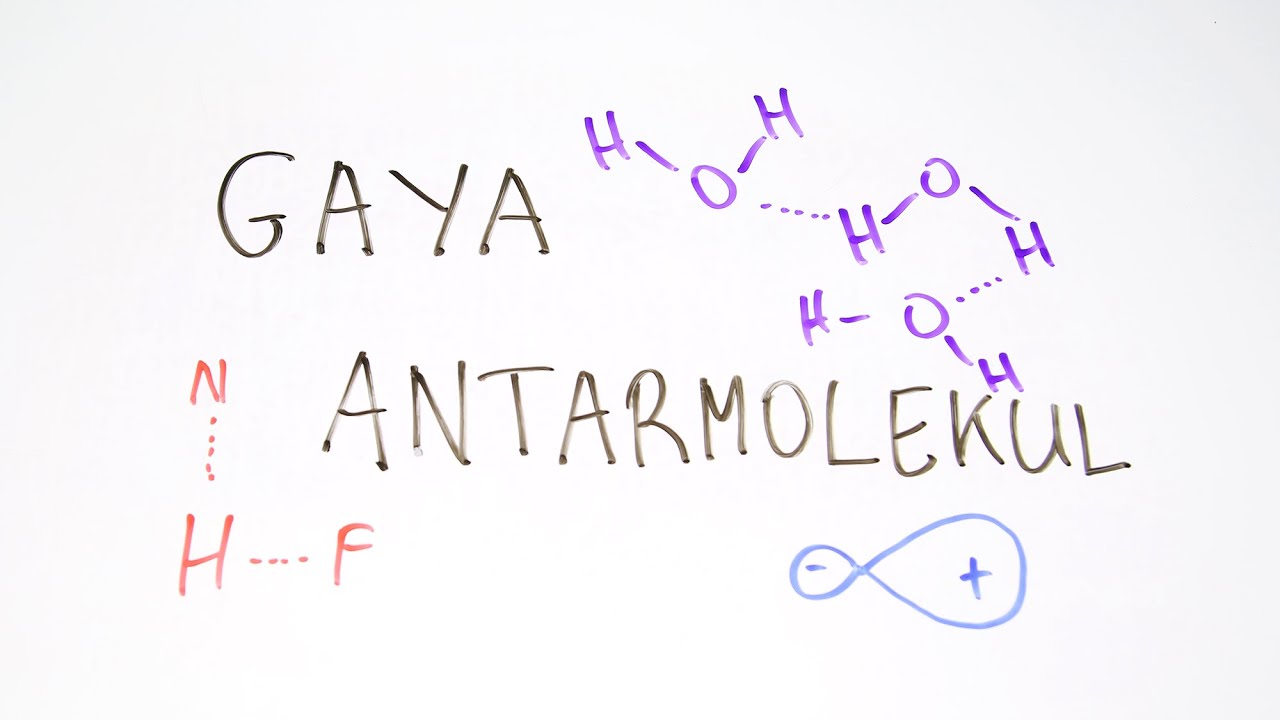
Gaya Antarmolekul Dipoldipol, London, dan Ikatan Hidrogen Kimia Kelas XI YouTube
Gaya antarmolekul terdiri dari 3 jenis: gaya dipol-dipol, gaya london, dan ikatan hidrogen. Apa sih 3 gaya tersebut?=====Kimia kelas X: ht.

PPT GAYA ANTARMOLEKUL PowerPoint Presentation ID5701479
Gaya dipol-dipol adalah gaya tark menarik antara sisi positif molekul polar dengan sisi negatif molekul polar lainnya. Gaya dipol-dipol mempunyai kekuatan yang berkisar antara 5-20 kJ per mol. Gaya ini lebih lemah dibandingkan ikatan kovalen atau ikatan ion, dan mempunyai pengaruh yang signifikan hanya ketika molekul-molekul saling berdekatan.
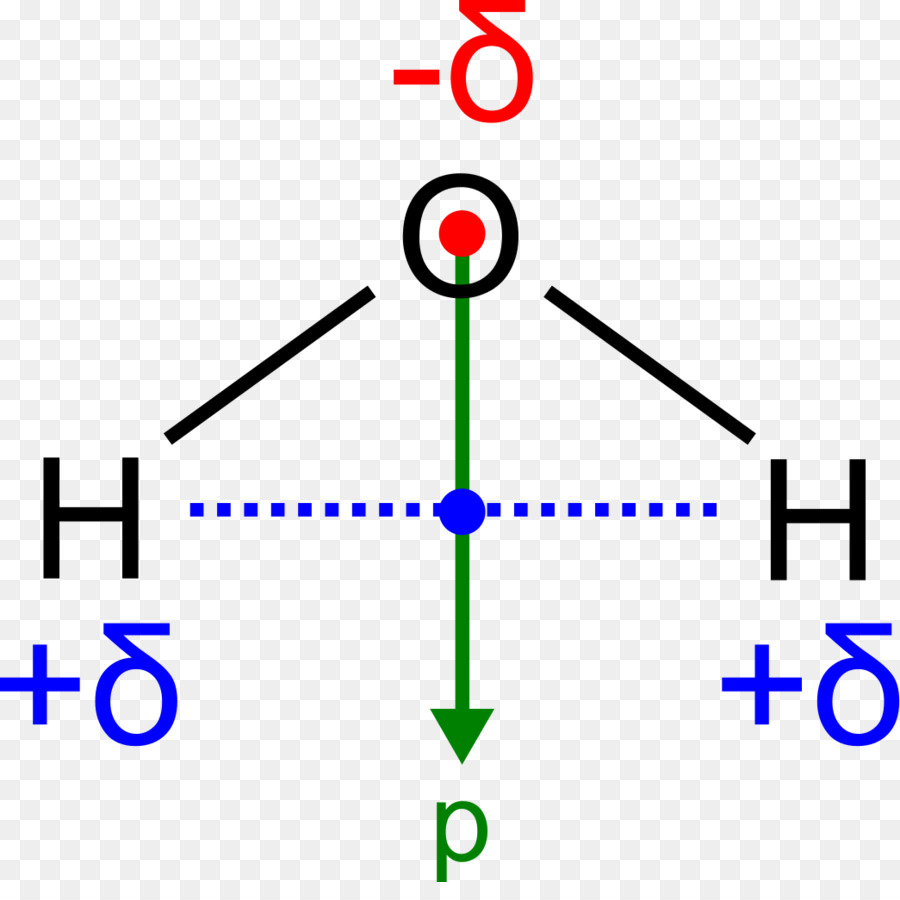
Dipol, Ikatan Dipol Sesaat, Polaritas Kimia gambar png
Konversi. Faktor konversi dipol yang paling bermanfaat adalah: 1 D = 3,335. 64 × 10-30 Cm. Untuk molekul diatomik hanya ada satu (tunggal atau banyak) ikatan sehingga momen dipol ikatan adalah momen dipol molekul, dengan nilai-nilai khas dalam kisaran 0 sampai 11 D. Pada satu ekstrim, molekul simetris seperti klorin (memiliki momen nol dipol.
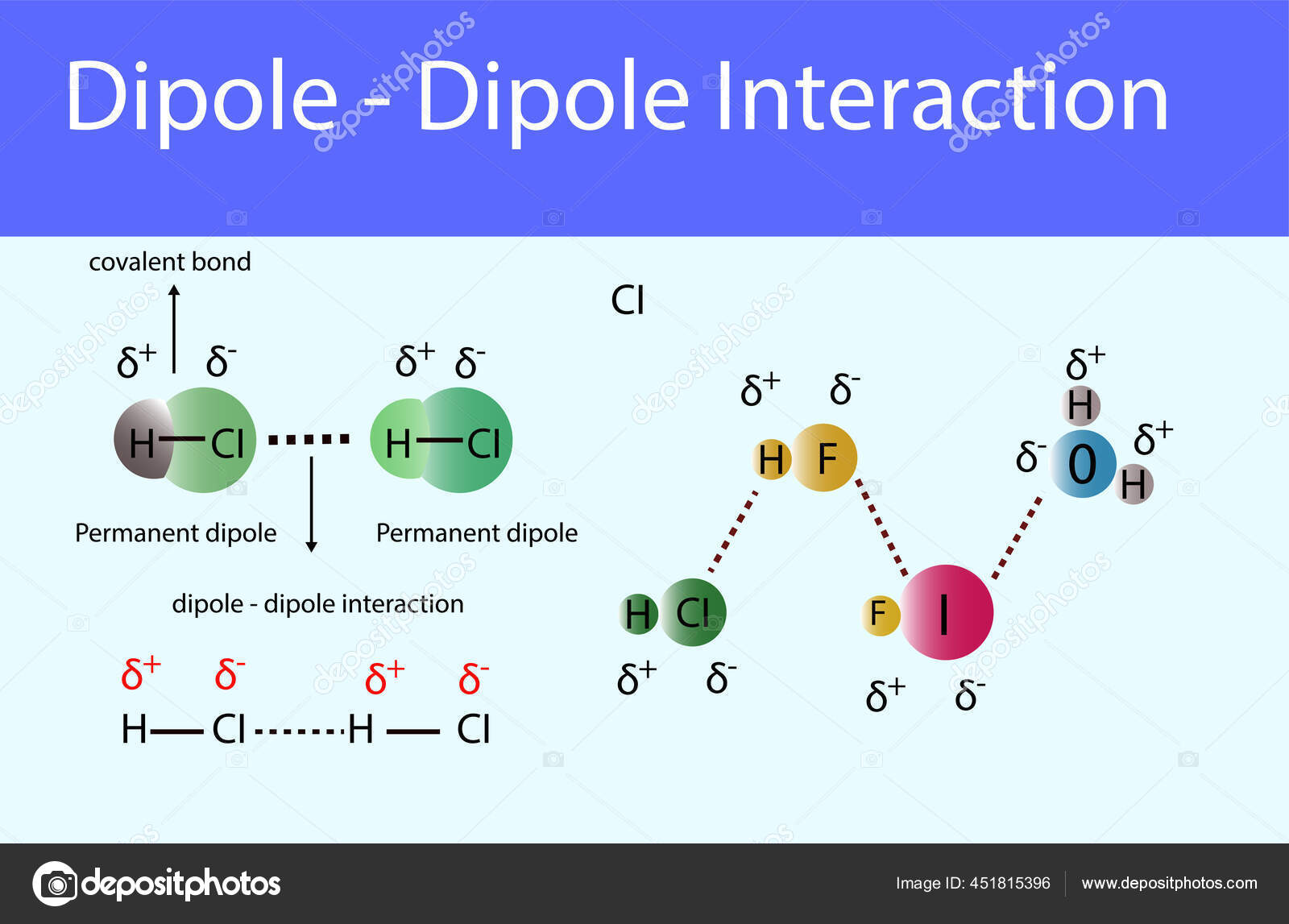
Dipol Dipol Wechselwirkungen Infografik Chemie Unterrichtsfach Dipol lizenzfreie
Ikatan sekunder adalah ikatan antar molekul. Gaya ikatan sekunder timbul dari dipol atom atau molekul. Pada dasarnya dipol listrik timbul jika ada jarak pisah antara bagian positif dan negatif dari sebuah atom dan molekul. Perlu diingat bahwa gaya tarik antarmolekul berikatan dengan sifat-sifat fisis zat, seperti titik leleh dan titik didih.

Dipoldipolbindningar YouTube
Gaya ion-dipol dan gaya dipol-dipol, merupakan istilah yang mengacu pada dua bentuk gaya antarmolekul. Beberapa contoh lain untuk gaya antarmolekul termasuk gaya dipol terinduksi ion, ikatan hidrogen, dan gaya Van der Waal. Gaya-gaya ini adalah gaya tarik elektrostatik karena molekul tertarik berdasarkan muatan listriknya.
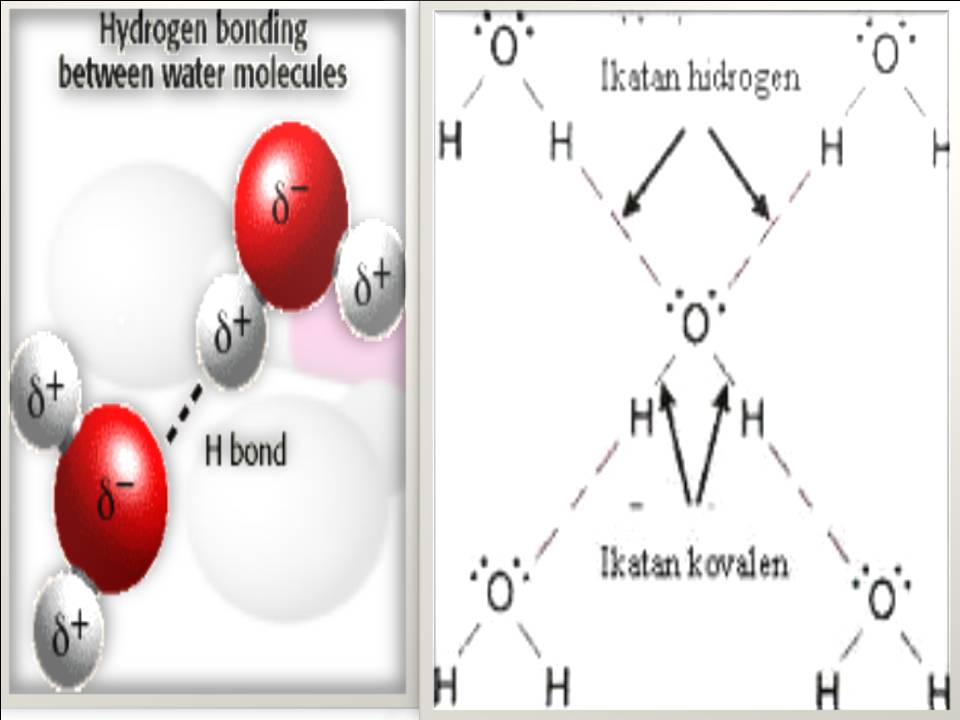
MATERI KELAS 10 GAYA INTERAKSI MOLEKUL
Ikatan hidrogen (hydrogen bond) adalah gaya tarik menarik antara suatu pasangan dari sebuah atom elektronegatif dan sebuah atom hidrogen yang terikat dengan nitrogen, oksigen, atau fluorin. Ikatan hidrogen sering digambarkan sebagai suatu interaksi dipol-dipol elektrostatik yang kuat.