
Menghitung Molalitas, Molaritas, Fraksi Mol, dan Persen () Massa !! SIfat Koligatif Larutan
Molalitas, disebut pula sebagai konsentrasi molal, adalah ukuran konsentrasi dari suatu zat terlarut di dalam suatu larutan dalam hal jumlah zat dalam sejumlah massa tertentu dari pelarut.Hal ini berbeda dengan definisi molaritas yang berdasarkan pada volume tertentu larutan.. Satuan yang umum digunakan untuk molalitas dalam kimia adalah mol/kg.Suatu larutan dengan konsentrasi 1 mol/kg juga.

Hitunglah Kemolalan Larutan Cuka Yang Mengandung 24 Massa Ch3cooh Belajar di Rumah
Hitung molalitas larutan cuka yang mengandung 24% massa CH 3 COOH . (Ar H = 1, C = 12,dan O= 16) SD. Menghitung M r CH 3 COOH . Menghitung massa air. Jika diasumsikan massa larutan 100 gram, maka: Sisanya adalah massa air yaitu 100 gram - 24 gram adalah 76 gram atau 0,076 kg.

Contoh Soal Molalitas Homecare24
Cara Menghitung Molalitas Larutan. Molalitas digunakan untuk menyatakan konsentrasi larutan ketika Anda melakukan eksperimen yang melibatkan perubahan suhu atau bekerja dengan sifat koligatif. Perhatikan bahwa dengan larutan berair pada suhu kamar, kerapatan air kira-kira 1 kg/L, sehingga M dan m hampir sama. Hitung Molalitas: mol zat terlarut.

Berapa massa NaOH padat yang harus ditambahkan ke dalam 100 ml larutan CH3COOH 0,3 M (Ka CH3COOH
Contoh soal: gram terlarut * (1/massa molar terlarut) = 3,4 g * (1 mol / 158 g) = 0,0215 mol. 5. Bagilah jumlah mol dengan banyaknya liter. Karena kamu sudah memiliki jumlah mol, kamu bisa membaginya dengan banyaknya liter larutan untuk mencari molaritas. Contoh soal: molaritas = mol terlarut / liter larutan = 0,0215 mol / 5,2 L = 0,004134615. 6.

Suatu larutan cuka makan mengandung 6 asam asetat. Ji...
Jadi, molaritas dari larutan urea adalah 0,2 Molar atau 0,2 mol/liter. Itu dia penjelasan mengenai rumus molaritas dan molalitas suatu larutan dalam Kimia. Masih sering merasa kesulitan belajar materi dari sekolah. Langganan paket belajar Zenius aja yuk, lewat penjelasan dari tutor yang asyik dan ilustrasi yang menarik bikin belajar nggak.

Hitunglah molalitas dan fraksi mol larutan NaOH dalam air yang kadarnya 40 (Mr NaOH = 40
Hasil pencarian yang cocok: Hitunglah kemolalan larutan cuka yang mengandung 24% massa CH3COOH. ( Ar H= 1 ; C = 12; O = 16 ) - 6434901.. Top 3: Hitung molalitas larutan cuka yang mengandung 24%. Pengarang: roboguru.ruangguru.com - Peringkat 168. Ringkasan: Molalitas menyatakan jumlah mol zat terlarut dalam 1000 gram (1 kg) pelarut.

Hitunglah molalitas dan fraksi mol larutan NaOH dalam air yang kadarnya 40 (Mr NaOH = 40
Satuan Konsentrasi Larutan. Hitung kemolalan larutan cuka yang mengandung 24% massa CH3COOH. (Ar H = 1,C = 12, dan O = 16) Satuan Konsentrasi Larutan. Sifat Koligatif Larutan. Kimia Fisik dan Analisis. Kimia.

Seorang siswa melakukan percobaan titrasi untuk menghitun...
Contoh soal molalitas suatu larutan 20% berat C2H5OH (Mr = 46 g/mol) adalah.. Cara mengerjakan molalitas: C2H5OH 20% artinya 20 gram. C2H5OH dalam 80 gram air. m = massa x 1.000 = 20 x 1.000 = 5,4. Mr P 46 80. Jadi, kemolalan larutan 20% berat C2H5OH adalah 5,4 m. Selamat belajar contoh soal molalitas, detikers!

Hitunglah Kemolalan Larutan Cuka Yang Mengandung 24 Massa Ch3cooh Belajar di Rumah
Jadi, kemolalan larutan cuka yang mengandung 24% massa CH3COOH adalah 5,26 mol kg−1. Kemolalan menyatakan jumlah mol zat terlarut dalam 1 kg pelarut (pelarut, bukan larutan). Kemolalan dinyatakan dengan lambang m dan satuannya adalah mol kg−1. Misal massa larutan % massa CH3COOH 24% massa zat terlarut massa pelarut = = = = = = = 100 g massa.

Ph Larutan Yang Mengandung 6 Gram CH3COOH (Mr=60) Dan 0,1 Mol CH3COONa (Ka=105) Adalah… Blog
Most popular Hyatt Place Glendale/Los Angeles $201 per night. Most popular #2 Embassy Suites Los Angeles - Glendale $223 per night. Best value Brand Plaza Hotel $116 per night. Best value #2 Glendale Express Hotel Los Angeles $131 per night.

Menghitung Molalitas Larutan Jika Diketahui Molaritas dan Kerapatan Larutannya YouTube
Hitung molalitas larutan cuka yang mengandung 24% massa CH3COOH. (Ar H = 1, C = 12, dan O = 16) Satuan Konsentrasi Larutan. Halo Google di sini ada soal Diketahui suatu larutan cuka yang mengandung 24% massa CH3COOH kemudian jam ditanya berapa molalitas larutan cuka Oke sebelum kita masuk ke konsep Desa perlu diketahui di sini ada kata kunci.

Hitunglah Kemolalan Larutan Cuka Yang Mengandung 24 Massa Ch3cooh Belajar di Rumah
1. hitung kemolalan larutan cuka yang mengandung 24% massa CH3COOH ; 2. Hitunglah kemolalan larutan cuka yg mengandung 24% massa ch3cooh! 3. Hitunglah kemolalan larutan cuka yang mengandung 24% massa ch3cooh ! (mr ch3cooh 60 dan mr air 18) 4. Hitung kemolalan larutan cuka yang mengandung 24 % massa CH3COOH jika Ar H = 1 ; C = 12 ; O = 16; 5.

Contoh Soal Fraksi Mol Dan Pembahasannya
Hitung molaritas larutan natrium sulfat tersebut. Larutan: Rumus molekul natrium sulfat yaitu Na 2 SO 4. Rumus molekul air adalah H 2 O. Massa molekul natrium sulfat dihitung dengan: M=23×2+32+16×4=142. Artinya, jumlah mol natrium sulfat dalam soal yang diberikan dihitung dengan: n = 15/142 = 0,106

Menghitung Molalitas Bab Sifat Koligatif Larutan YouTube
Jadi, massa NaCl yang harus dilarutkan pada 500 gram air untuk menghasilkan larutan 0,15 m adalah 4,38 gram. Soal 8. 8. Berapakah molalitas larutan yang mengandung 4 gr NaOH (Ar Na = 23 gr/mol, Ar O = 16 g/mol, dan Ar H = 1 gr/mol) terlarut dalam 250 gr air? Penyelesaian: Diketahui: massa NaOH = 4 gr. Ar Na = 23 gr/mol. Ar O = 16 g/mol. Ar H.

(PDF) Perhitungan Molaritas Dan Molalitas Larutan Dari DOKUMEN.TIPS
Hai CoFriends, yuk latihan soal ini:Hitung molalitas larutan cuka yang mengandung 24% massa CH3COOH. (Ar H = 1, C = 12, dan O = 16) Topik atau Materi: Satuan.
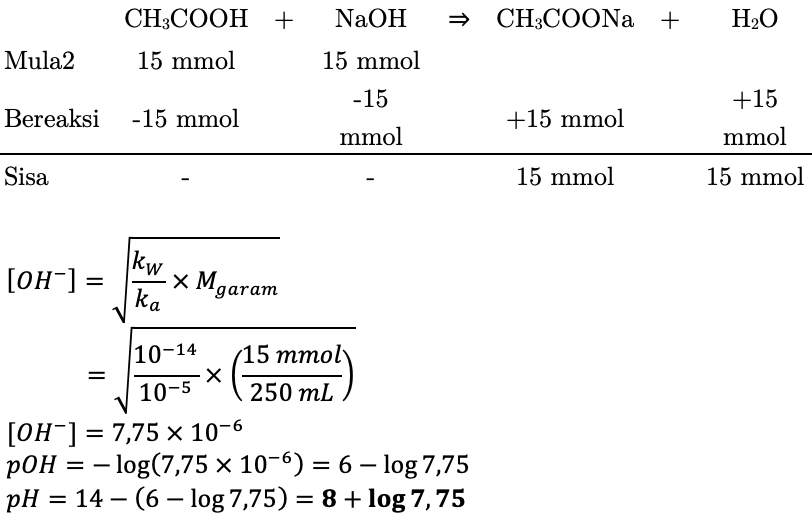
Larutan CH3COOH 0,15 M yang volumenya 100 mL dicampur dengan 150 mL larutan NaOH 0,1 M Mas Soal
Ingat, rumus molaritas pencampuran adalah: Maka, konsentrasi larutan setelah dicampurkan adalah: M campuran = (100 x 0,1) + (150 x 0,2) / (100 + 150) = 40 / 250. = 0,16 M. Quipperian, itu dia pembahasan mengenai rumus molaritas beserta contoh soal dan pembahasannya. Agar semakin paham dan mahir dalam menggunakan rumus molaritas, cobalah untuk.