
Foto Hukum Faraday I dan II tentang Elektrolisis Halaman 1
Pengertian dan Bunyi hukum Faraday 1 dan 2☑️ Rumus (persamaan), Contoh Soal dan pembahasan hukum Faraday 1 dan 2 lengkap☑️ Seorang ilmuwan yang berasal dari Inggris bernama Michael Faraday menemukan sebuah hukum yang digunakan dalam ilmu kimia dinamakan Hukum Faraday. Hubungan antara penggunaan muatan listrik dan hasil massa zat dalam electrode dijelaskan melalui hukum ini.
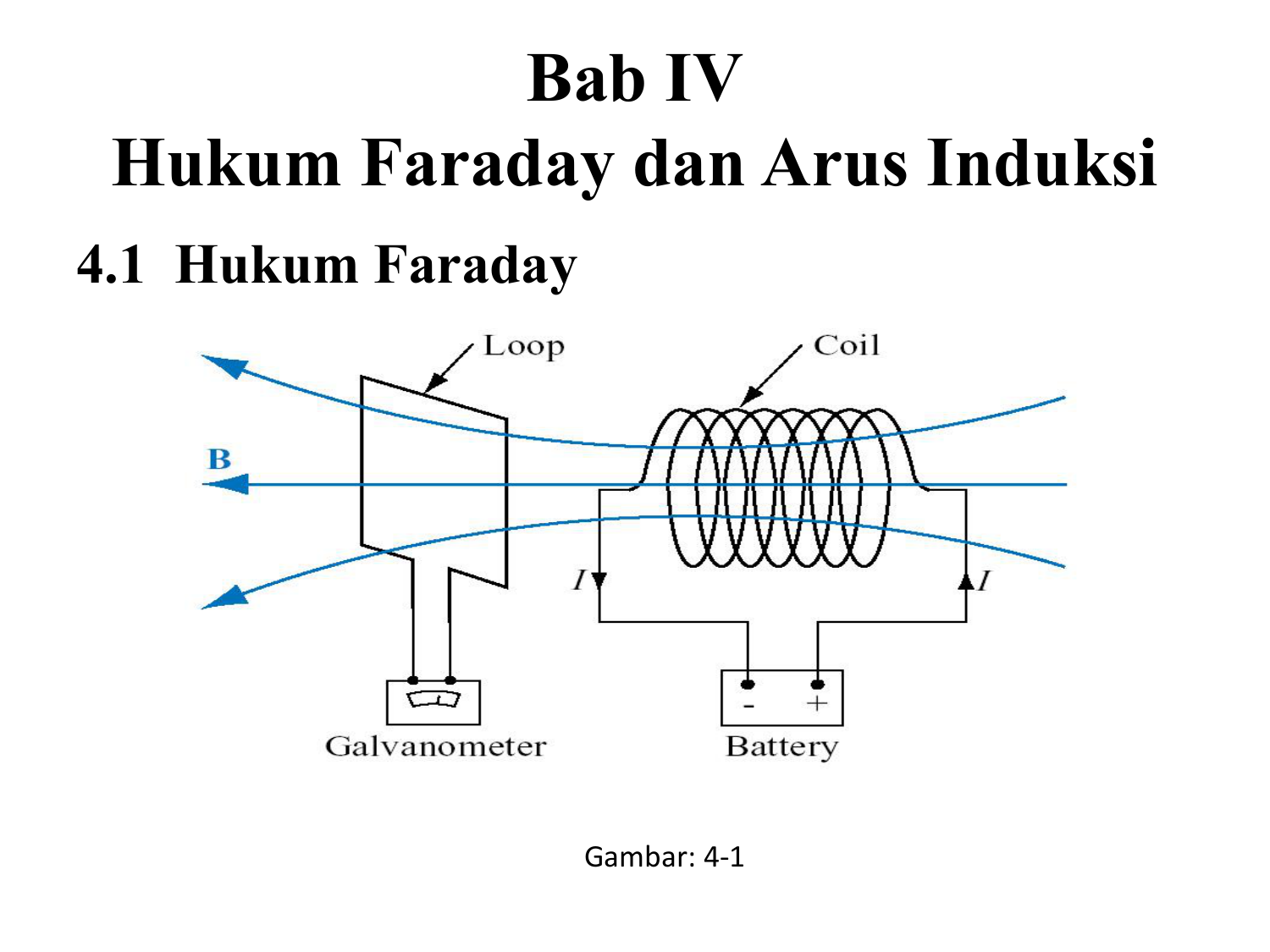
Hukum Faraday dan Arus Induksi
Jadi, Hukum Faraday 1 itu merupakan massa zat yang dihasilkan pada suatu electrode selama proses elektrolisis berbanding lurus dengan muatan listrik yang digunakan. Kita sudah mengetahui bahwa massa zat (w) yang dihasilkan pada elektrode berbanding lurus dengan jumlah molelektron.. Perhatikan gambar di atas, terlihat bahwa jika jumlah.
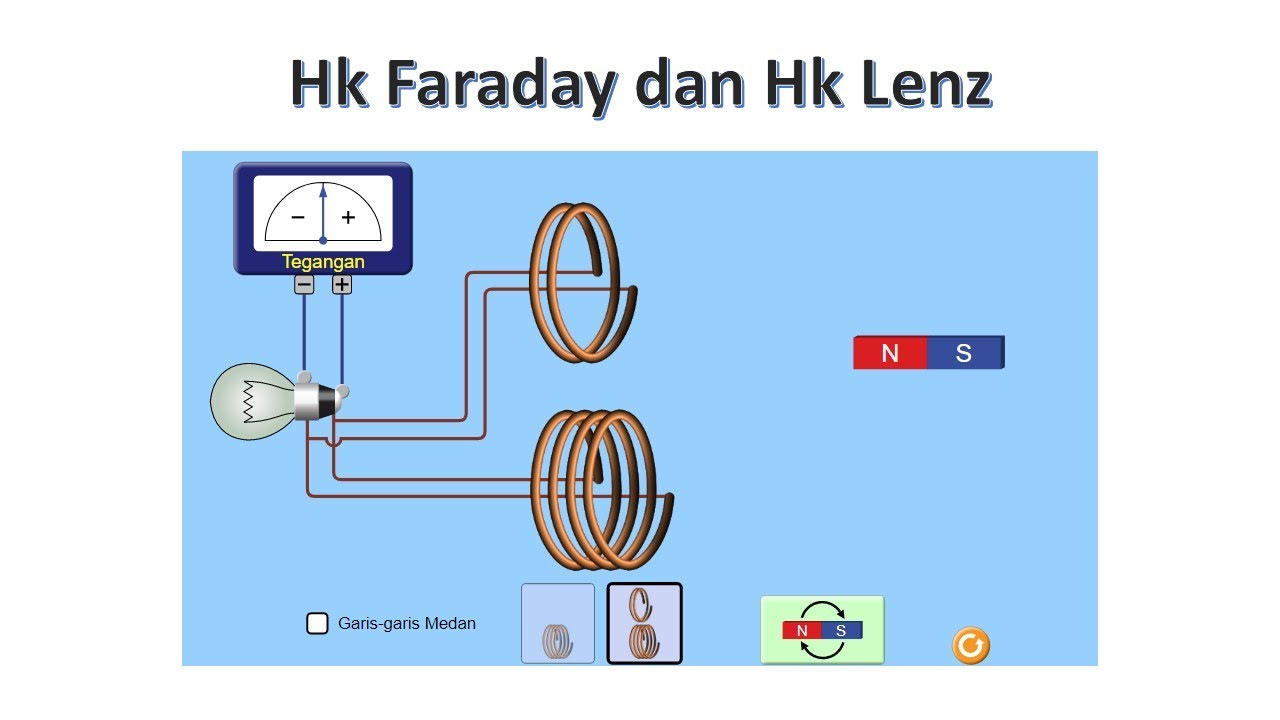
Hukum Faraday dan Hukum Lenz YouTube
Bunyi hukum Faraday 1 yaitu: "Massa zat yang diperoleh pada elektroda saat proses elektrolisis, sebanding dengan jumlah muatan listrik yang mengalir". Dari bunyi di atas, kita dapat melihat bahwa massa produk (W) yang diendapkan pada elektroda akan semakin banyak selama beriringan dengan peningkatan muatan listrik (Q) yang dipakai, maka W ≈ Q.

Definisi Hukum Faraday
Contoh Soal Hukum Faraday. 1. Soal 1. Sumber dari gaya gerak listrik adalah.. a. magnet yang bergerak di sekitar kumparan. b. muatan listrik yang bergerak di sekitar kumparan. c. magnet yang diam di sekitar kumparan. d. dua buah magnet diam di sekitar kumparan. e. interaksi kutub-kutub magnet di sekitar kumparan.
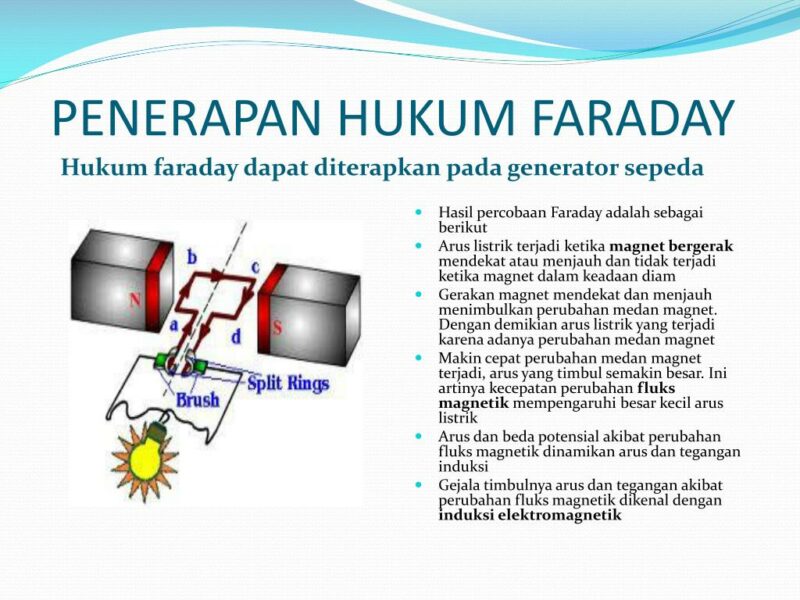
√ Hukum Faraday Pengertian, Bunyi, Rumus dan Contoh Soal
Judul gambar diatas adalah "Hukum Faraday", semoga dengan tampilan gambar yang lebih besar dapat dilihat lebih jelas dan dapat dipahami. Untuk melihat gambar-gambar lain dari artikel Hukum Faraday, anda dapat memilih gambar pada bagian dibawah. Dan untuk kembali ke halaman utama website "Fisika Zone" atau kembali ke artikel "Hukum Faraday" anda.

Induksi Hukum Faraday (Fisika SBMPTN, UN, SMA) YouTube
Pengertian Hukum Faraday. Hukum Faraday adalah hukum yang menjelaskan tentang hubungan antara jumlah listrik yang digunakan dengan massa zat yang dihasilkan, baik di katode maupun anode pada proses elektrolisis. Hukum ini ditemukan oleh Michael Faraday, seorang ahli kimia dan fisika asal Inggris pada tahun 1834.

Hukum Faraday dan Hukum Lens Rocking Mama For Smart And Powerful Moms
Hukum Faraday tentang induksi elektromagnetik terdiri dari beberapa prinsip utama yang menjelaskan hubungan antara fluks magnetik dan arus listrik yang terinduksi dalam suatu kawat atau konduktor. Prinsip-prinsip ini sangat penting dalam pemahaman kita tentang induksi elektromagnetik dan penerapannya dalam teknologi modern. 1. Hukum Faraday I
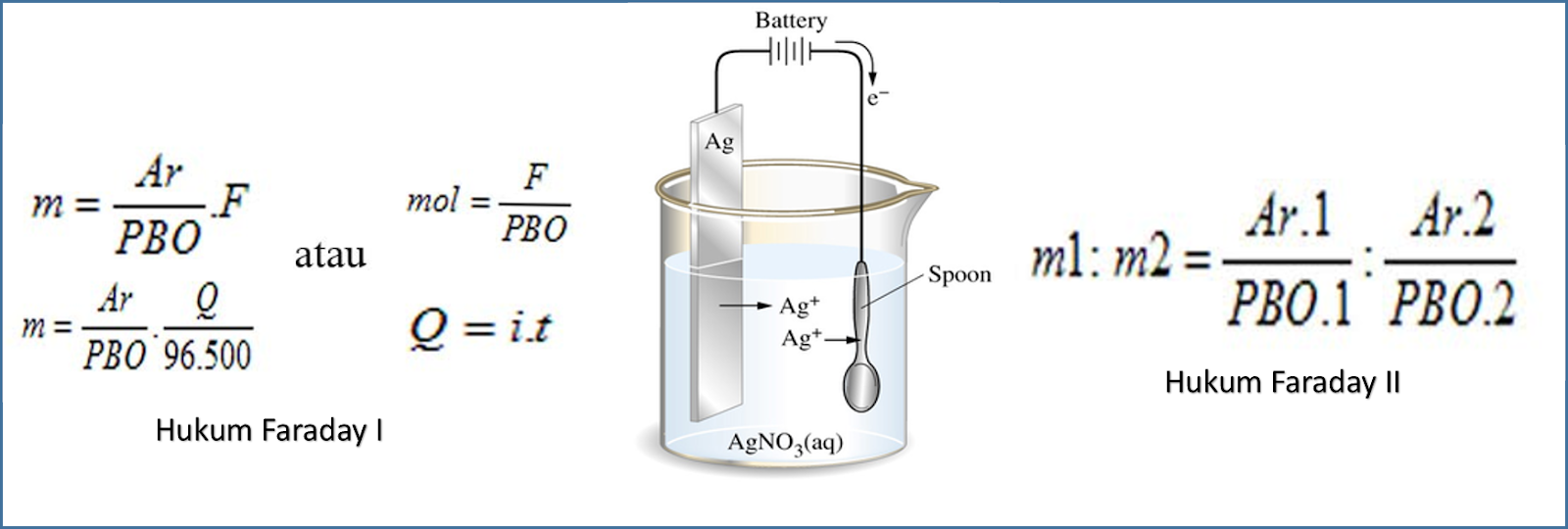
Hukum Faraday Pojok Kimia
Kita menamakan ini sebuah arus induksi ( induced current) dan ggl yang diperlukan untuk menyebabkan arus ini dinamakan sebuah ggl induksi ( induced emf ). Gambar 1: Perangkat Percobaan untuk pengamatan gejala arus induksi. Dalam gambar 1c kita mengganti magnet dengan sebuah kumparan kedua yang disambungkan ke sebuah aki.
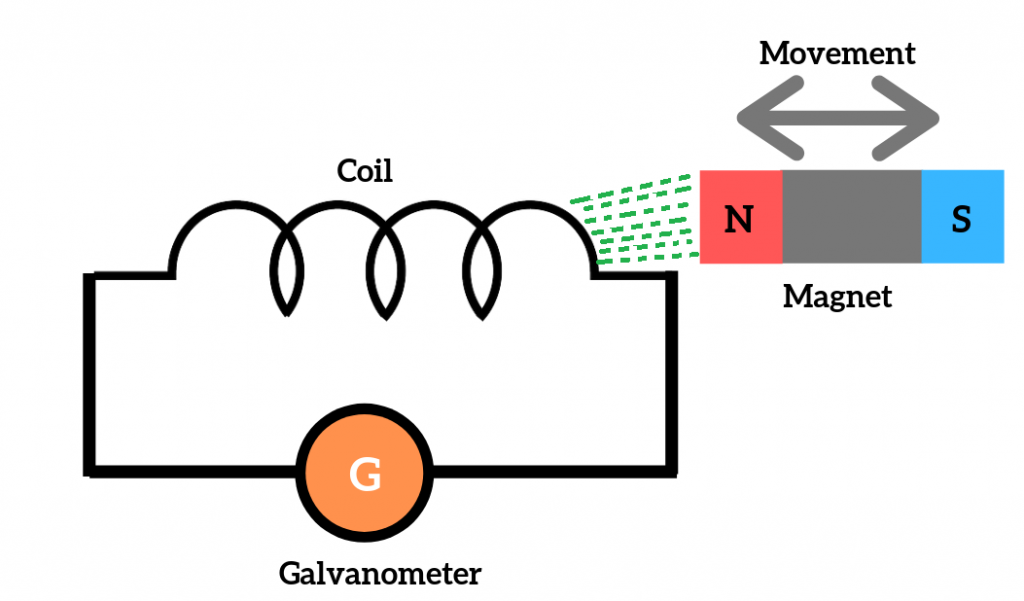
Hukum Faraday Mengenai Induksi
Dickson Kho Teori Elektronika. Pengertian Hukum Faraday dan Bunyi Hukum Faraday - Hukum Faraday adalah Hukum dasar Elektromagnetisme yang menjelaskan bagaimana arus listrik menghasilkan medan magnet dan sebaliknya bagaimana medan magnet dapat menghasilkan arus listrik pada sebuah konduktor. Hukum Faraday inilah yang kemudian menjadi dasar.
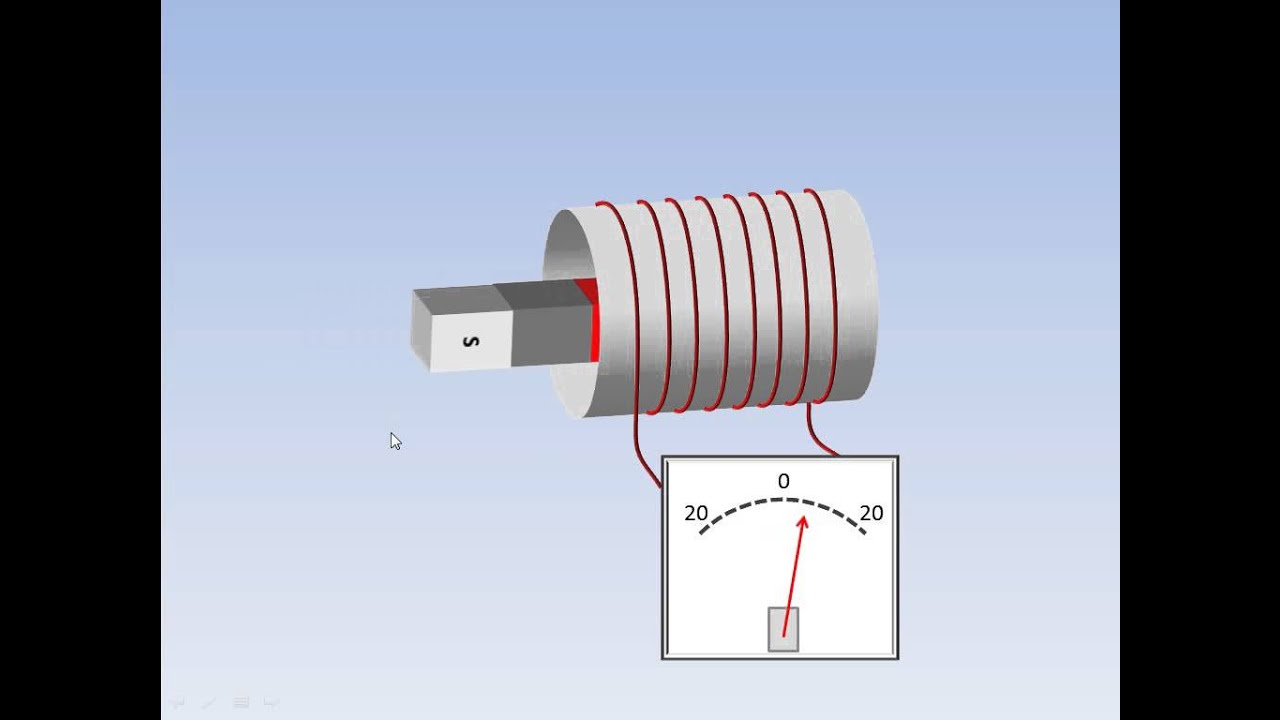
Animasi induksi hukum Faraday YouTube
Contoh soal hukum Faraday nomor 6. Kawat PQ yang panjangnya 25 cm digeser ke kanan dengan kecepatan 4 m/s seperti pada gambar berikut. Contoh soal hukum Faraday nomor 6. Jika induksi magnet 0,2 T, besar GGL dan arah arus pada kawat PQ masing-masing adalah. A. 0,2 V dari P ke Q B. 0,2 V dari Q ke P C. 2,5 V dari P ke Q D. 2,5 V dari Q ke P

HUKUM FARADAY 1 & 2Contoh soal HUKUM FARADAY UTBKSBMPTN YouTube
Ag + (aq) + e - → Ag (s). Dari reaski di atas dapat dikatakan bahwa untuk menghasilkan 1 mol logam Ag, diperlukan 1 mol elektron. Jumlah listrik yang dialirkan ke dalam sel elektrolisis untuk mendapatkan 1 mol elektron dinamakan hukum 1 faraday.. Berdasarkan percobaan diperoleh bahwa 1 mol elektron mengandung muatan listrik sebesar 96500 Coulomb atau 1 mol elektron = 1 Faraday = 96500 Coulomb

Elektrolisis (Reaksi Elektrolisis dan Hukum Faraday) Kimia XII YouTube
Hukum Lenz merupakan pelengkap dari Hukum Faraday. Dikutip dari buku Fisika Dasar (2017) oleh Mikrajuddin Abdullah, penjelasan di dalam Hukum induksi Faraday hanya mengungkapkan besarnya gaya gerak listrik induksi.. Magnet yang digerakkan dalam kumparan menghasilkan arah yang bisa dilihat melalui gambar berikut: Sederhananya, induksi magnet.
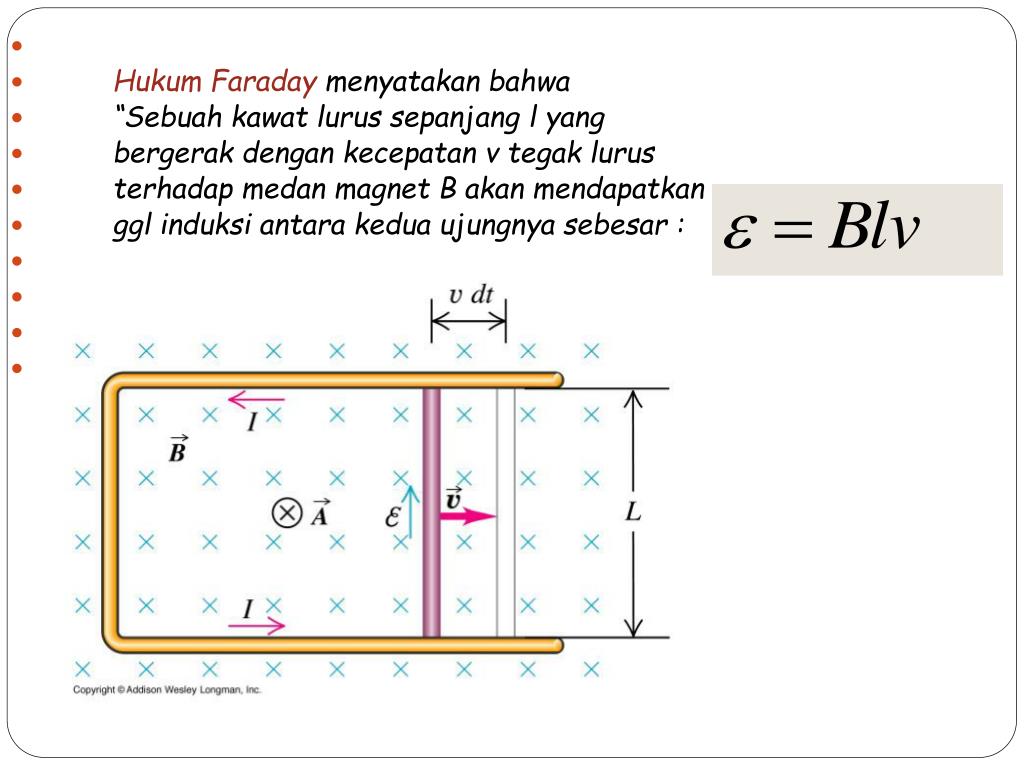
PPT HUKUM INDUKSI FARADAY PowerPoint Presentation, free download ID5738336
Play with a bar magnet and coils to learn about Faraday's law. Move a bar magnet near one or two coils to make a light bulb glow. View the magnetic field lines. A meter shows the direction and magnitude of the current. View the magnetic field lines or use a meter to show the direction and magnitude of the current. You can also play with electromagnets, generators and transformers!

Hukum Faraday Definisi, Kegunaan dan Aplikasi Root of Science
Gambar di bawah menunjukkan corak medan magnet yang terbentuk di kutub utara dan kutub selatan magnet. Corak Medan Magnet.. Hukum Faraday. Michael Faraday telah menemui perkaitan penting antara elektrik dan magnet iaitu aruhan elektromagnet yang ditemui pada tahun 1831. Michael Faraday telah mencipta satu hukum yang dipanggil Hukum Faraday

PPT HUKUM INDUKSI FARADAY PowerPoint Presentation, free download ID5738336
Bunyi Hukum Induksi Faraday dan Pengaplikasiannya. by Mizzart Al Fatih. April 27, 2022. Kali ini, kita bakal mempelajari bunyi hukum Faraday yang terdapat di dalam hukum induksi Faraday. Selain itu, kita juga akan melihat pengaplikasiannya di dalam kehidupan sehari-hari. Sewaktu masih kecil dulu, gue tinggal di sebuah daerah yang sering banget.
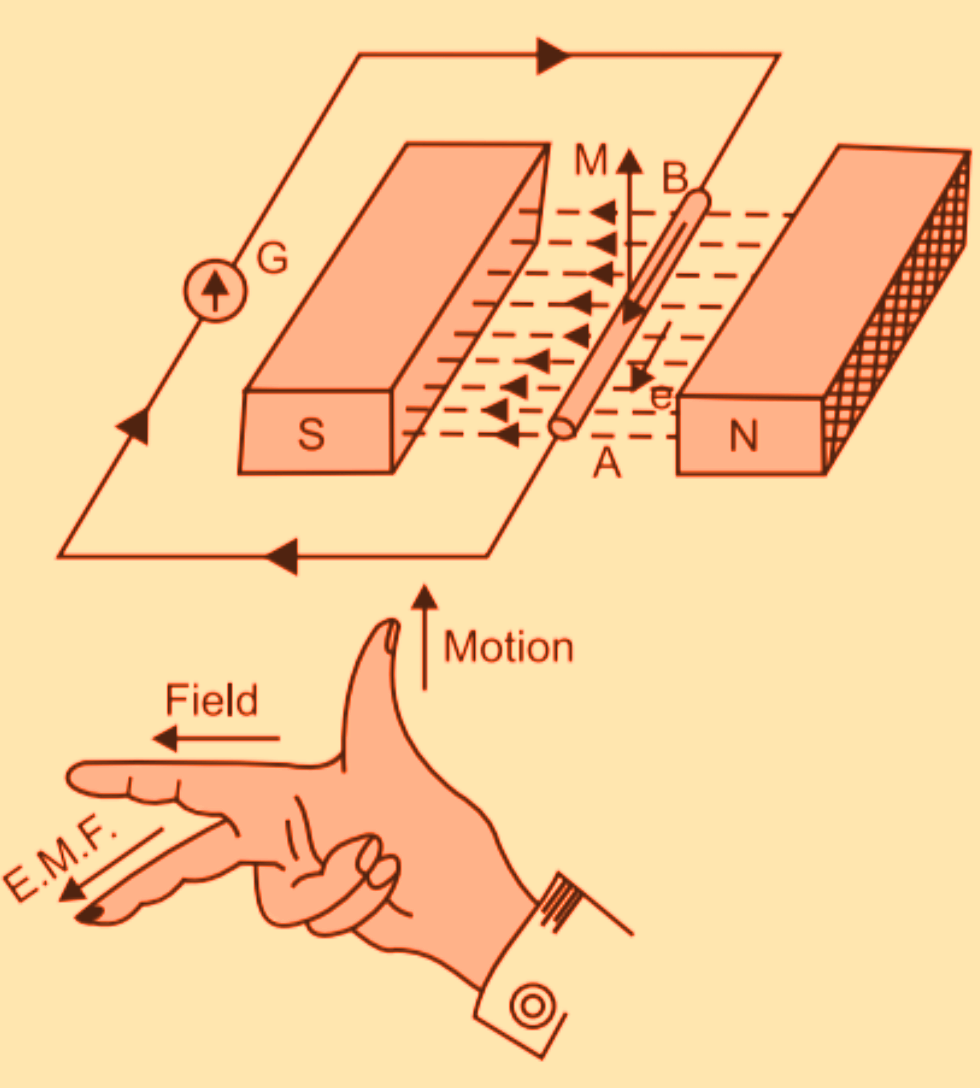
faraday law of induction
Bunyi hukum Faraday II: "Massa zat yang dilepaskan pada elektrolisis berbanding lurus dengan massa ekuivalen zat itu" Berdasarkan bunyi hukum Faraday 2 tersebut, maka rumusnya adalah: Keterangan: ME = massa ekivalen. x = jumlah elektron yang diterima atau dilepaskan. Jika rumus hukum Faraday 1 dan 2 ini digabungkan, maka akan diperoleh.