
PPT POTENSIOMETRI PowerPoint Presentation, free download ID3473552
Sel volta anoda bermuatan negatif, dan sel volta katoda bermuatan positif. Anoda merupakan elektroda yang terjadi saat reaksi oksidasi, terjadinya reaksi reduksi elektroda disebut dengan katoda. Elektroda adalah benda yang digunakan sebagai penghantar arus listrik (konduktor). Tembaga, seng, timah hitam, besi, nikel perak, platinum, emas.

Elektrokimia Pengertian, Jenis, Aplikasi dan Contohnya
positif dan elektroda negatif. Hal ini d isebabkan k arena elektroda tersebut akan dialiri oleh ar us. listrik sebagai sumber energi dalam pertukaran elektron. Konsep elektrokimia didasari oleh.

Tab Baterai Lithium Aluminium Nikel Untuk Koneksi Elektroda Negatif Positif
Elektroda positif, juga dikenal sebagai anoda, akan terhubung dengan kutub positif sumber arus, sedangkan elektroda negatif, atau disebut katoda, terhubung dengan kutub negatif. Inilah saatnya reaksi misterius dimulai! Setelah arus listrik dialirkan melalui larutan, molekul CuSO4 akan terpecah menjadi ion-ion tembaga (Cu²⁺) dan sulfat.

ELEKTRODA POSITIF GUITAR SOLO STUDIO GHEGURIT YouTube
Elektroda. Komponen sel elektrolisis yang pertama adalah elektroda. Elektroda merupakan konduktor listrik berupa logam yang terdiri dari dua bagian, yaitu elektroda positif dan negatif. Elektroda positif disebut dengan anoda, sedangkan elektroda negatif disebut dengan katoda. Baca juga: Sel Elektrokimia: Sel Volta dan Sel Elektrolisis.
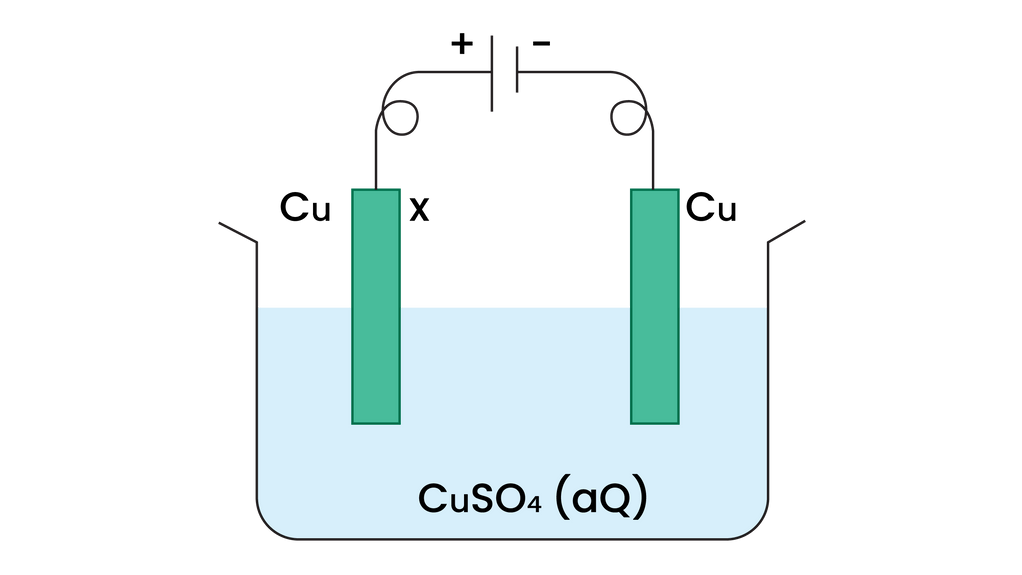
Pada elektrolisis seperti gambar di bawah ini, per...
Ion positif adalah atom dengan satu elektron terlalu sedikit. Ketika mereka mencapai katoda, mereka bergabung dengan elektron dan kehilangan muatan positifnya. Pada saat yang sama, ion bermuatan negatif bergerak ke elektroda positif, yang disebut anoda.
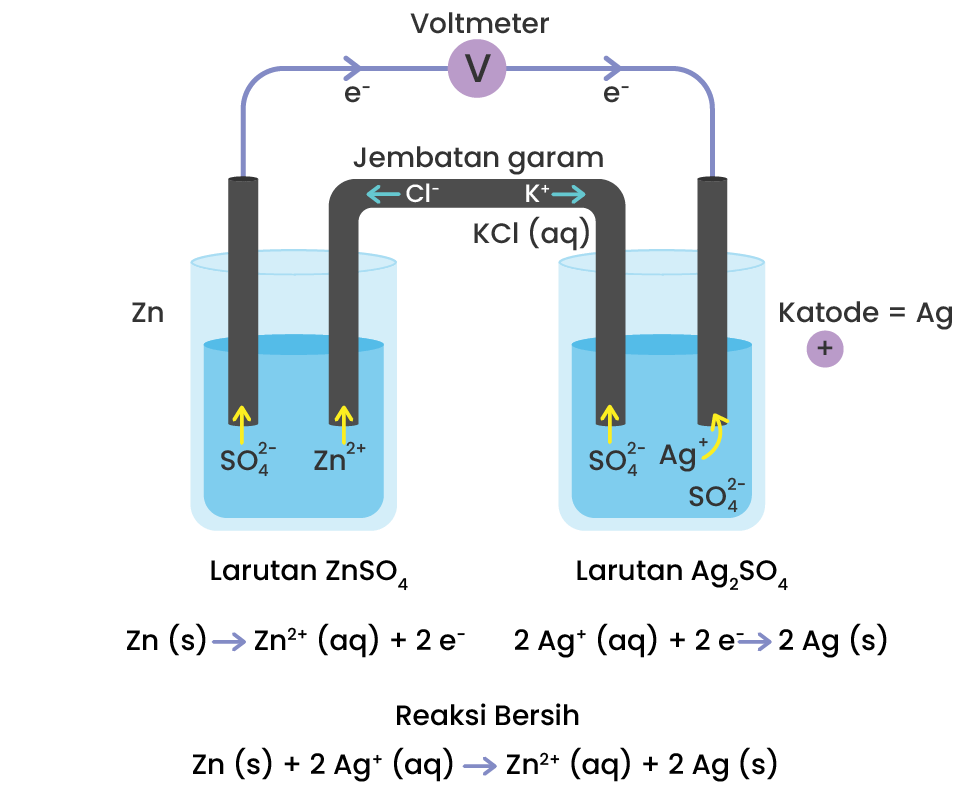
Gambarlah rangkaian alat pada sel volta Zn dan Ag!
1. Hubungan dengan elektroda. Anoda berhubungan dengan elektroda dimana oksidasi (kehilangan elektron) terjadi. Katoda berhubungan dengan elektroda dimana reduksi (penguatan electron) terjadi. 3. Sel elektrolitik. Anoda bertindak sebagai terminal positif. Katoda memegang polaritas negatif. 3.

firstwisnu media Sel Volta Si Pengubah Reaksi Kimia Menjadi Energi Listrik, Kece Deh!
Sel elektrolisis tersusun dari elektroda-elektroda yang dicelupkan dalam suatu kompartemen yang berisi larutan elektrolit. Pada sel elektrolisis terdapat 2 buah elektroda yang dihubungkan pada sumber listrik yaitu anoda di kutub positif dan katoda di kutub negatif. Anoda pada sel elektrolisis merupakan tempat terjadinya reaksi oksidasi.

Pada elektrolisis larutan CuSO4 seperti terlihat pada gam...
Pergerakan elektron menuju katoda (yang membawa muatan negatif) berarti arus berangkat dari katoda (muatan positif). Jadi, untuk sel galvanik Daniell, elektroda tembaga adalah katoda dan terminal positif. Jika arus dibalik dalam sel Daniell, sel elektrolitik dihasilkan, dan elektroda tembaga tetap menjadi terminal positif, namun menjadi anoda.
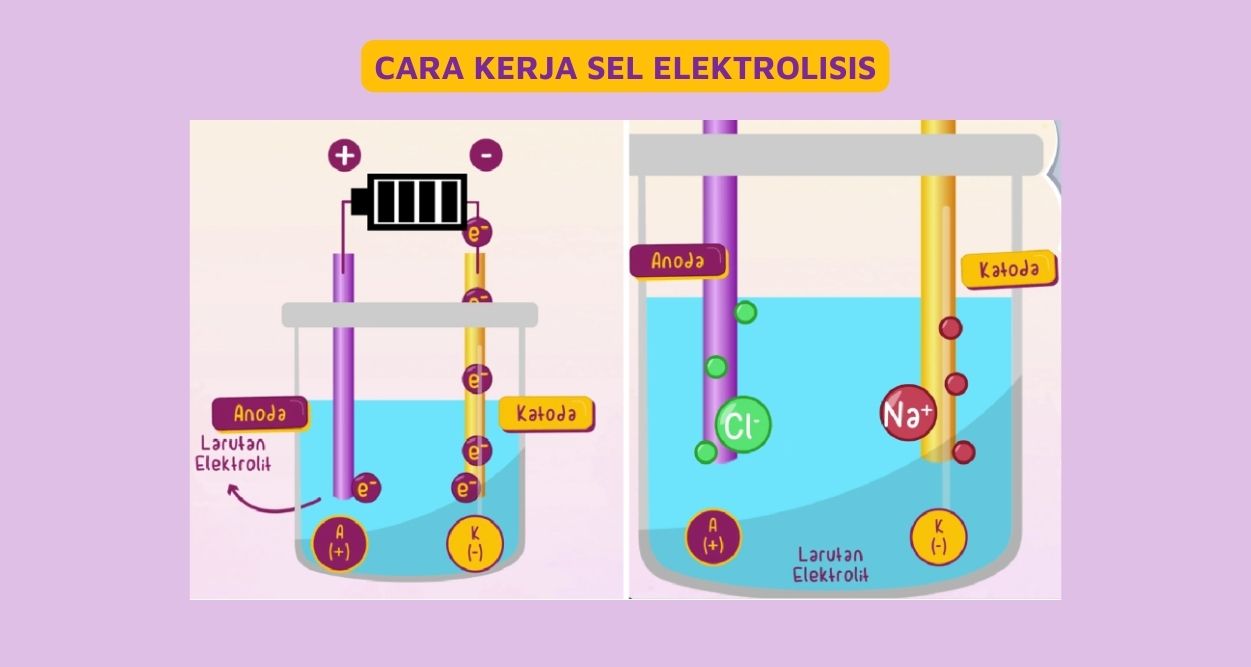
Sel Elektrolisis Pengertian, Reaksi, dan Contoh Soal
Katoda (elektroda positif) Komponen ini adalah elektrode tembaga (Cu) yang bertindak sebagai tempat terjadinya reaksi reduksi. Kalau bagian-bagian sel volta tersebut diperhatikan, elo bisa melihat kalau prinsip dasar sel volta ini dapat dilihat secara langsung pada baterai yang kita gunakan sehari-hari, yaitu pada keberadaan anoda dan katoda.
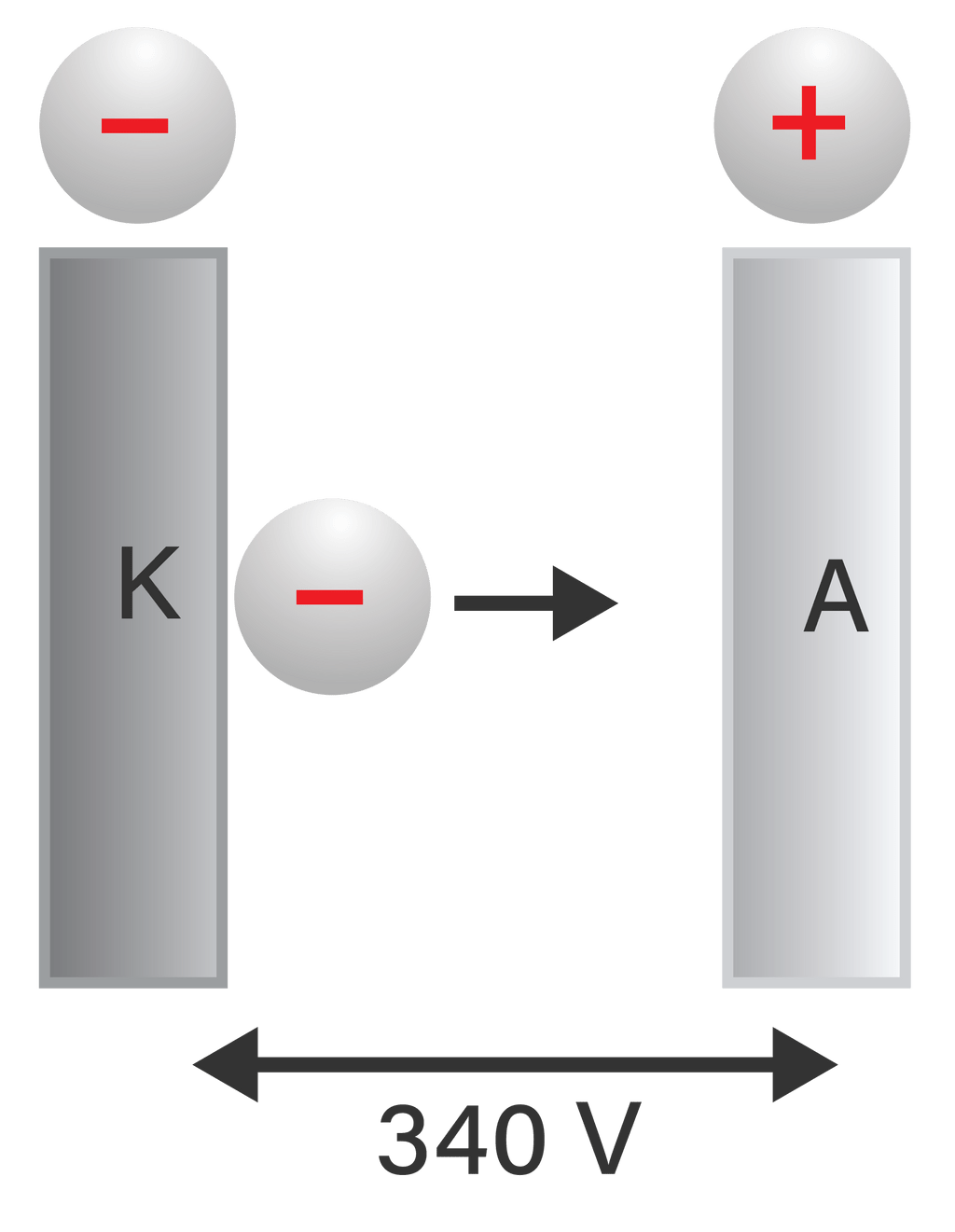
Dalam suatu tabung hampa yang mempunyai elektroda
Sel elektrolisis mempunyai dua elektroda bersifat negatif dan positif. Cara kerja sel elektrolisis yaitu dengan menghubungkan sumber arah dari kutub negatif ke katode dan kutub positif ke anode. Kemudian terjadi over potential yang mendorong reaksi reduksi dan oksidasi non-spontan dapat berjalan. Sehingga elektron dapat mengalir dari katode ke.
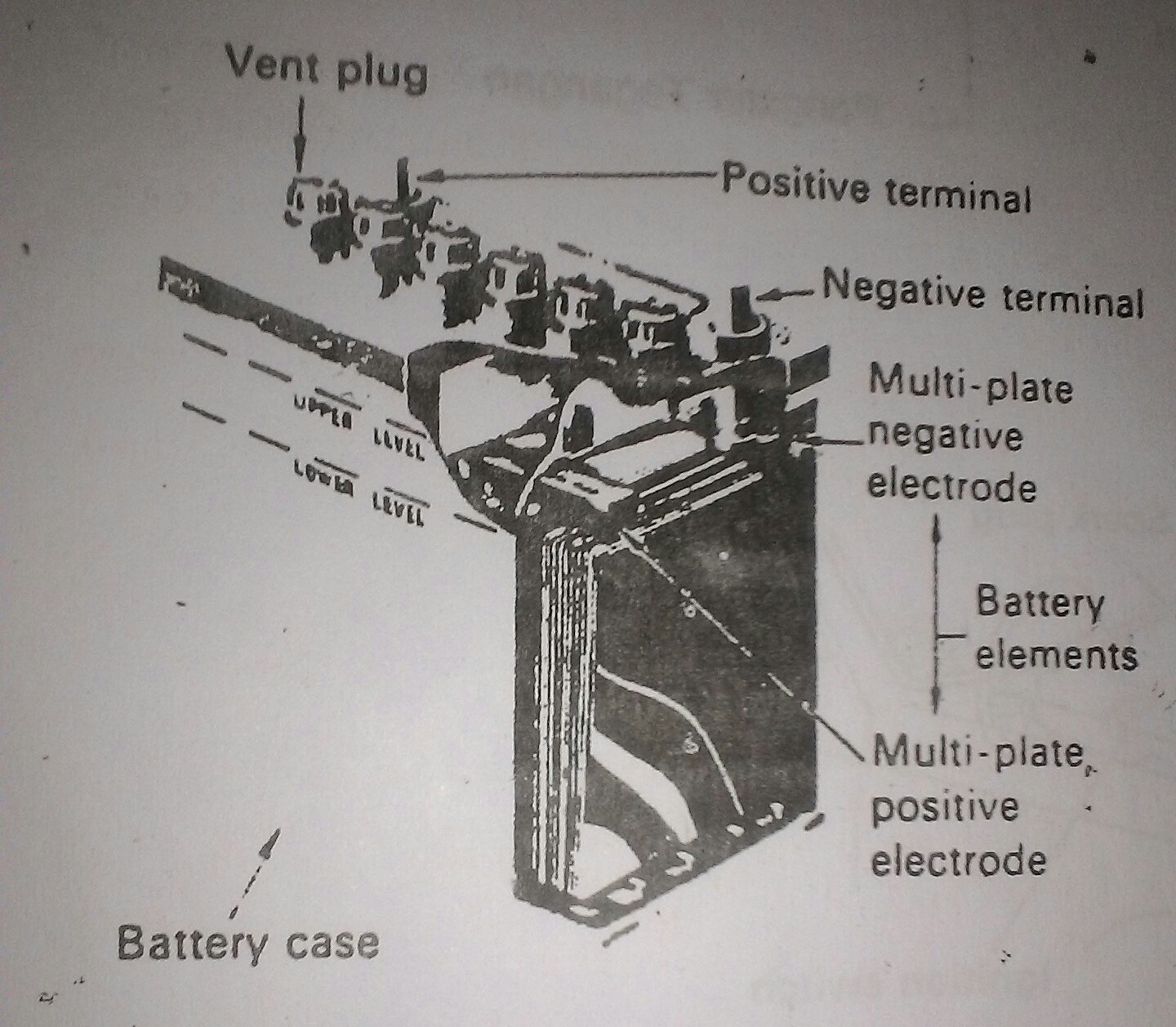
otomotif PENGERTIAN BATERAI/AKI DAN KOMPONEN PENYUSUN ,REAKSI KIMIA DALAM BATERAI
Dari Wikipedia bahasa Indonesia, ensiklopedia bebas. Elektrode adalah penghantar listrik yang terhubung dengan larutan elektrolit dari sebuah rangkaian listrik. Dalam suatu sel elektrokimia, elektrode dapat berperan sebagai anode ketika proses oksidasi maupun katode ketika proses redoks. Peran elektrode sebagai anode dan katode ditentukan oleh.
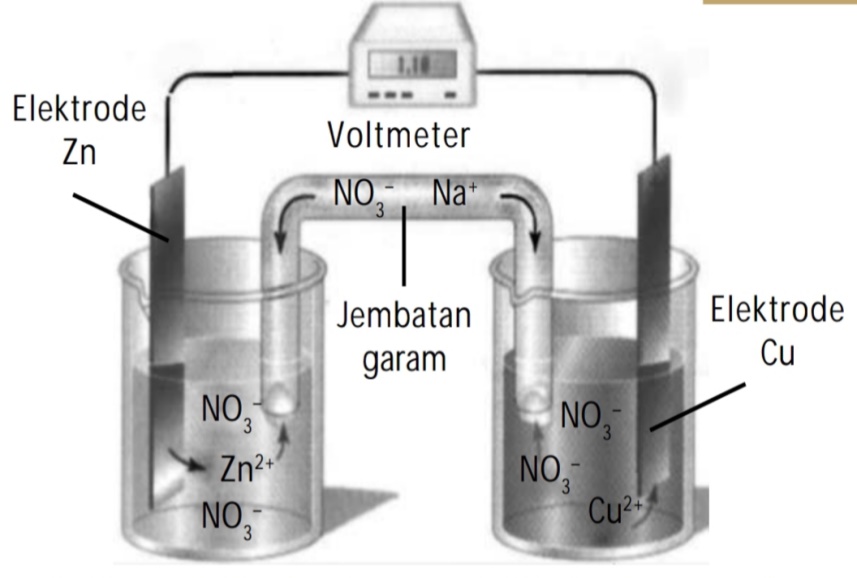
Jelaskan Prinsip Penggunaan Sebuah Bahan Ditaruh Di Suatu Elektroda (Anoda Atau Katoda
Faiprianda Assyari Rahmatullah. 2019. Elektrokimia merupakan ilmu kimia yang mempelajari tentang perpindahan electron yang terjadi pada sebuah media pengantar listrik (elektroda). Elektroda terdiri dari elektroda positif dan elektroda negatif. Hal ini disebabkan karena elektroda tersebut akan dialiri oleh arus listrik sebagai sumber energi.

Tabel Potensial Elektroda
Elektroda Pelat: Umumnya digunakan dalam baterai dan kapasitor, elektroda pelat memiliki bentuk datar dan lebar. Dampak Lingkungan dari Produksi Elektroda. Produksi elektroda memiliki beberapa dampak signifikan terhadap lingkungan, yang sebagian besar berasal dari pertambangan dan pemrosesan bahan yang digunakan untuk membuat elektroda. Berikut.

Tabel Potensial Elektroda
Muatan positif pada elektroda-anoda ditarik oleh muatan negatif pada elektroda-katoda, menciptakan medan listrik yang mendorong ion-ion dalam larutan elektrolit untuk bergerak sesuai dengan arah arus. Arus listrik kemudian mengalir dari elektroda-anoda melalui larutan elektrolit ke elektroda-katoda. 3. Reaksi Redoks di Anoda dan Katoda

Jelaskan Prinsip Penggunaan Sebuah Bahan Ditaruh Di Suatu Elektroda (Anoda Atau Katoda
2. Menghantarkan Arus Listrik. Elektroda berfungsi sebagai penghantar arus listrik dari sumber ke larutan elektrolit atau permukaan benda yang akan direaksikan. Elektroda akan membantu memfasilitasi terjadinya reaksi elektrokimia dengan menghantarkan arus listrik melalui elektrolit. 3. Mengukur Potensial.

PPT DETEKSI RADIOAKTIF PowerPoint Presentation, free download ID3952975
Elektroda positif kemudian dapat diorientasikan sebagai permukaan jam. Menurut konvensi, 0° didefinisikan sebagai horizontal dan ke kiri, gerakan searah jarum jam adalah positif, dan gerakan berlawanan arah jarum jam adalah negatif. Dengan konfigurasi ini, menjadi jelas bahwa I dan aVL berada pada arah umum yang sama, masing-masing 0 ° dan.