
Diketahui entalpi pembentukan senyawa NH4NO3, N2O, dan H2...
14. Beberapa contoh penerapan sifat koligatif larutan dalam kehidupan sehari-hari adalah sebagai berikut. 1. Proses penyerapan air dalam tanah oleh akar tanaman 2. Membasmi lintah dengan menabur garam dapur 3. Pemakaian garam dapur untuk pencairan salju 4. Penambahan etilena glikol pada radiator mobil

Diketahui diagram pembentukan gas SO3 sebagai berikut. 0
LAMPIRAN A. Data Percobaan Dari percobaan praktikum kimia analisis kolorimetri diperoleh data hasil percobaan sebagai berikut : Tabel 1. Data Percobaan Praktikum Kimia Analisis Kolorimetri No Volume Larutan Sampel (mL)/No Volume Larutan Standar (mL)/No V 1 (mL) V 2 (mL) ∆V (mL) 1. Larutan Sampel 1 Larutan FeCl 3 1 15 17 2 2.

Data percobaan pembentukan uap air dari gas hidrogen dan
Berikut ini pembahasan soal pilihan ganda pokok bahasan stoikiometri. Semua ada 70 soal pilihan ganda yang dibagi dalam 3 bagian.. Diketahui data percobaan pembentukan senyawa pirit sebagai berikut. Perbandingan Fe : S adalah. A. 1 : 2 B. 2 : 3 C. 4 : 3. Jika diketahui massa atom relatif H = 1, S = 32, O = 16 dan massa molekul.
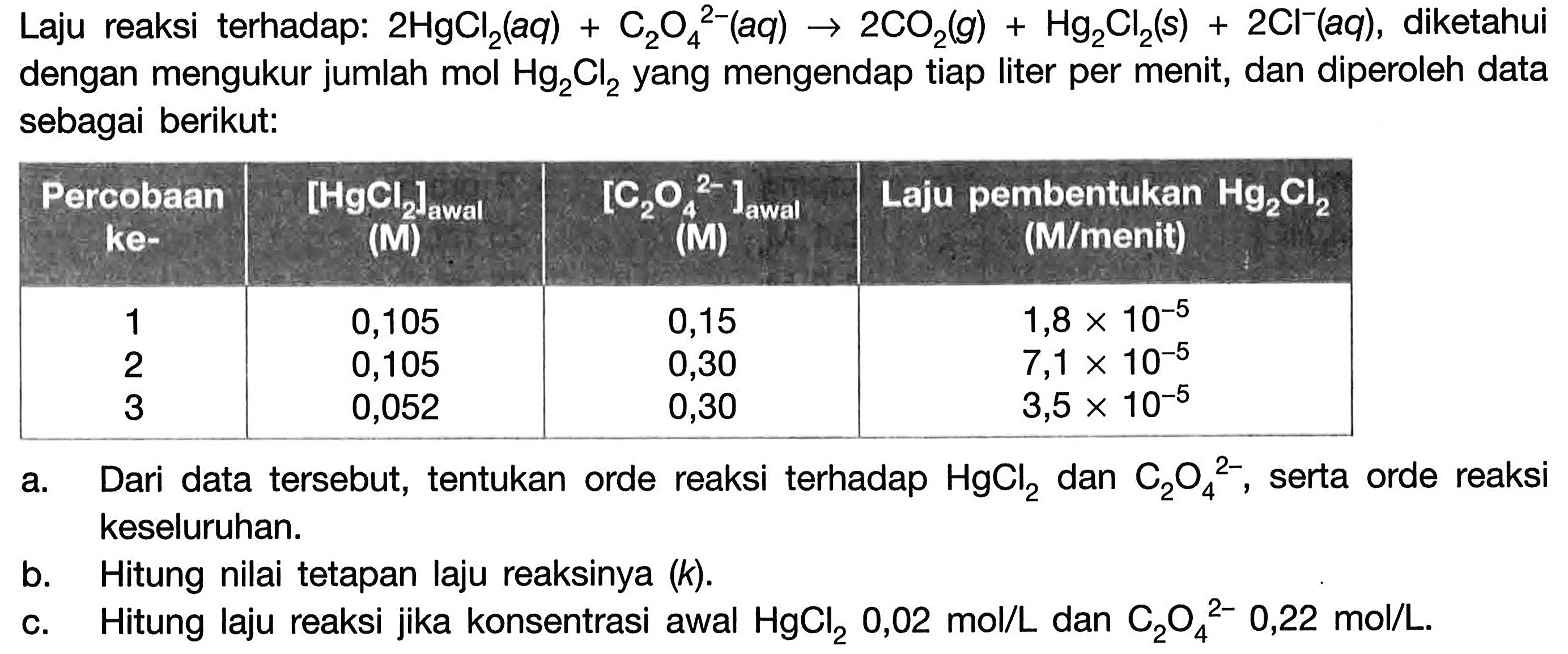
Perhatikan data hasil eksperimen dari reaksi berikut. A(a...
Diketahui data percobaan pembentukan senyawa pirit sebagai berikut. Perbandingan Fe : S adalah. . A. 1 : 2 B. 2 : 3 C. 4 : 3 D. 5 : 8 E. 7 : 8. Diketahui data percobaan pembentukan senyawa pirit. AR. Arky R. 03 Februari 2022 03:00. Pertanyaan. Diketahui data percobaan pembentukan senyawa pirit sebagai berikut. Perbandingan Fe : S adalah.

Diketahui Entalpi Pembentukan Co G Kj Mol H O G Kj My XXX Hot Girl
Hidrokarbon. Dalam bidang kimia, hidrokarbon adalah sebuah senyawa yang terdiri dari unsur atom karbon (C) dan atom hidrogen (H). Seluruh hidrokarbon memiliki rantai karbon dan atom-atom hidrogen yang berikatan dengan rantai tersebut. Istilah tersebut digunakan juga sebagai pengertian dari hidrokarbon alifatik. Sebagai contoh, metana () adalah hidrokarbon dengan satu atom karbon dan empat atom.

PPT MENGENAL PIRIT PowerPoint Presentation, free download ID2136296
Pembahasan. Untuk menentukan perbandingan tetap massa dalam suatu senyawa yang paling mudah adalah mencari massa Fe dan S yang habis bereaksi. Dalam tabel semua percobaan habis bereaksi sehingga dapat dipilih misal percobaan nomor 1 yaitu : Fe : S = 7 gram : 8 gram sehingga perbandingannya adalah 7 : 8 (sudah merupakan bilangan bulat sederhana)

Diketahui data percobaan pembentukan senyawa pirit sebaga...
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Diketahui data percobaan.

Diketahui data titik didih beberapa senyawa berikut. Seny...
20. Diketahui data percobaan pembentukan senyawa pirit sebagai berikut Massa Besi ( Fe) Massa belerang (S) Massa Pirit ( FeS2) 7 gram 8 gram 15 gram 14 gram 16 gram 30 gram 21 gram 24 gram 45 gram Perbandingan Fe S adalah. A. 1 2 B. 2 3 C. 3 D. 5 8 E. 7 8 1. Perbandingan massa magnescium dengan macse okeicon delan

Diketahui data titik didih beberapa senyawa berikut. Seny...
Pembentukan 1 mol NH 3 akan melepaskan kalor sebanyak a kJ. Ingat! Entalpi standar merupakan entalpi untuk pembentukan 1 mol senyawa. Topik: Laju Reaksi. Subtopik : Faktor - faktor yang memengaruhi laju reaksi. Level: HOTS. 10. Seorang siswa melakukan percobaan kinetika kimia dengan mereaksikan sejumlah zat.

Diketahui data entalpi pembentukan standar sebagai beriku...
Reaksi pembentukan amonia setelah setara adalah sebagai berikut: N 2(g) + 3H 2(g) ⇌ 2NH 3(g) Sehingga perbandingan volume gas N 2, H 2 dan NH 3 berturut - turut adalah 1 : 3 : 2. 9. Senyawa oksida logam M x O y dihasilkan dari reaksi antara padatan logam M sebanyak 0,5 mol dengan 0,625 mol gas oksigen. Jika reaksi tersebut menghasilkan 0,25.

Diketahui kalor pembentukan beberapa senyawa sebagai beri...
34. Diketahui data percobaan pembentukan senyawa pirit sebagai berikut. Perbandingan Fe : S adalah. . A. 1 : 2 D. 5 : 8. B. 2 : 3 E. 7 : 8. C. 4 : 3. Massa Besi (Fe) Massa Belerang (S) Massa Pirit (FeS 2) 7 gram 8 gram 15 gram. 14 gram 16 gram 30 gram

Perhatikan Gambar Berikut Senyawa Yang Dihasilkan Dari Reaksi Tersebut Adalah bonus
Pada tabel tersebut perbandingan massa Fe dan massa S dapat diketahui saat kedua unsur tepat habis bereaksi. ︎ percobaan 1 7 gram Fe dengan 8 gram S menghasilkan 15 gram FeS sehingga perbandingannya adalah 7: 8. ︎percobaan 2 14 gram Fe dengan 16 gram S menghasilkan 30 gram FeS sehingga perbandingannya adalah 14 : 16 = 7 : 8 ︎percobaan 3.

Diketahui entalpi pembentukan beberapa senyawa sebagai be...
Diketahui data percobaan pembentukan senyawa pirit sebagai berikut.Massa Besi (Fe) Massa Belerang (S) Massa Pirit (FeS2)7 gram 8 gram 15 gram14 gram 16 gram 30 gram21 gram 24 gram 45 gramPerbandingan Fe:S adalah.. Hukum-Hukum Dasar Kimia.

LENGKAP ‼️ PEMBENTUKAN SENYAWA ION DARI KATION DAN ANION ‼️ KIMIA KELAS 10 YouTube
LAPORAN RESMI PRAKTIKUM ANALISIS SENYAWA KIMIA PERCOBAAN II "PENGUJIAN BORAKS DAN ASAM BORAT DALAM BAHAN PANGAN" Disusun oleh: Nama : Hasna Ulfiani NIM : 12312241028 Prodi : Pendidikan IPA Kelompok : II B Tanggal Praktikum : 28 Mei 2015 LABORATORIUM KIMIA ANALITIK FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA 2015 A. Judul Pengujian Boraks dan Asam Borat dalam.

Perhatikan penamaan senyawasenyawa berikut!1) N2O3= di...
Perhatikan percobaan di bawah ini!. Diketahui data potensial reduksi sebagai berikut: E 0 Ca 2+ /Ca = - 2.87V. E 0 Pb 2+ /Pb = -0.13V. E 0 Mg 2+ /Mg = -2.37V.. Struktur lewis dari kedua unsur dalam membentuk suatu senyawa adalah sebagai berikut : Senyawa YX 2 tersebut terbentuk dari sharing.
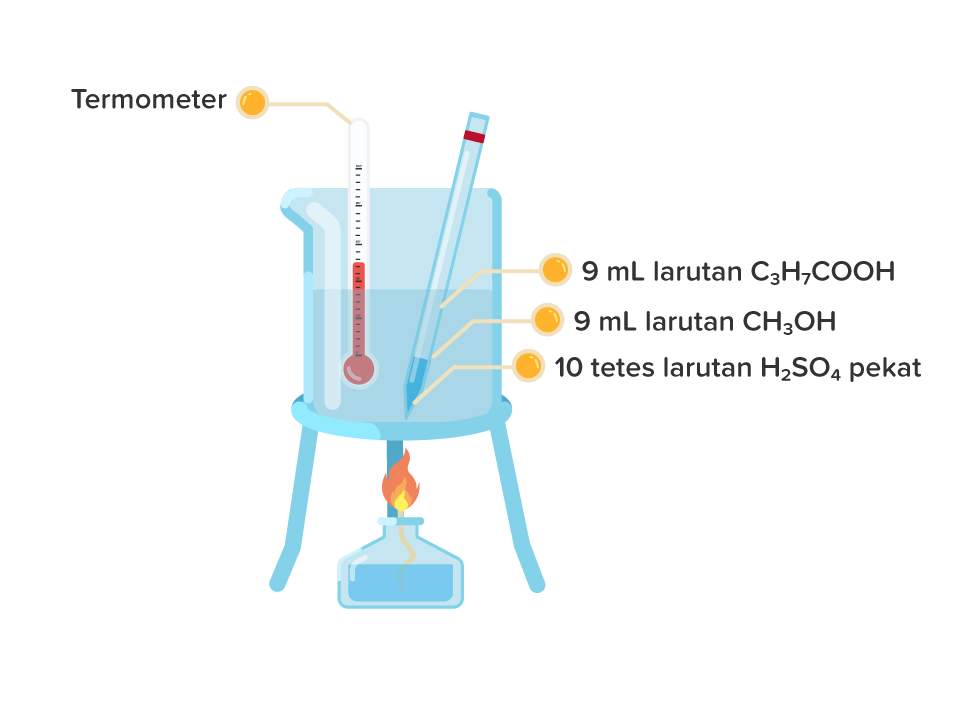
Perhatikan gambar berikut ! Senyawa yang dih...
Kimia Fisik dan Analisis Kelas 10 SMA. Hukum-Hukum Dasar Kimia dan Stoikiometri. Hukum-Hukum Dasar Kimia. Diketahui data percobaan pembentukan senyawa pirit sebagai berikut. Massa besi (Fe) Massa belerang (S) Massa Pirit (FeS2 7 gram 8 gram 15 gram 14 gram 16 gram 30 gram 21 gram 24 gram 45 gram Perbandingan Fe : S adalah..