
Cara Menghitung Ph Larutan Asam Kuat Dan Asam Lemah Panduan Kimia Riset Sexiz Pix
Pertanyaan. Dalam suasana asam, larutan yang mengandung VOn− mengoksidasi logam menurut persamaan reaksi berikut (belum setara): VOn−(aq)+Zn(s) →V2++Zn2+. Sebanyak 9,75 gram logam Zn (Ar=65) tepat habis bereaksi dengan 200 mL larutan 1,5 M yang diperoleh dari pengenceran 40 mL larutan . Konsentrasi larutan sebelum diencerkan adalah..

Kmno Bereaksi Dengan H C O Dalam Suasana Asam Menghasilkan Co Dan My XXX Hot Girl
LAPORAN PRAKTIKUM BIOKIMIA Isolasi Amilum (Pati) pada Kentang (Solanum tuberosum) serta Uji Iodida untuk Amilum dalam Suasana Asam, Basa dan Netral INTAN LOGOR 12301561 ILMU KIMIA SEM 6 SELASA, 06 APRIL 2015 PROGRAM STUDI ILMU KIMIA JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI MANADO 2015 Judul percobaan : Isolasi Amilum (Pati) pada Kentang (Solanum tuberosum.

Cara Menghitung Ph Larutan Asam Basa Garam Beserta Contoh Soal Dan Riset Images and Photos finder
Mengidentifikasi reaksi anilin dengan dalam suasana asam dengan penambahan asam sulfat dengan cara pemanasan. Hasil dan Pembahasan Protein adalah poliamida yang jika dihidrolisis akan menghasilkan asam amino.. , penambahan sebanyak 5 tetes yang berperan sebagai oksidator. Dalam larutan asam kuat, ion dikromat direduksi menjadi kromium (iii.

Reaksi Asam Basa Bagian 1 Materi Larutan Asam Basa Kimia SMA Pojan.id YouTube
Dalam larutan suasana asam 0,56 mol ion VO2^+ tepat habis bereaksi dengan 0,28 mol Sn^2+. jika pada reaksi ini terbentuk ion Sn^4+, maka spesi vanadium - 888863… estywul estywul 27.12.2016 Kimia Sekolah Menengah Atas terjawab • terverifikasi oleh ahli

MENGHITUNG PH ( LARUTAN ASAM & BASA) Belajar Asyik
Contoh Soal Titrasi Lanjutan (Kompleksometri) dan Pembahasan. 1. Pada suatu proses titrasi, 20 mL HCl sebagai sampel diencerkan hingga volumenya tepat 100 mL. Sebanyak 10 mL dari larutan tersebut diambil dan dititrasi dengan KOH 0,1 M. Dari hasil eksperimen ditemukan bahwa peniter berkurang sebanyak 20 mL.

Cara Menentukan Senyawa Bersifat Asam Basa Atau Netral Digunakan
11. Sebanyak 1, 12 gram besi (Ar = 56) dilarutkan dalam asam, dan besi berubah menjadi Fe 2+ kemudian larutan ini di reaksikan dengan dengan larutan KMnO 4 0,125 M menurut reaksi Fe 2+ + MnO 4 - → Mn 2+ + Fe 3+. Maka volume larutan KMnO 4 yang diperlukan adalah A. 16 mL B. 25 mL C. 32 mL D. 40 mL E. 42 mL 12. Diketahui potensial reduksi sbb
PEMBUATAN LARUTAN 1000 ML Na2S2O3 0,1 N DARI PADATAN Na2S2O3 5H2O
Titrasi argentomentri metode volhard harus dalam suasana asam. Oleh karena itu maka ditambahkan larutan asam nitrat 0,5 - 1,5 N ke dalam sampel (analit). Apabila titrasi terjadi dalam suasana basa maka menyebabkan ion besi (III) akan diendapkan menjadi Fe(OH) 3, sehingga titik akhir tidak dapat dicapai.
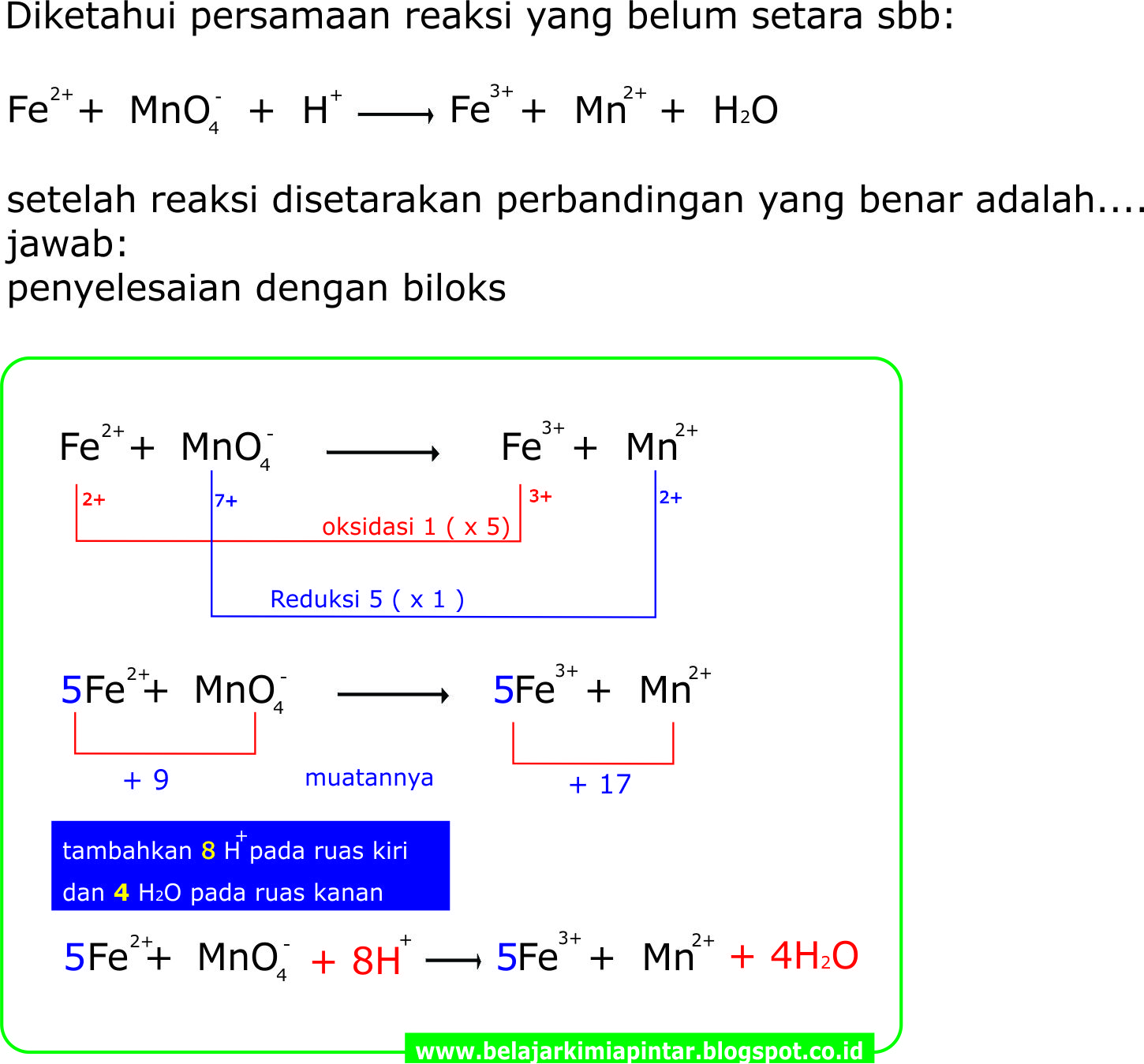
TRIK PENYETARAAN REAKSI REDOKS CARA BILOKS (SUASANA ASAM) KIMIA OKE PINTAR
permanganat dalam larutan asam. Asam yang digunakan adalah asam sulfat encer. Senyawa ini dapat diperoleh dengan tingkat kemurnian yang tinggi, stabil pada saat pengeringan, dan nonhigroskopik. Reaksinya berjalan lambat dalam suhu ruangan, sehingga larutan biasanya dipanaskan sampai sekitar 60 oC, mangan (II) bertindak sebagai katalis 5C 2 O 4

Contoh Soal Penyetaraan Reaksi Redoks Cara PBO Suasana Asam YouTube
Pembahasan Reaksi redoks setara: perbandingan koefisien sama dengan perbandingan mol. Perbandingan mol VO 2 + dan Sn 2 + 0 , 56 mol : 0 , 28 mol 2 : 1 Maka, persamaan reaksinya: Jumlah muatan di ruas kiri dan kanan harus sama: 10 − 2 n = 2 2 n = 8 n = 4 Maka vanadium yang terbentuk memiliki biloks +4, sehingga senyawa yang tepat pada pilihan jawaban adalah VO 2 + .
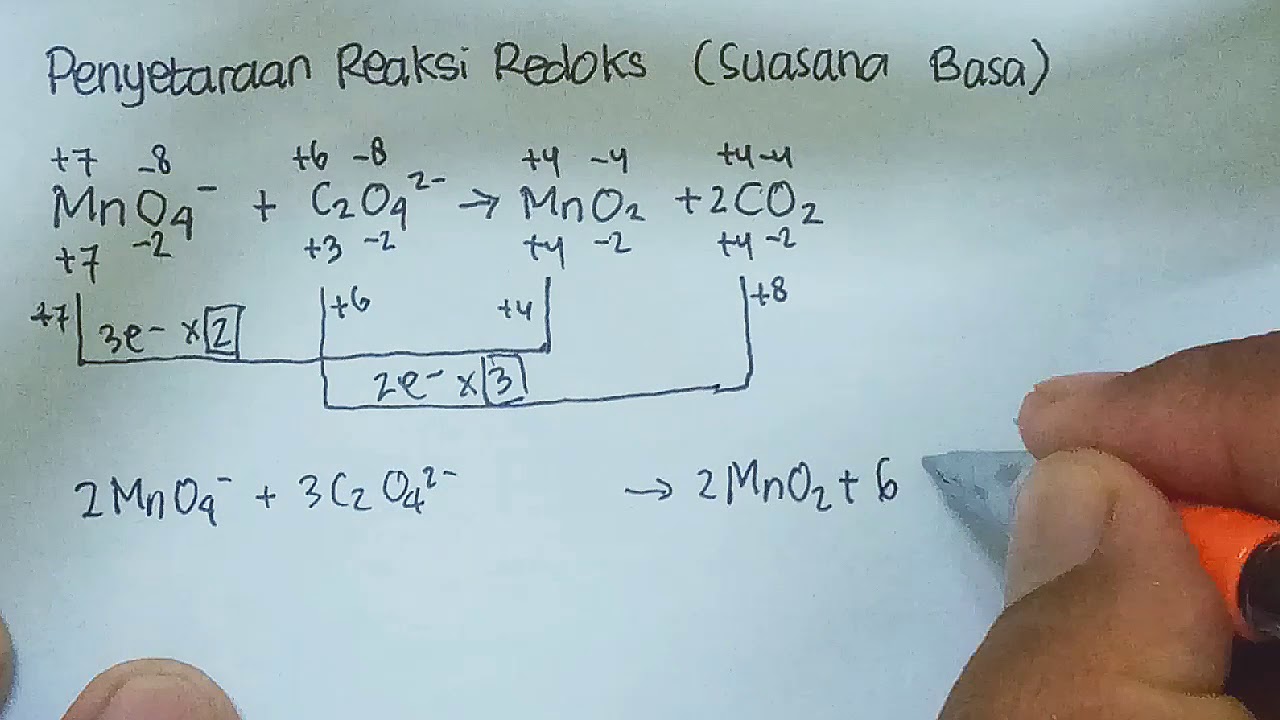
Contoh Soal Penyetaraan Reaksi Redoks Cara Reaksi Suasana Asam Sexiz Pix
Dalam suasana asam besi (II) dititrasi dengan larutan kalium permanganate 0,0206 M, larutan KMnO 4 yang diperlukan 40,20 mL. Hitunglah mg besi dalam larutan tersebut. Penyelesaian : Dalam suasana asam: MnO 4-+ 8H++ 5e → Mn2+ + 4H 2 O x 1 Fe2+ →Fe3+ + e x 5

√ Larutan Asam Basa Teori, Sifat, Jenis dan Indikatornya
Pertanyaan. Sebanyak 1,12 gram besi ( A r Fe = 56) dilarutkan dalam asam, dan besi larut sebagai Fe 2 + . Larutan ini kemudian direaksikan dengan larutan KMnO 4 0,125 M, menurut reaksi (belum setara): Fe 2 + MnO 4 − → Fe 3 + + Mn 2 + Larutan KMnO 4 yang diperlukan adalah.

Reaksi Redoks PK dengan Iodida dalam suasana asam. YouTube
Dalam larutan suasana asam 0,56 mol ion VO 2 + tepat habis bereaksi dengan 0,28 mol Sn 2 + . Jika pada reaksi ini terbentuk ion , Sn 4 + maka spesi vanadium yang terbentuk adalah.. 2. 4.7. Jawaban terverifikasi. Iklan. Iklan. Berapa Faraday yang diperlukan untuk mereduksi bikromat? 80. 0.0.

Penyetaraan reaksi redoks metode setengah reaksi suasana asam YouTube
Dalam suasana asam reaksi dapat dituliskan sebagai berikut: MnO4 - + 8 H+ + 5 e- → Mn2+ + 4 H2O Dengan demikian berat ekivalennya seperlima dari berat molekulnya atau 31,606. Untuk larutan tidak berwarna, tidak perlu menggunakan indikator, karena 0,01 mL kalium permanganat 0,1 N dalam 100 mL larutan telah dapat dilihat warna ungunya.

PERUBAHAN WARNA INDIKATOR KIMIA BUATAN DALAM LARUTAN ASAM DAN BASA YouTube
Dalam larutan suasana asam 0,56 mol ion VO2+ tepat habis bereaksi dengan 0,28 mol Sn2+ Jika pada reaksi ini terbentuk ion Sn4+, maka spesi vanadium yang terbentuk adalah (A) V. Dalam suasana asam, larutan yang mengandung VOn⎻ mengoksidasi logam menurut persamaan reaksi (belum setara)
Soal Larutan Asam Basa
Pertanyaan. Sampel besi karbonat dititrasi dengan larutan kalium permanganat dalam suasana asam sesuai reaksi berikut (belum setara). Fe 2 + + MnO 4 − + 8 H + → Fe 3 + + Mn 2 + + 4 H 2 O Untuk titrasi 20 mL larutan dari pelarutan 50 g padatan sampel besi karbonat dalam 1 L air diperlukan 12 mL kalium permanganat.

Contoh Larutan Asam Dalam Kehidupan Sehari Hari Berbagai Contoh Otosection
Contoh Soal & Pembahasan Reaksi Redoks SBMPTN Kimia SMA. Contoh Soal & Pembahasan. Reaksi Redoks. SBMPTN Kimia SMA. Soal No.1 (UTBK 2019) Diketahui reaksi : 3HOCl + NaI → NaIO 3 + 3HCl. Dalam suatu larutan NaI 0,05 M dan 100 ml HOCl hasil pengenceran dari 5 ml larutan HOCl 3 M. Jumlah mol elektron yang terlibat untuk setiap mol NaI adalah….