[Solved] Have to figure out this equation. The ClausiusClapeyron Equation... Course Hero
http://bit.ly/20202KimiaFisikaIPerubahanKeadaanKomentar video: terlambatSumber:1. PW Atkins. Kimia Fisika Jilid 1 Edisi Keempat. Bab 1. Sifat-sifat gas2..

SOLUTION 3 problem set persamaan clapeyron clausius clapeyron 1 Studypool
Contoh soal di bawah ini menunjukkan bagaimana menentukan energi aktivasi suatu reaksi dari konstanta laju reaksi pada temperatur yang berbeda.. Gunakan Persamaan Clausius-Clapeyron Untuk Memprediksi Tekanan Uap. 09 Dec, 2019. Mengapa Api Itu Panas (dan Seberapa Panas Itu) 21 Nov, 2020. Hitung Kecepatan Akar Kuadrat Partikel Gas.

Clausius Clapeyron Equation ChemTalk
Clausius-Clapeyron. Sumber: Gabriel Bolivar. Gambar di atas menunjukkan persamaan Clausius-Clapeyron sebelum diintegrasikan. Biasanya biasanya diterapkan untuk sistem cair-uap, di mana ΔH uap digunakan dan diinginkan untuk menghitung berapa tekanan uap cairan pada suhu tertentu. Demikian juga, ini digunakan untuk menghitung uap ΔH cairan tertentu dalam kisaran suhu.

SOLUTION 3 problem set persamaan clapeyron clausius clapeyron 1 Studypool
This chemistry video tutorial provides 4 different forms of the clausius clapeyron equation / formula that will help you find the temperature, vapor pressure.

PERSAMAAN CLAUSIUSCLAPEYRON PENENTUAN HARGA ENTALPI DALAM KESETIMBANGAN FASA YouTube
Memprediksi Tekanan Uap. Persamaan Clausius-Clapeyron adalah relasi yang dinamai Rudolf Clausius dan Benoit Emile Clapeyron. Persamaan tersebut menggambarkan transisi fase antara dua fase materi yang memiliki komposisi yang sama. Dengan demikian, persamaan Clausius-Clapeyron dapat digunakan untuk memperkirakan tekanan uap sebagai fungsi suhu.

SOLUTION 3 problem set persamaan clapeyron clausius clapeyron 1 Studypool
In this example problem, we solve for vapor pressure using the Clausius-Clapeyron equation.Determine the vapor pressure in mm Hg of a substance at 45 degrees.
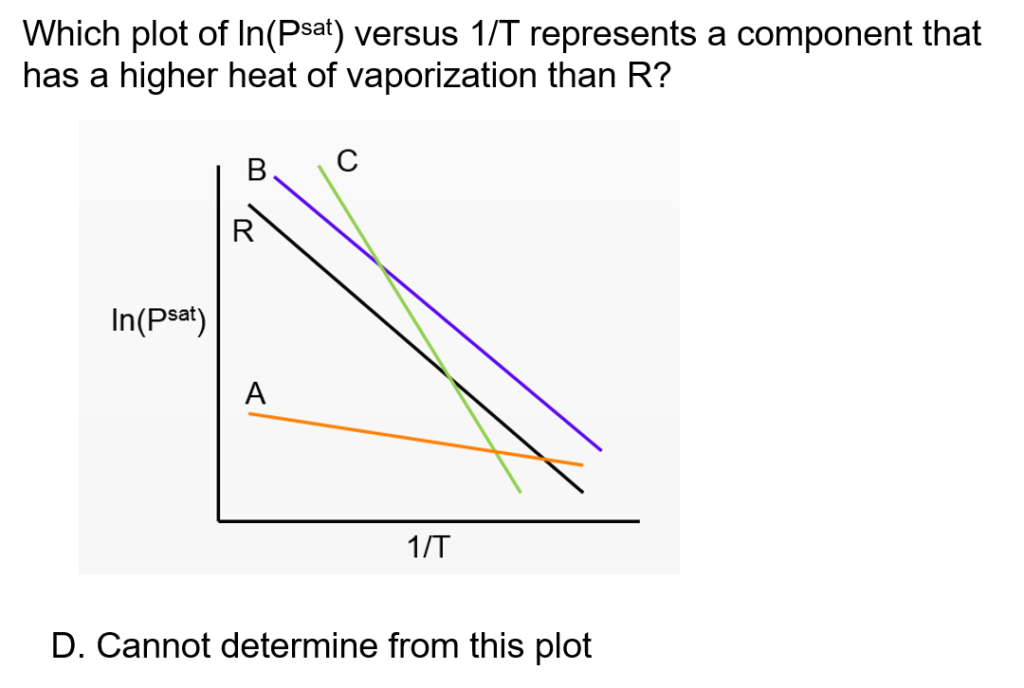
clapeyronclausiusclapeyronandantoineequationsconceptestandexampleproblem LearnChemE
Larutan. Persamaan Clausius-Clapeyron menghubungkan tekanan uap solusi pada temperatur yang berbeda dengan panas penguapan . Persamaan Clausius-Clapeyron diekspresikan oleh. Dalam [P T1, vap / P T2, vap ] = (ΔH vap / R) [1 / T 2 - 1 / T 1 ] dimana. ΔHap adalah entalpi penguapan larutan. R adalah konstanta gas ideal = 0,008314 kJ / K · mol.

Solved Question 17 3 pts When using the Clausius Clapeyron
The Clausius-Clapeyron relation, in chemical thermodynamics, specifies the temperature dependence of pressure, most importantly vapor pressure, at a discontinuous phase transition between two phases of matter of a single constituent. It's named after Rudolf Clausius and Benoît Paul Émile Clapeyron. However, this relation was in fact originally derived by Sadi Carnot in his Reflections on.

PPT ClausiusClapeyron Equation PowerPoint Presentation, free download ID6569609
Persamaan terakhir ini disebut persamaan Clausius-Clapeyron, meskipun beberapa teks termodinamika sebut saja persamaan Clapeyron, mungkin untuk membedakannya dari pendekatan bawah. Ketika transisi adalah fase gas, volume spesifik akhir dapat berkali-kali ukuran volume spesifik awal. Sebuah pendekatan alami akan mengganti Δ v dengan v 2,.

SOLVED ClausiusClapeyron Equation In pz In p1 44(11/ R 71 T2 , Given the normal boiling
Dalam contoh kita di Bagian 1, kita melihat bahwa persamaan Clausius-Clapeyron sangatlah berguna untuk mencari tekanan uap untuk zat-zat murni. Akan tetapi, tidak semua soal akan meminta Anda untuk mencari P1 atau P2 — banyak soal akan meminta Anda untuk mencari nilai suhu atau bahkan terkadang nilai ΔH uap. Untungnya, dalam kasus-kasus ini.

Solved 6. The ClausiusClapeyron equation can be used to
Clausius-Clapeyron Relationship (or equation) (Persamaan Clausius-Clapeyron) adalah persamaan diferensial yang berkaitan dengan tekanan dari suatu zat (biasanya uap air) tehadap suhu dalam sistem di mana dua fase substansi (air) berada dalam kesetimbangan.
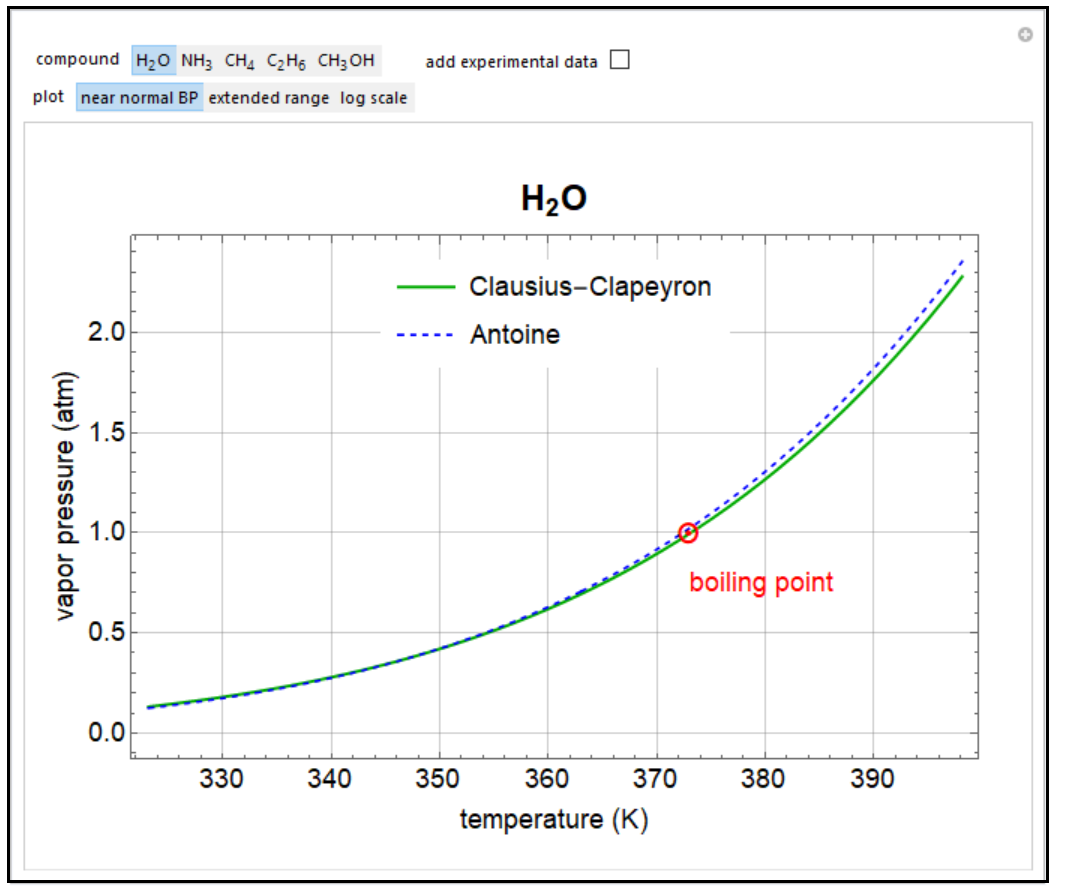
compareclausiusclapeyronandantoineequations LearnChemE
Solution. The enthalpy of sublimation is ΔHsub Δ H s u b. Use a piece of paper and derive the Clausius-Clapeyron equation so that you can get the form: ΔHsub = R ln(P273 P268) 1 268 K − 1 273 K = 8.3145 ln(4.560 2.965) 1 268 K − 1 273 K = 52, 370 J mol−1 Δ H s u b = R ln ( P 273 P 268) 1 268 K − 1 273 K = 8.3145 ln ( 4.560 2.965) 1.

General Chemistry 2 State of Matter ClausiusClapeyron Equation (حساب حرارة التبخر) Lecture 5
Persamaan Clausius-Clapeyron merupakan hubungan penting antara tekanan, suhu, perubahan entalpi dan volume jenis yang terkait dengan perubahan fasa. Persamaan ini didapat dari penurunan persamaan Clapeyron dengan mengasumsikan bahwa uap mengikuti hukum gas ideal dan mengabaikan volume cairan. Persamaan ini digunakan untuk menentukan entalpi proses seperti penguapan, sublimasi dan transisi.

Ejercicio Ecuación de Clausius Clapeyron YouTube
Dalam persamaan Clausius-Clapeyron, suhu dinyatakan dalam nilai skala Kelvin, jadi langkah pertama adalah mengubah suhu dari soal derajat Celcius ke skala Kelvin. Untuk melakukan ini, kita harus menjumlahkan 273,15, lalu T 1 = 287,85 K dan T2 = 325,95 K. Sekarang kita dapat memasukkan nilai dari masalah kita ke dalam persamaan Clausius-Clapeyron.

clausius clapeyron equation
Penyelesaian. Persamaan Clausius-Clapeyron mengaitkan tekanan wap larutan pada suhu yang berbeza dengan haba pengewapan . Persamaan Clausius-Clapeyron dinyatakan oleh. ln [P T1,vap /P T2,vap ] = (ΔH vap /R) [1/T 2 - 1/T 1 ] Di mana: ΔH vap ialah entalpi pengewapan larutan. R ialah pemalar gas ideal = 0.008314 kJ/K·mol.

MT2202 Termodinamika Material Kesetimbangan sistem satu komponen 03 YouTube
Equation 23.4.1 is known as the Clausius-Clapeyron equation. We can further work our the integration and find the how the equilibrium vapor pressure changes with temperature: ln(P2 P1) = − ΔHvap molar R [ 1 T2 − 1 T1] Thus if we know the molar enthalpy of vaporization we can predict the vapor lines in the diagram.