
Memahami Makna Diagram Kesetimbangan Kimia YouTube
Reaksi Kimia dalam Konsep Kesetimbangan. Dikutip dari Modul Paket Keahlian Kimia Kesehatan SMK (2016), dalam konsep kesetimbangan, reaksi kimia berdasarkan sifat berlangsungnya, dibedakan menjadi 2, yakni reaksi satu arah (irreversible) dan reaksi dua arah (reversible). Berikut ini penjelasan dari reaksi-reaksi yang dimaksud tersebut: a.

SOLUTION Rangkuman materi kesetimbangan kimia dan contoh soal serta
Rangkuman materi kesetimbangan kimia kelas XI. Reaksi kesetimbangan kimia adalah reaksi kimia di mana zat-zat hasil reaksi atau produk dapat bereaksi kembali membentuk zat-zat semua atau reaktan. Bisa juga dikatakan, kesetimbangan kimia adalah reaksi kimia yang berlangsung dua arah. Persamaan reaksinya: aA + bB ⇌ cC + dD Pergeseran arah kesetimbangan kimia dipengaruhi oleh beberapa faktor,

SOLUTION Rangkuman materi kesetimbangan kimia dan contoh soal serta
Jenis Kesetimbangan Kimia. Kesetimbangan Kimia Homogen. Reaksi pada kesetimbangan ini terjadi ketika produk dan reaktannya berasal dari fase yang sama, misalnya semuanya gas (g) atau semuanya liquid/cairan (l). Contoh reaksinya: H2 (g) + l2 (g) ↔ 2Hl (g). Kesetimbangan Kimia Heterogen. Reaksi pada kesetimbangan heterogen ini terjadi pada saat.

Soal Kimia SMA Tentang Kesetimbangan Kimia dan Pembahasannya
Sebagai contoh, hukum kesetimbangan kimia untuk reaksi berikut dapat ditulis dalam 2 bentuk: N 2 (g) + 3H 2 (g) ⇌ 2NH 3 (g) atau. atau. Hubungan antara K p dan K c adalah: di mana, R = tetapan gas universal, T = temperatur, dan Δn g = jumlah mol produk gas - jumlah mol reaktan gas. Dalam perhitungan konstanta kesetimbangan reaksi heterogen.

CONTOH SOAL KESETIMBANGAN KIMIA DAN JAWABANNYA PART 2 Rozezisme
Nah itu dia sedikit rangkuman materi kesetimbangan kimia untuk kelas 11! Cek juga catatan lengkapnya disini: CLEARNOTE INDONESIA. Aplikasi berbagi catatan, 100% GRATIS. Tersedia di Indonesia, Jepang, Thailand dan Taiwan. Kesetimbangan kimia ini adalah suatu reaksi kimia dimana hasil reaksi yang dihasilkan dapat diuraikan kembali menjadi zat.

PPT KESETIMBANGAN KIMIA PowerPoint Presentation, free download ID
Latihan Soal Kesetimbangan Kimia (Sukar) Pertanyaan ke 1 dari 5. Pada suhu 300 K ke dalam wadah bervolume 2 L dimasukkan 0,1 mol N2 dan 0,1 mol Cl2 berdasarkan reaksi berikut: H2(g)+Cl2(g) ⇌ 2HCl(g) Jika harga tetapan kesetimbangan KC = 16. Maka jumlah mol dari gas HCl yang diperoleh adalah. .

Kesetimbangan Kimia rangkuman Kesetimbangan Kimia Pendahuluan
Pengertian Kesetimbangan Kimia. Perhatikan reaksi di bawah ini! A + B --> C. Jika A kita ibaratkan sebagai terigu, lalu akan kita campurkan dengan B kita misalkan sebagai telur, maka C kita ibaratkanlah sebagai adonan. A dan B yang posisinya di sebelah kiri panah bolak-balik kita sebut reaktan. Apabila A dan B tadi bercampur membentuk C.

KESETIMBANGAN KIMIA ( KIMIA SMA KELAS 11 ) YouTube
rangkuman kesetimbangan kimia pendahuluan kesetimbangan kimia tetapan kesetimbangan dan cara menyatakanya perhitungan berdasarkan tetapankesetimbangan. Skip to document. 📚

Kimia Kesetimbangan Kimia Terkupas Share & Download
Untuk informasi lebih jelas mengenai kesetimbangan kimia, mulai dari pengertian, jenis, rumus, hingga contoh soalnya, kamu bisa menyimaknya dalam ulasan berikut ini, ya! 1. Pengaruh volume terhadap kesetimbangan. 2. Pengaruh tekanan terhadap kesetimbangan. 3. Pengaruh suhu terhadap kesetimbangan. 4.

Contoh Soal Kesetimbangan Kimia Dan Penyelesaian Nya Soal Kelasmu
1. Kesetimbangan Homogen. Sesuai dengan namanya yang mengandung kata "homogen", kesetimbangan ini merupakan jenis kesetimbangan yang terjadi pada saat produk dan juga reaktan nya berasal dari fase yang sama, yaitu seluruhnya gas (g) atau seluruhnya cairan (aq), seperti di bawah ini. aA (g) + bB (g) ⇄ cC (g) + dD (g)
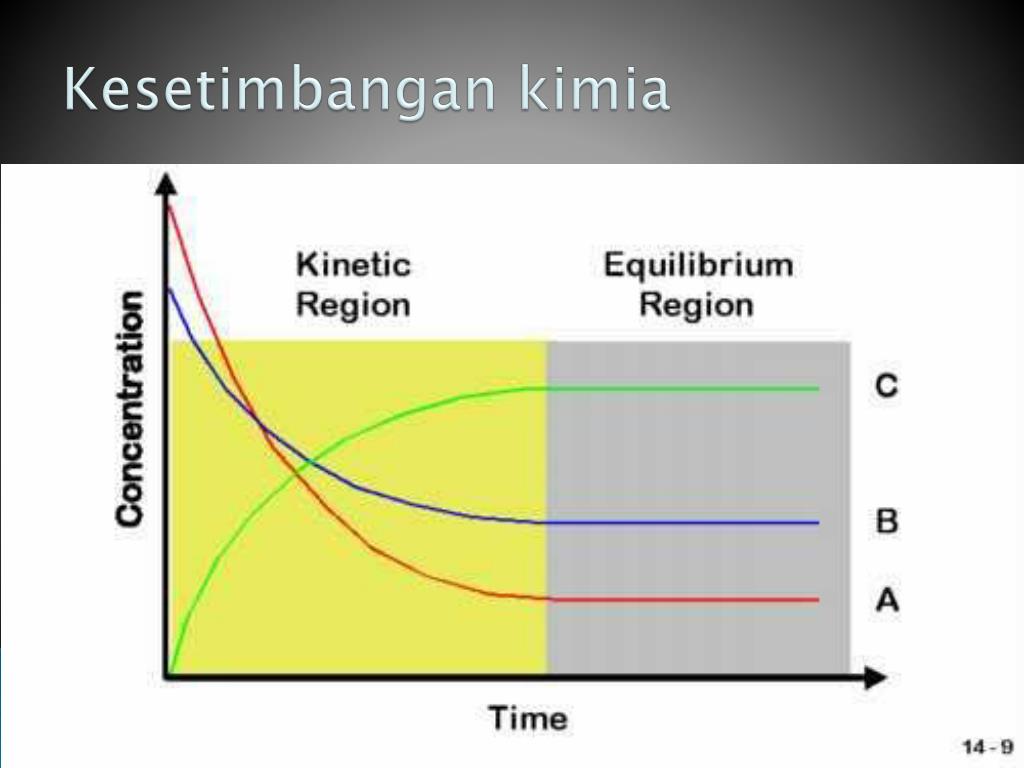
PPT KESETIMBANGAN KIMIA PowerPoint Presentation, free download ID
Contoh Soal Kesetimbangan Kimia. Satu liter campuran gas pada suhu 100°C pada keadaan setimbang mengandung 0,0045 mol dinitrogen tetraoksida dan 0,03 mol nitrogen dioksida. Tuliskan rumus tetapan kesetimbangan gas tersebut. Hitung tetapan kesetimbangannya. Jawab:

PPT Kesetimbangan Kimia PowerPoint Presentation, free download ID
Kesetimbangan Kimia - Konsep, Pergeseran, Tetapan dan Aplikasinya - Di alam sekitar kita banyak terjadi reaksi-reaksi kimia, seperti fotosintesis.. Rangkuman. Kesetimbangan akan terjadi bila suatu reaksi kimia dapat berlangsung dua arah. Pada saat kesetimbangan tercapai, kecepatan reaksi ke kiri adalah sama dengan kecepatan reaksi ke.

Rangkuman Kesetimbangan Kimia Kelas 11 Clear Indonesia News
Pengertian Kesetimbangan Kimia: Konsep Dasar, Faktor dan Contoh Soal. Written by Restu N. Mengenal pengertian kesetimbangan kimia - Kesetimbangan kimia adalah materi pelajaran kimia yang dipelajari di kelas 11 SMA. Sebagai pelajaran IPA ,biasanya Kimia mudah terlupa. Banyak yang mendadak amnesia.

kesetimbangan kimia
Rangkuman Kesetimbangan Kimia Dirangkum dari Modul Pembelajaran SMA Kimia (2020), reaksi kimia dapat dibagi menjadi dua jenis, yaitu reaksi searah dan reaksi dua arah. Reaksi searah bersifat tidak dapat balik atau irreversible, di mana produk tidak dapat berubah kembali menjadi reaktan. Ciri-ciri reaksi searah mencakup persamaan reaksi dengan satu anak panah ke arah produk atau ke kanan (→.

PPT KESETIMBANGAN KIMIA PowerPoint Presentation, free download ID
reaksi kesetimbangan pada reaksi yang dapat balik (bolak-balik): Gambar kiri: N2 + 3H2 -> 2NH3 (N2 dan H2 berkurang sedangkan NH3 bertambah) Gambar kanan: NH3 -> N2 + 3H2 (reaksi kebalikan yang kiri, N2 dan H2 bertambah sedangkan NH3 berkurang) Saran Artikel : Pembahasan kimia erlangga Kesetimbangan kimia Pada kesetimbangan dinamis, setiap pengurangan atau penambahan konsentrasi secara.

8 kesetimbangan kimia
RANGKUMAN MATERI KESETIMBANGAN KIMIA. 1. Pengertian Kesetimbangan Kimia. Kesetimbangan kimia merupakan reaksi bolak-balik yang mana laju reaksi reaktan. dan produk sama dan konsentrasi keduanya tetap. Kesetimbangan kimia hanya terjadi. pada reaksi bolak-balik yang mana laju terbentuknya reaktan sama dengan laju terbentuknya produk.