
Perlukah Menghafal Aturan Bilangan Oksidasi? Urip dot Info
Materi ini bertujuan untuk memahami aturan untuk mencari biloks suatu molekul atau atom dalam senyawa, baik dalam bentuk unsur bebas atau ion, bisa ion biasa.

Biloks H Studyhelp
Bilangan oksidasi. Dalam kimia, bilangan oksidasi, biloks, atau keadaan oksidasi, adalah muatan hipotesis sebuah atom jika semua ikatannya dengan atom yang berbeda sepenuhnya ionik. Bilangan ini menggambarkan tingkat oksidasi (kehilangan elektron) dari sebuah atom dalam senyawa kimia. Secara konseptual, bilangan oksidasi dapat berupa bilangan.

Konsep mudah menentukan biloks Kimia SMA YouTube
Enter the formula of a chemical compound to find the oxidation number of each element. A net ionic charge can be specified at the end of the compound between { and }. For example: ZnCl4 {2-} or NH2NH3 {+}. Enter just an element symbol to show the common and uncommon oxidation states of the element. Use uppercase for the first character in the.
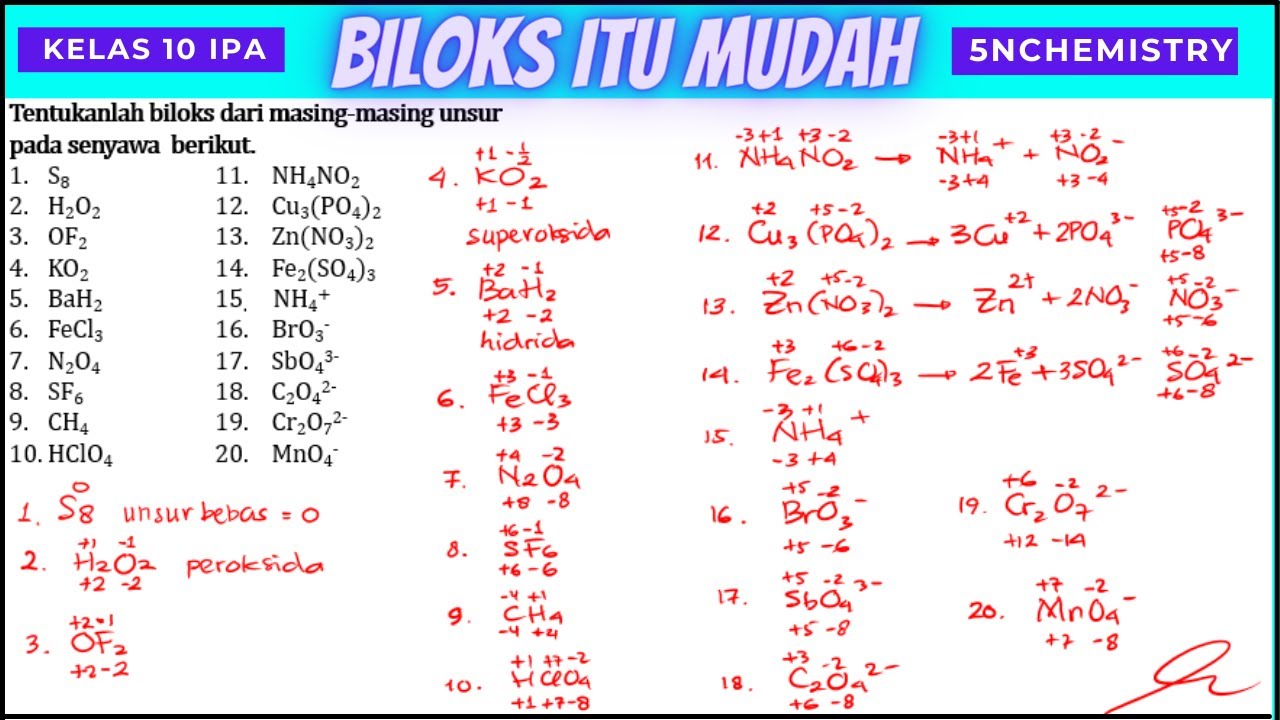
LENGKAP ‼️MENENTUKAN BILOKS UNSUR DALAM SENYAWA YouTube
Bilangan oksidasi atau yang disingkat dengan nama Biloks merupakan istilah kimia, berdefinisi sebagai jumlah muatan negatif dan positif dalam atom, yang secara tidak langsung menunjukkan jumlah elektron yang telah diterima atau diserahkan ke atom lain.Beberapa atom hanya mempunyai satu biloks, namun ada beberapa atom yang mempunyai lebih dari satu biloks.

Aturan Biloks Kls X PDF
Agar jumlah biloks H dan O sama dengan 0, maka biloks O harus bernilai -2. Unsur golongan logam (IA, IIA, IIIA) memiliki biloks = positif sesuai golongannya; Biloks golongan IA = H, Li, Na, K, Rb, Cs, Fr = +1. Contoh: Bilangan oksidasi Na dalam senyawa NaCl adalah +1. Biloks golongan IIA = Be, Mg, Ca, Sr, Ba, Ra = +2.

Biloks & Penyetaraan Reaksi Redoks Metode Setengah Reaksi Reaksi Redoks Kimia Kelas 12 YouTube
Postingan ini membahas contoh soal bilangan oksidasi atau biloks dan pembahasannya / penyelesaiannya. Bilangan oksidasi adalah nilai muatan atom dalam sebuah senyawa atau ion. Ketentuan dalam menentukan biloks sebagai berikut: Atom unsur bebas seperti O2, N2, Fe dan lainnya mempunyai biloks = 0.Atom logam golongan IA (Li, Na, K, Rb, Cs) mempunyai biloks = +1.Atom

3 Contoh Soal Bilangan Oksidasi (Biloks) YouTube
Dalam mata pelajaran Kimia juga ada bilangan yang disebut bilangan oksidasi atau dikenal juga dengan nama biloks.. Bilangan oksidasi Li, K, Rb, Ca, Fr dalam semua senyawanya adalah +1. 6. Bilangan oksidasi unsur-unsur golongan alkali tanah (IIA) dalam berbagai senyawa yang dibentuknya adalah +2.

Biloks Cl dalam KClO 4 adalah
Bilangan Oksidasi Bilangan oksidasi ( biloks ) didefinisikan sebagai jumlah muatan negatif dan positif dalam atom, yang secara tidak langsung menandakan jumlah elektron yang telah diterima atau diserahkan. Atom yang menerima elektron akan bertanda negatif, atom yang melepaskan elektron bertanda positif.. (Li, Na, K, Rb, Cs, Fr), bilangan.

Aturan penentuan biloks
Ingat aturan biloks nomor 5, jumlah bilangan oksidasi unsur yang membentuk ion akan sama dengan jumlah muatannya. Jadi, biloks Cr dan O apabila dijumlah, hasilnya harus -2. Cr 2 O 7 2-Biloks O = -2. Karena atom O memiliki indeks 7, maka biloks O dikalikan dengan indeks O = -2 x 7 = -14. Agar jumlah biloks Cr dan O = -2, maka biloks Cr harus.

PPT Reaksi Redoks PowerPoint Presentation, free download ID7436241
konsep mudah menentukan bilangan oksidasi atau biloks . kimia sma

Reaksi Redoks2 Penyetaraan Reaksi Cara PBO/Biloks & Pembahasan Soal YouTube
Jumlah Biloks Ion Poliatomik → Biloks = Muatannya. Contoh: (SO4) 2-(1 x biloks S) + (4 x biloks O) = -2. Biloks Hidrogen. Jika hidrogen berikatan dengan logam, maka biloks = -1; Contoh: NaH, hidrogen lebih elektronegatif daripada Na, sehingga hidrogen akan menarik elektron dan Na melepaskan elektron. Maka, H bermuatan negatif dan Na bermuatan.

BILANGAN OKSIDASI (BILOKS) YouTube
elektron / Penurunan biloks Reaksi oksidasi : - Reaksi penangkapan oksigen / Reaksi pelepasan elektron / Kenaikan biloks. P 4 b. jumlah biloks atom dalam senyawa netral = 0 c. jumlah biloks atom dalam ion = muatan ion Prioritas biloks : IA : Li, Na, K, Rb, Cs, B = + IIA : Be, Mg, Ca, Sr, Ba, B = +2 Yang atas didahulukan. Al, B = +3.

biloks Cu biloks kimia kelas X YouTube
Prinsip penentuan bilangan oksidasi (biloks) pada atom/ion logam pusat senyawa kompleks tidak beda dengan penentuan biloks unsur dari senyawa lain. Namun yang sering dirasa sulit adalah banyaknya unsur atau spesi dalam senyawa kompleks itu. Bila ingin melihat trik sederhana menghitung biloks unsur pada senyawa umum dapat dilihat di sini.

PENENTUAN BILANGAN OKSIDASI (BILOKS). YouTube
Biloks H = +1. Atom H memiliki indeks 4, maka biloks H dikalikan dengan indeks H = +4. Karena jumlah muatan NH₄+ = +1, maka biloks N haruslah -3, agar ketika biloks N dan H dijumlahkan, hasilnya sesuai dengan jumlah muatannya, yaitu +1. 8. Bilangan oksidasi oksigen (O) dalam senyawa peroksida = -1. Bilangan oksidasi O dalam senyawa non.

Cara Mengerjakan Soal Kimia Biloks Read Master
Biloks atau bilangan oksidasi suatu unsur adalah bilangan yang menunjukkan sumbangan muatan suatu atom unsur pada molekul atau ion yang dibentuknya. Bilangan oksidasi sering disingkat dengan b.o. Bilangan oksidasi suatu unsur pada suatu senyawa umumnya sama dengan jumlah elektron yang dilepas atau dipasangkan oleh satu atom unsur pada senyawa.

Kumpulan Soal Biloks Lembar Soal
Jumlah aljabar bilangan oksidasi seluruh atom-atom dalamsuatu senyawa netral adalah nol(0). Jumlah aljabar bilangan oksidasi seluruh atom-atom dalamsuatu ion adalah sama denganmuatan ion tersebut. Atom-atom golongan lA (Li, Na, K, Rb, Cs, dan Fr) dalamsenyawa selalu mempunyai bilangan oksidasi +1.