
Cara Menentukan Bilangan Oksidasi dan Contohnya
Pada senyawa peroksida, seperti H 2 O 2, Na 2 O 2 dan BaO 2 , bilangan oksidasinya adalah -1. 3. Pada senyawa superoksida, seperti KO 2 dan NaO 2, bilangan oksidasinya adalah -½ . ' Bilangan oksidasi unsur O pada H 2 O, KOH, H 2 SO 4 dan Na 3 PO 4 adalah -2. 7. Jumlah bilangan oksidasi unsur-unsur dalam senyawa adalah 0 (nol).

Cara Menentukan Bilangan Oksidasi yang Mudah, Berikut Penjelasannya
Bilangan oksidasi unsur H pada H 2 O, HCl, H 2 S, dan NH 3 ialah +1. Bilangan oksidasi unsur H pada NaH, CaH 2, dan AlH 3 ialah -1. 6. Bilangan oksidasi unsur O pada senyawanya ialah -2, kecuali :', yaitu: 1. Pada senyawa biner dengan F, bilangan oksidasinya ialah +2. 2. Pada senyawa peroksida, seperti H 2 O 2, Na 2 O 2 dan BaO 2 , bilangan.

Bilangan Oksidasi H Bernilai Negatif Terdapat Pada Senyawa Mobile Legends
Atom H pada AlH 3 berindeks 3, jadi biloks H = -3 dibagi 3 (indeks H) = -1. Jadi terbukti jika bilangan oksidasi H bertemu logam (Al) adalah -1. 8. Bilangan Oksidasi Oksigen (O) adalah -1 dalam Senyawa Peroksida dan -2 dalam Senyama Non-Peroksida. Contoh dari penerapan aturan ini seperti misalnya pada H 2 O 2 (hidrogen peroksida) bilangan.

tentukan bilangan oksidasi setiap atom pada senyawa ion dibawah ini
Bilangan oksidasi adalah jumlah muatan positif atau negatif pada atom. Kenali cara menentukan bilangan oksidasi dan contoh soalnya di sini!. (redoks) yang ketiga, yaitu berdasarkan perubahan pada bilangan oksidasi. Nah, langsung aja kita bahas, yuk! Baca Juga: Apa Itu Reaksi. Sedangkan, Na melepaskan elektron, sehingga bernilai +1. Contoh.

Bilangan oksidasi Mn tertinggi terdapat pada senyawa....
Adapun syarat-syarat dalam menentukan bilangan oksidasi suatu unsur yang sudah menjadi ketetapan adalah sebagai berikut :. Bilangan oksidasi untuk setiap atom unsur adalah nol. contoh : biloks H 2 = 0; Bilangan oksidasi ion adalah sebesar muatan atom tersebut. contoh : biloks H + = +1; Jumlah bilagan oksidasi pada senyawa netral adalah nol dan jika senyawa tersebut memiliki muatan, maka.

Atom Belerang Dengan Bilangan Oksidasi Yang Sama Terdapat Pada Senyawa
Pengertian bilangan oksidasi. Dilansir dari Chemistry LibreTexts, bilangan oksidasi adalah bilangan positif dan negatif yang diberikan pada suatu atom untuk menunjukkan tingkat oksidasi atau reduksinya. Bilangan oksidasi disebut juga sebagai biloks. Perubahan bilangan oksidasi dikarenakan oleh transfer elektron dalam reaksi redoks.
.png)
Unsur Logam Bilangan Oksidasi Bernilai Negatif? Urip dot Info
Jumlah bilangan oksidasi unsur O pada senyawanya adalah -2; Jumlah bilangan oksidasi unsur O pada molekul unsur O 2 adalah 0. Jumlah bilangan oksidasi unsur O pada senyawa biner dengan F adalah +2. Jumlah bilangan oksidasi unsur O pada senyawa peroksidasi adalah -1. Jumlah bilangan oksidasi unsur O pada senyawa superoksida adalah -½.
.png)
Unsur Logam Bilangan Oksidasi Bernilai Negatif? Urip dot Info
8. Bilangan oksidasi oksigen (O) dalam senyawa proksida = -1. Bilangan oksidasi O dalam senyawa non-peroksida = -2. Contoh: Biloks O dalam BaO 2 = -1. Bukti: Atom Ba merupakan unsur logam golongan IIA, sehingga biloks Ba = +2. Jumlah biloks Ba dan biloks O harus 0 (aturan biloks poin 6). Oleh sebab itu, biloks O harus bernilai -2.

Bilangan Oksidasi S Yang Terkecil Terdapat Dalam Lengkap
Kemudian, bilangan oksidasi H pada senyawa 2HCl bernilai +1 sebab unsur H berhubungan dengan unsur lain dan H merupakan golongan dari IA. Selanjutnya, sebab H = +1, maka berarti Cl = -1 supaya jumlah bilangan oksidasi 2HCl = 0. Di ruas sebelah kanan, bilangan oksidasi Mg pada senyawa MgCl yaitu +2 sebab Mg berikatan dan merupakan unsur golongan.

Bilangan oksidasi yang bernilai +1 dan 0 terdapat pada
Contoh senyawa dengan bilangan oksidasi H negatif adalah hidrida logam seperti magnesium hidrida (MgH2), amida (R-NH2), dan alkil hidrida (R-H). Dengan pemahaman tentang bilangan oksidasi H negatif, kita dapat lebih memahami sifat dan reaktivitas senyawa-senyawa tersebut. Bilangan Oksidasi H Bernilai Negatif Terdapat Pada Senyawa.

Bilangan Oksidasi Dan Tatanama
Bilangan oksidasi hidrogen (H) biasanya bernilai positif ketika terdapat dalam senyawa. Namun, ada beberapa kasus di mana bilangan oksidasi hidrogen dapat menjadi negatif dalam senyawa tertentu. Contohnya adalah dalam senyawa yang disebut hidrida logam, di mana hidrogen bertindak sebagai ion H- (hidrida).

6+ Bilangan Oksidasi H Bernilai Negatif Terdapat Pada Senyawa Baru Kursus Digital
UJI KUALITATIF KARBOHIDRAT-Owandity. Pendahuluan Penyusun Karbohidrat adalah C, H, dan O yang terbentuk dari peristiwa fotosintesis pada tumbuhan. atau merupakan suatu senyawa karbon, hidrohen dan oksigen yang terdapat di alam Atau merupakan polihidroksil aldehida, atau keton. Secara umum karbohidrat didefenisikan sebagai senyawa dengan rumus.

Bilangan Oksidasi Unsure MN Terkecil Terdapat Pada Senyawa PDF
1. Bilangan oksidasi unsur bebas adalah 0 (nol) 2. Bilangan oksidasi ion monoatomik sama dengan muatannya. 3. Jumlah bilangan oksidasi semua atom unsur yang terdapat dalam dalam sebuah senyawa adalah 0 (nol) 4. Bilangan oksidasi atom-atom pembentuk ion poliatomik sama dengan muatannya. 5.

Bilangan Oksidasi atom N= 3 terdapat pada senyawa YouTube
Bilangan oksidasi unsur H pada NaH, CaH 2, dan AlH 3 adalah -1. 6. Bilangan oksidasi unsur O pada senyawanya adalah -2, kecuali:' 1. Pada senyawa biner dengan F, bilangan oksidasinya adalah +2. 2. Pada senyawa peroksida, seperti H 2 O 2, Na 2 O 2 dan BaO 2, bilangan oksidasinya adalah -1. 3. Pada senyawa superoksida, seperti KO 2 dan NaO 2.

Harga Bilangan Oksidasi Sama Dengan Nol Terdapat Pada
Sementara unsur yang bilangan oksidasinya negatif biasanya berupa unsur nonlogam seperti Cl, F, O, dan unsur nonlogam lainnya. Selain perbedaan berdasarkan perubahan bilangan oksidasi tersebut, masih terdapat perbedaan lainnya antara reduksi dan oksidasi dalam beberapa poin berikut ini.
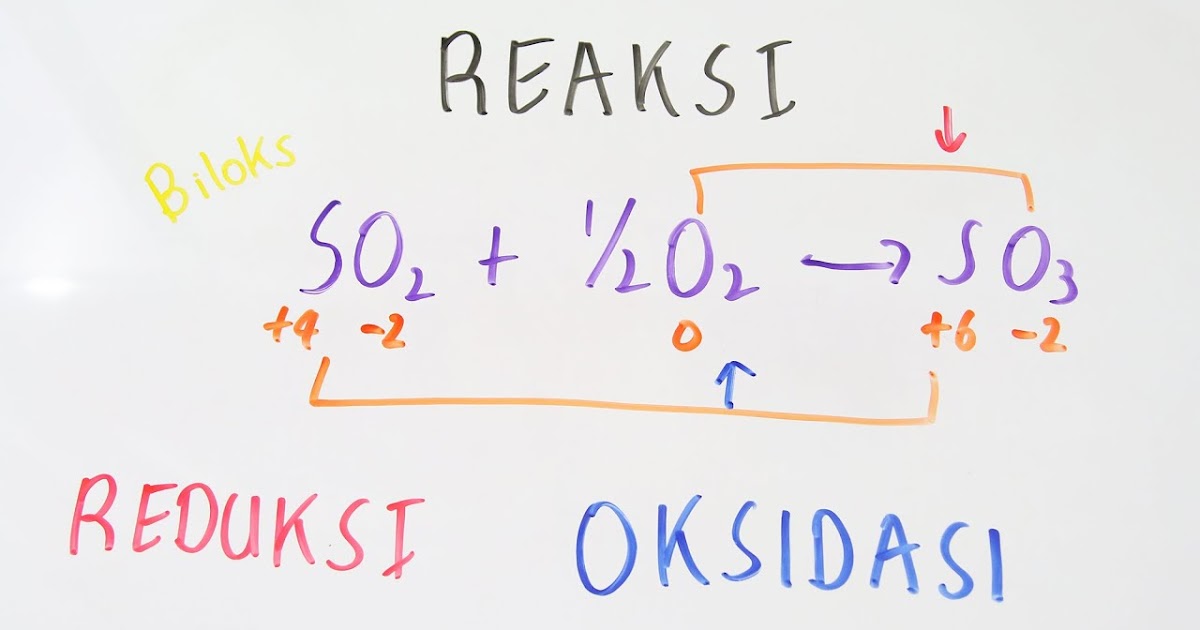
Cara Menentukan Bilangan Oksidasi Dari Unsur Yang Terdapat Di Dalam Senyawa Ion Pejuangtoga
Pada ion OH-, bilangan oksidasi O ditambah dengan bilangan oksidasi H = -1. Pada ion SO42-, bilangan oksidasi S ditambah dengan 4 kali bilangan oksidasi O = -2. Pada ion NH+4, bilangan oksidasi N ditambah dengan 4 kali bilangan oksidasi H = +1. 5. Bilangan oksidasi unsur-unsur golongan alkali (IA) dalam berbagai senyawa yang dibentuknya adalah +1