
Bilangan oksidasi Cr dalamsenyawa K2Cr204 adalah..... *O +3O +4O +5O +6O +75 poinDi antara
Aturan Penentuan Bilangan Oksidasi. Setelah memahami pengertian, Sobat Zenius juga harus tahu aturan biloks. Aturan yang menentukan bilangan oksidasi yang benar adalah: Unsur Bebas → Biloks = 0. Contoh: Na, K, Cl 2, M 2, dan O 2. Logam yang Berikatan dengan Unsur Lain → Biloks = Positif. Contoh: Gol I: Na, K, Rb → biloks = +1
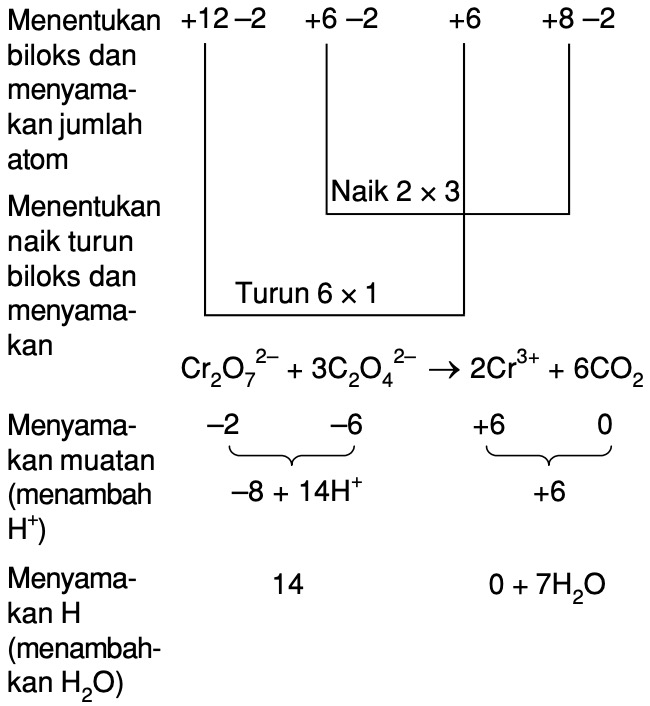
Setarakan Reaksi Berikut Dengan Metode Bilangan Oksidasi Cr O My XXX Hot Girl
Dalam kimia, bilangan oksidasi, biloks, atau keadaan oksidasi, adalah muatan hipotesis sebuah atom jika semua ikatannya dengan atom yang berbeda sepenuhnya ionik.Bilangan ini menggambarkan tingkat oksidasi (kehilangan elektron) dari sebuah atom dalam senyawa kimia.Secara konseptual, bilangan oksidasi dapat berupa bilangan positif, negatif, atau nol. Walaupun ikatan ionik sepenuhnya tidak.

Biloks Cr Pada K2cr2o7 Kondisko Rabat
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Bilangan oksidasi Cr dal.

Bilangan Oksidasi Cr Pada Senyawa K2Cr2O7 Adalah Lengkap
Berikut adalah pengertian, aturan, cara menentukan, dan contoh soal tentang bilangan oksidasi dalam kimia.. Tentukan bilangan oksidasi atom unsur Cr dalam senyawa K2Cr2O7! Jawaban: Muatan K2Cr2O7 = (2 x b.o K) + (2 x b.o Cr) + (7 x b.o O) 0 = 2 x (+1) + 2 x (x) + 7 x (-2) (-2x) = (-12) x = +6. ADVERTISEMENT. Jadi, bilangan oksidasi unsur Cr.

Bilangan Oksidasi S Yang Terkecil Terdapat Dalam Lengkap
Tentukan bilangan oksidasi atom Cr dalam K2Cr2O7 Pembahasan : H2Cr2O7 adalah senyawa netral sehingga jumlah bilangan oksidasi atom penyusunnya = 0.. Bilangan oksidasi adalah harga yang menunjukkan kemampuan suatu atom untuk melepaskan atau menerima elektron dalam suatu reaksi 2. Aturan Penentuan Bilangan Oksidasi : a. Atom H dalam senyawa.

Cara Menentukan Bilangan Oksidasi yang Mudah, Berikut Penjelasannya
Konsentrasi kalium dikromate dapat dihitung dari data kurva standar di peroleh panjang gelombang maksimum 429,6 nm dengan persamaan garis y = 70.25x + 0.005. viskositas kalium dikromat mengalami.

Perubahan berikut yang merupakan oksidasi adalah....A. Cr...
- Bilangan oksidasi H dalam H 2 yaitu 0 - Bilangan oksidasi O dalam O 2 yaitu 0 - Bilangan oksidasi Cl dalam Cl 2 yaitu 0 - Bilangan oksidasi P dalam P 4 yaitu 0 - Bilangan oksidasi S dalam S 8 yaitu 0. 2. Bilangan oksidasi logam dalam senyawa selalu positif. Unsur logam golongan 1 (sistem lama gol. IA) (Li, Na, K, Rb, Cs, Fr.

Cara Menentukan Bilangan Oksidasi dan Contohnya
Aturan dalam Menentukan Bilangan Oksidasi. 1. Bilangan oksidasi unsur bebas adalah 0 (nol) 2. Bilangan oksidasi ion monoatomik sama dengan muatannya. 3. Jumlah bilangan oksidasi semua atom unsur yang terdapat dalam dalam sebuah senyawa adalah 0 (nol) 4. Bilangan oksidasi atom-atom pembentuk ion poliatomik sama dengan muatannya.

Cara mudah menentukan bilangan oksidasi dalam senyawa kimia YouTube
Bilangan oksidasi adalah bilangan yang menandakan jumlah elektron yang diserah / terima oleh suatu unsur. bilangan oksidasi unsur oksigen akan ditulis terlebih dahulu sebesar { -2 } tiap unsurnya dan diikuti unsur - unsur lain berdasarkan golongannya masing - masing.

Contoh Reaksi Reduksi Dan Oksidasi Berdasarkan Perubahan Bilangan Oksidasi Sketsa
Tentukan susunan I, II, atau III (semua molekul adalah CH2Cl2) yang akan mempunyai gaya tarik antarmolekul paling kuat, dan berikan alasan untuk pilihan Anda. Jawaban terverifikasi. Unsur Mn yang mempunyai bilangan oksidasi sama dengan bilangan oksidasi Cr dalam K2Cr2O7 adalah.. A. KMnO4 B. MnO C. K2MnO4 D. MnO2 E. MnSO4.

Bilangan Oksidasi Krom Dalam K2cr2o3 Adalah Kondisko Rabat
Master Teacher. Hallo Anonim, jawabannya biloks Cr = +6. Ayo simak penjelasan berikut agar kamu lebih paham.^^ Berikut adalah beberapa aturan penentuan bilangan oksidasi (biloks): 1. Biloks unsur atau senyawa netral = 0 2. Biloks ion = muatannya 3. Biloks atom H = +1, kecuali atom H yang berikatan dengan unsur golongan IA dan IIA, biloksnya -1 4.

Bilangan Oksidasi Cr Dalam Senyawa K2Cr2O7 Lengkap
Bilangan oksidasi adalah +1 karena merupakan unsur golongan IA, sedangkan bilangan oksidasi dalam senyawa adalah -2. Jumlah bilangan oksidasi setiap unsur dalam senyawa netral adalah nol. Sehingga biloks dalam dapat ditentukan sebagai berikut:. Jadi, jawaban yang benar adalah C.

Bilangan Oksidasi Unsur Cr Dalam Senyawa Na2cr2o7 Adalah Mobile Legends
Strontium merupakan logam alkali tanah dengan tekstur yang lunak dan berwarna putih keperakan kekuningan yang sangat reaktif secara kimiawi. Logam stronsium membentuk lapisan oksida gelap ketika terkena udara. Stronsium memiliki sifat fisik dan kimia yang mirip dengan dua tetangga vertikalnya dalam tabel periodik, kalsium dan barium.

Nilai bilangan oksidasi dari Cr didalam K2CrO4 adalah . . .a. 4b. 5c. 6d. 7e. 8 YouTube
Biloks atau bilangan oksidasi adalah suatu bilangan yang diberikan pada suatu unsur menurut aturan tertentu untuk menyatakan tingkat keteroksidasian atau ketereduksiannya. Beberapa aturan penentuan bilangan oksidasi (biloks) untuk menyelesaikan soal diatas yaitu : - Jumlah biloks dalam senyawa netral = 0

Bilangan Oksidasi Cr Dalam K2 Cr2 O7 Adalah RadarMadiun.co.id
Kalium dikromat, K 2 Cr 2 O 7, adalah suatu pereaksi kimia anorganik yang umum, yang biasa digunakan sebagai agen pengoksidasi dalam berbagai aplikasi laboratorium dan industri. Seperti halnya seluruh senyawa kromium heksavalensi, senyawa ini akut dan secara kronis berbahaya bagi kesehatan. Senyawa ini adalah kristal padat ionik dengan warna merah-jingga yang sangat terang.

Kumpulan Soal Dan Pembahasan Bilangan Oksidasi
Ada 8 aturan dalam menentukan bilangan oksidasi suatu unsur, di antaranya: 1. Bilangan oksidasi unsur bebas adalah 0. Unsur bebas adalah unsur yang tidak bergabung atau berikatan secara kimia dengan unsur lain. Unsur bebas terbagi menjadi dua, yaitu unsur bebas berbentuk atom, seperti C, Ca, Cu, Na, Fe, Al, Ne dan unsur bebas berbentuk molekul.