TEORI ATOM 2 BILANGAN KUANTUM APA YANG DIMAKSUD
Bilangan kuantum digunakan untuk menyatakan tempat kedudukan elektron dalam suatu atom. Terdapat empat bilangan kuantum, yaitu: Bilangan kuantum utama ( n) Menyatakan tingkat energi orbital atau kulit atom. Bilangan kuantum azimut ( l) Menyatakan subkulit atau bentuk orbital. Orbital dinyatakan dengan huruf s, p, d, f, dan seterusnya.

Cara Menentukan Bilangan Kuantum Elektron Terakhir dari Unsur Besi (26Fe) Mekanika Kuantum
Bilangan kuantum spin. Disimbolkan dengan huruf (s) yang menyatakan spin elektron pada sebuah atom. Penjelasan : 1. Bilangan kuantum utama. Bilangan kuantum utama adalah bilangan kuantum primer yang difungsikan untuk menyatakan berapa tingkat energi yang telah dimiliki oleh elektron didalam sebuah atom. Perlu diingat, bahwa bilangan kuantum.

Foto Bilangan Kuantum Spin dan Fungsinya
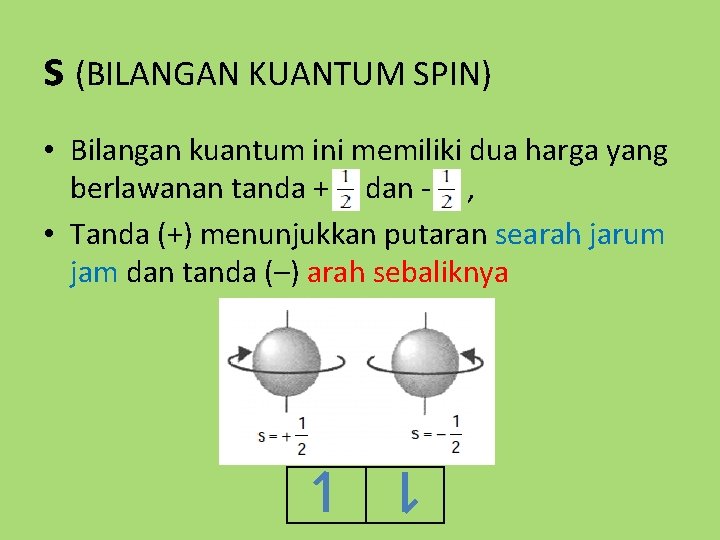
Simbol Bilangan Kuantum Spin. Bilangan kuantum spin menyatakan momentum sudut suatu partikel. Spin mempunyai simbol "s" atau sering ditulis dengan ms (bilangan kuantum spin magnetik). Suatu elektron dapat mempunyai bilangan kuantum spin s = +1/2 atau -1/2. Nilai positif atau negatif dari spin menyatakan spin atau rotasi partikel pada sumbu.
√ 4 Bilangan Kuantum Utama, Orbital, Spin
Bilangan kuantum spin menyatakan arah perputaran atau rotasi pada sebuah sumbu elektron. Arah perputaran bisa searah jarum jam atau berlawanan. Bilangan kuantum spin tidak bergantung dengan bilangan kuantum lainnya. Bilangan kuantum spin ini ditunjukan dengan ± 1/2 atau -1/2. Bilangan kuantum spin positif artinya arah putaran elektron ke atas.

Cara Mudah‼️Menentukan Bilangan Kuantum (Utama, Azimut, Spin) YouTube
Bilangan kuantum (bahasa Inggris: Quantum number) adalah bilangan yang menyatakan kedudukan atau posisi elektron dalam atom yang diwakili oleh suatu nilai yang menjelaskan kuantitas kekal dalam sistem dinamis. Bilangan kuantum menggambarkan sifat elektron dalam orbital.. Bilangan kuantum menentukan tingkat energi utama atau jarak dari inti, bentuk orbital, orientasi orbital, dan spin elektron.

Cara Mencari 4 Bilangan Kuantum
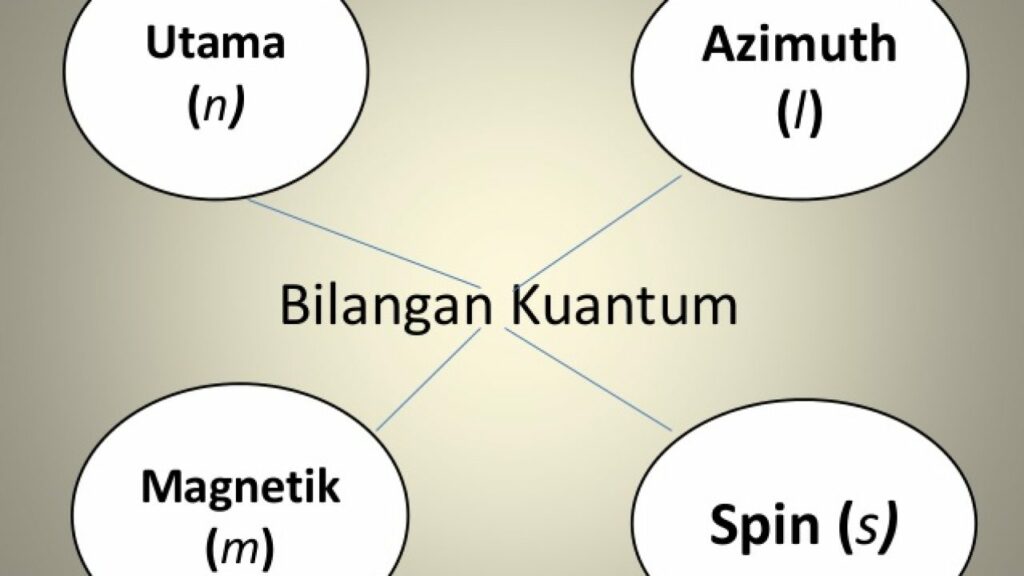
Baca juga: Menentukan Bilangan Kuantum. Elektron tidak mengelilingi atom secara serempak di posisi yang sama, mereka memiliki orbitnya masing-masing dan tidak saling menganggu satu sama lain. Ada empat buah bilangan kuantum yaitu bilangan kuantum utama, azimuth, magnetik, dan spin. Berikut penjelasannya: Bilangan kuantum utama (n)

Kimia kelas 10 bilangan kuantum utama, azimut, dan spin YouTube
Jadi, bilangan kuantum spin mempunyai nilai $+\frac{1}{2}$ atau $-\frac{1}{2}$. Bagaimana menentukan bilangan kuantum? Bilangan kuantum utama dan bilangan kuantum azimut ditentukan dengan melihat konfigurasi elektron terakhir dari suatu atom. Konfigurasi elektron yang dimaksud adalah konfigurasi berdasarkan subkulit atom.

Kimia bilangan kuantum utama, azimut, dan spin YouTube
Yuk, belajar cara mencari bilangan kuantum dengan mudah melalui artikel Kimia kelas X berikut ini! —. Sadar nggak sih, kalau dunia kita ini penuh sekali akan berbagai hal yang teratur dengan rapi. Mulai dari matahari yang terbit dari arah Timur hingga terbenam ke arah Barat. Kemudian, ada bumi yang mengelilingi matahari dalam dua belas bulan.

Bilangan Kuantum Spin Apa Itu? Simak Penjelasannya Berikut Ini!
Certified by Madd Dog Athletics, she has been instructing spin classes for almost two years. A genuine athlete at heart, Jen is passionate about spinning as a vehicle to a healthy mind, body and spirit. She believes that the challenge indoor cycling presents pushes people to test their physical and personal limits. Her philosophies as a coach.

Contoh Bilangan Kuantum Ilmu Kimia
Bilangan kuantum spin menyatakan momentum sudut intrinsik suatu partikel. Spin mempunyai simbol "s" atau sering ditulis dengan ms (bilangan kuantum spin magn.

🔴BILANGAN KUANTUM DAN CARA MENENTUKAN BILANGAN KUANTUM ELEKTRON ATOM YouTube
Sebelumnya kita telah mengetahui tentang teori atom niels bohr yang menyatakan bahwa atom dapat bergerak mengelilingi inti atom pada lintasannya.. Apabila sebuah bil. kuantum memiliki bilangan spin +1/2 maka elektronnya memiliki orientasi spin up. Dibawah ini adalah contoh tabel bilangan kuantum agar kalian lebih memahami tentang bil. kuantum.

Contoh Bilangan Kuantum Panduan Lengkap dan Terperinci
Spin (s) Bilangan ini menyatakan momentum sudut suatu partikel. Spin mempunyai simbol s atau sering ditulis dengan m s (bilangan kuantum spin magnetik). Suatu elektron dapat mempunyai bilangan kuantum spin s = +½ atau -½. Nilai positif atau negatif dari spin menyatakan spin atau rotasi partikel pada sumbu. Sebagai contoh, untuk nilai s.

Konsep Bilangan Kuantum, Cara Memahami dan menyusunnya SainsPedia
Bilangan Kuantum Spin; Bilangan kuantum spin menyatakan spin elektron yang ada pada sebuah atom, bilangan ini disimbolkan dengan huruf 's'. Bilangan kuantum ini menunjukkan arah perputaran atau rotasi pada sebuah elektron terhadap sumbunya. Arah perputaran dapat searah dengan jarum jam ataupun berlawanan dengan arah jarum jam.

Bilangan kuantum Utama, Azimut, dan Spin YouTube
Bilangan kuantum magnetik (m) Menyatakan orientasi orbital dalam subkulit. Nilainya adalah dari -l sampai +l . Contoh: Untuk l=0, maka m= 0. Untuk l=1, maka m= -1, 0, +1. Untuk l=2, maka m= -2, -1, 0, +1, +2. 4. Bilangan kuantum spin (s) Menggambarkan arah rotasi atau putaran elektron dalam satu orbital. Dimana hanya ada 2 arah putaran yang.

journal of dhamar [STRUKTUR ATOM] Bilangan Kuantum dan Bentuk Orbital
Bilangan kuantum utama menyatakan tingkat energi utama elektron suatu atom atau menunjukkan kulit atom. Kalau Sobat Zenius ingat model atom Bohr, bilangan dengan lambang "n" ini melambangkan kulit atomnya, nih. Nah, Sobat Zenius, gue punya rekomendasi video materi singkat yang ngebahas soal bilangan kuantum utama, nih.

26+ Contoh Soal Bilangan Kuantum Spin Frankie Parsons
Bilangan Kuantum Spin (s). Pada pembahasan soal no satu di atas sudah dijelaskan bahwa bilangan kuantum utama menyatakan kulit atom. n = 4 artinya elektron berada pada tingkat energi ke empat atau kulit keempat (kulit N). Jadi agar suatu elektron memiliki nilai bilangan kuantum magnetik (m ) = - 3, maka atom itu harus memiliki setidaknya 4.